Что делать если не знала что беременна и пила антибиотики
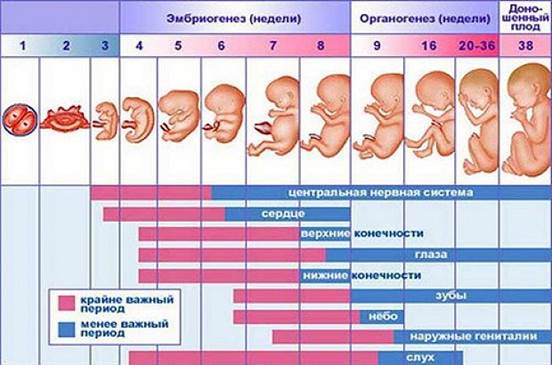
Рис.1 Внутриутробное развитие
Различают 3 вида патологических вариантов воздействия лекарственных средств на развитие плода: эмбриотоксический, тератогенный,фетотоксический. Эмбриотоксическое действие лекарственных препаратов, возникающее в первые 2-3 недели беременности, отмечается в негативном влиянии на зиготу и бластоцисту. Как следствие, может возникнуть гибель плода или морфофункциональные нарушения клеточных систем. Среди препаратов, которые вызывающие эмбриотоксическое действие выделяют противоопухолевые средства, противосудорожные препараты, никотин, эстрогены, гестогены, минералокортикоиды, антибиотики, сульфаниламиды, мочегонные препараты. (Табл. 1) Тератогенные эффекты, возникающие с 3 недели эмбриогенеза, вызывают нарушения биохимического, морфологического и функционального характера. Действие зависит от химической структуры, способности проникать через плаценту, дозировки препарата и скорость выведение лекарства из организма матери. По опасности препараты с тератогенными эффектами делятся на 3 группы: препараты, высоко опасные для плода, их употребление категорически запрещается даже за 6 месяцев до беременности, лекарства с определенной тератогенной опасностью, препараты, вызывающие отклонения при наличии определенных условий, например, высокий возраст беременной женщины, дозы применяемых лекарств [6]. Препараты с тератогенными эффектами являются наиболее опасными, так как они действуют на плод во время гистогенеза и органогенеза. Таким образом нарушение дифференцировки тканей может привести к порокам опорно-двигательной системы, а также внутренних органов. К таким средствам относятся: противоэпилептические средства, препараты половых гормонов, антибиотики, антикоагулянты, анальгетики, антидепрессанты, противомалярийные и противоопухолевые средства. Также известно, что прием ретиноидов, которые оказывают тератогенный эффект, вызывал врожденные аномалии развития, даже если курс лечения был завершен до начала беременности. (Табл. 1) [2,7]. Фетотоксическое действие наблюдается с 14-ой по 38-ую неделю беременности. Вызывают дисфункцию жизненно-важных систем органов. Примеры препаратов: аминогликозидные антибиотики, бета-адреномиметики и т.д. ( Табл. 1) [2,7] Лекарственные препараты проникают в организм плода через систему «мать-плацента-плод». Безусловно, самым важным органом во время беременности является плацента. Она служит своеобразным барьером между организмом матери и плода. Изначально толщина плаценты достигает 25мкм, но ближе к завершению беременности плацента становится заметно тоньше, ее толщина достигает 2 мкм. Этот факт способствует более легкому проникновению лекарств через плацентарный барьер в кровь плода. Также на ослабление плацентарного барьера влияют различные заболевания, например, сахарный диабет. Способность к проникновению различных веществ через плаценту обусловлена различными факторами, среди которых морфофункциональное состояние плаценты, плацентарный кровоток, физико-химическая характеристика лекарственных веществ и т.д. Известно, что большей проницаемостью через плаценту обладают низкомолекулярные вещества. Проникновение различных веществ через плаценту возможно различными путями, среди которых пиноцитоз, диффузия, активный транспорт. После проникновения лекарственного препарата происходит его дальнейшее попадание в пупочную вену, поэтому препарат достигает главных органов, например, сердце и мозг, минуя печень. Также важной проблемой является то, что некоторые препараты могут несколько раз циркулировать по организму плода, вызывая у него больший риск возникновения аномалий и пороков [8].
Таблица 1. Влияние лекарственных препаратов на развитие плода в первом, втором и третьем триместре беременности [4,5,9].
Антибиотики в первом триместре беременности
Антибиотики подавляют размножение бактерий — причину инфекционных заболеваний. Обычно врачи стараются избегать их назначения во время беременности, особенно в 1 триместре, но к сожалению, бывает и так, что без них не обойтись. В каких случаях их прием оправдан? Могут ли они негативно влиять на ребенка? Каковы последствия антибактериального лечения? Постараемся ответить на все эти вопросы, развеять страхи и предубеждения.
В каких случаях не обойтись без антибактериальной терапии
Во время беременности иммунная защита организма ослабевает. Это естественный механизм, который помогает сохранить плод, ведь он является чужеродным элементом для иммунной системы. Поэтому женщина в период вынашивания не застрахована от болезней и даже более того — находится в группе риска по ОРВИ и другим инфекционным заболеваниям. Без приема антибиотиков не обойтись при таких патологиях, как:
В отсутствие должного лечения здоровье и жизнь женщины находятся под угрозой. Поэтому применение антибактериальной терапии оправдано. Она необходима также в реабилитационный период после операционных вмешательств при беременности, а также кесарева сечения. Препараты подбирают, учитывая уровень опасности для женщины и ребенка, срок беременности, фактор лактации и др.
Почему опасны антибиотики при беременности в 1 триместре
С 1 по 12 неделю закладываются и формируются все органы ребенка: сердце, мозг, легкие, печень, щитовидная и поджелудочная железа, зачатки рук и ног, половых органов, пищеварительная, дыхательная и кровеносная системы.
Именно поэтому, если есть возможность, врач всегда попробует отложить антибактериальное лечение на 2 или 3 триместры, заменяя его симптоматической терапией или лекарствами местного действия. Прием антибиотиков в 1 триместре оправдан, если польза от них превышает возможные риски. Ведь плацента еще не сформирована, а значит эмбрион не защищен от негативного влияния препаратов.
Бесконтрольное употребление антибиотиков оказывает токсическое действие и может вызывать:
Поэтому подбирать антибиотик может только врач после тщательной диагностики и анализа на чувствительность к тому или иному антибактериальному средству. Кроме того, среди всего многообразия препаратов можно выбрать те, что разрешены к использованию при беременности.
Какие антибиотики можно беременным в I триместре
Все лекарственные средства проходят специальные исследования на безопасность, по результатам которых их можно разделить на 5 групп:
Среди антибиотиков нет тех, что относились бы к группе А. Поэтому во время вынашивания специалист может назначить препараты группы В или С. К ним относят пенициллины, цефалоспорины и макролиды.
Список разрешенных в 1 триместре антибиотических препаратов
| Пенициллины | Цефалоспорины | Макролиды | |
|---|---|---|---|
| Препараты | Азлоциллин, Амоксициллин, Ампициллин, Оксациллин | Цефуроксим, Цефазолин, Цефотаксим, Цефаклор, Цефепим | Эритромицин, Азитромицин, Джозамицин |
| Категория безопасности | B | B | B |
| Против чего эффективны | Стафилококки, энтерококки, стрептококки, листерии, клостридии и обусловленные ими менингит, сальмонеллез, инфекции кожи, воспаления миндалин, бронхов. | Менингит, инфекции мочевыводящих и дыхательных путей, сепсис, поражения кожи. | Кожные патологии, пневмония, хламидиоз, гонорея, микоплазмоз, хеликобактерная инфекция на фоне язвы желудка, токсоплазмоз. |
| Как влияют на плод | Проникают через плаценту, но не повреждают органы и системы плода. | Способны проходить через плаценту в низких концентрациях, не опасных для будущего малыша. | Нет данных об увеличении числа врожденных аномалий. |
| Побочные эффекты у беременной | Анемия, аллергия, головная боль, нарушения стула. | Рвота, диарея или запор, холестаз, анемия, лейкопения. | Аллергическая реакция, расстройства желудка, дисфункция печени, тошнота и рвота. |
Пенициллины высоко эффективны против стафилококков и используются при подготовке к операциям с профилактической целью. 3 и 4 поколение цефалоспоринов хорошо справляются с гонококками, пневмо- и менингококками, успешно используются специалистами для лечения женщин при беременности и в реабилитационный период после кесарева сечения, поскольку не влияют на лактацию.
Джозамицин незаменим для лечения хламидиоза, гонореи и сифилиса у беременных. Эритромицин — единственный не проникающий в грудное молоко, поэтому абсолютно безопасен при грудном вскармливании.
Выбор средства зависит от результатов анализа на чувствительность к антибиотикам. Только в экстренных случаях возможен прием препаратов широкого спектра действия.
Что строго запрещено
Категорически нельзя включать в лечение заболеваний до 12 недели вынашивания следующие группы антибиотиков:
Данные антибиотики в первом триместре беременности могут вызывать самопроизвольное прерывание, замирание плода и генетические мутации. Их прием в более поздние сроки не вызовет гибель ребенка, но спровоцирует серьезные нарушения здоровья новорожденного.
Многие препараты не разрешены к использованию у беременных, потому что не проводилось контролируемых исследований относительно их безопасности. Это Нитрофураны, Хинолоны, Гликопептиды.
Я принимала антибиотики, когда не знала, что беременна: что делать
Вероятнее всего, это произошло до 3-4 недели гестации. В эти сроки точно предугадать эффект от антибиотиков сложно. С одной стороны, плацента еще не сформирована, и эмбрион беззащитен перед воздействием негативных факторов. Но в то же время он еще развивается вне общего с матерью кровотока, поэтому антибиотик просто не может до него «добраться».
В любом случае это не повод для прерывания желанной беременности. Однако рекомендуем все же сообщить о лечении врачу, сделать дополнительное УЗИ и сдать тест на ХГЧ, чтобы выявить возможные нарушения в динамике развития эмбриона.
Планирование беременности после антибиотических препаратов
Если женщина или ее партнер проходили антибактериальную терапию, то зачатие следует отложить на 3 месяца. За этот время остатки лекарственных средств полностью выйдут из организма, иммунитет окрепнет, и беременность будет протекать без осложнений.
О чем еще не забыть
Еще раз напомним, что самостоятельный подбор и прием антибиотиков в период вынашивания недопустим! Чтобы не навредить себе и своему будущему ребенку, по вопросам подбора любых лекарственных средств обязательно проконсультируйтесь с гинекологом, наблюдающим беременность.
акушер-гинеколог, гемостазиолог, профессор, доктор медицинских наук, эксперт международного уровня по проблемам тромбозов и нарушений свертывания крови
Беременность и инфекции мочевыводящих путей (ИМВП)
Во время беременности инфекции мочевыводящих путей (ИМВП) встречаются не редко. К урологам обращаются женщины как впервые столкнувшиеся с этой ситуацией, так и с обострением хронического, ранее существовавшего, заболевания.
Беременные более уязвимы для инфекций мочевыводящих путей, так как организм женщины испытывает состояние физиологического иммунодефицита, из-за чего он становится более восприимчивым к различного рода инфекционным факторам. И мочевыделительная система не в последнюю очередь подвергается воспалительным процессам, особенно если до беременности не пролечены все хронические заболевания.
Второй момент, влияющий на ИМВП – это увеличивающаяся в размерах «беременная» матка, которая по мере своего роста начинает сдавливать мочеточник (больше правый), вызывая тем самым нарушение оттока мочи. По УЗИ в этом случае можно увидеть каликопиелоэктазию – расширение чашечек и лоханок почек. Это является физиологическим состоянием, но оно может способствовать развитию инфекции.
Существует несколько состояний, характеризующий ИМВП при беременности:
Вопрос, который задают очень часто: «Зачем мне пить антибиотики, если я себя хорошо себя чувствую?»
– Да, конечно, симптомов ИМВП может не быть, но наличие большого титра бактерий в моче может в дальнейшем осложнить течение родов и послеродового периода, вплоть до преждевременных родов и внутриутробной инфекции плода, а также развиться в «явную» форму ИМВП уже с наличием симптоматики!
Хотелось бы также отметить, что не стоит бояться антибиотиков (часто после упоминания о них женщины начинают переживать) и их возможного воздействия на ребенка. Есть определенный перечень допустимых антибактериальных препаратов в разные триместры беременности!
В первом триместре допускается использование: защищенных пенициллинов (Ампициллин, Амоксициллина/клавулонат, Амоксициллин/сульбактам), Фосфомицина трометалол (Монурал) (можно использовать во всех триместрах), макролидов (Джозамицин, Азитромицин). Во втором и третьем триместре: к первому списку добавляются цефалоспорины третьего поколения (Цефиксим, Цефтриаксон, Цефотаксим, Цефтазидим). Но помните, что прием тех или иных препаратов, а при беременности особенно, должен быть только по назначению врача.
Кроме антибиотиков во время беременности часто назначаются растительные уроантисептики (Фитолизин, Канефрон, Цистон и др.) в качестве поддерживающей терапии наряду с антибактериальными препаратами. Довольно часто гинекологи назначают их как профилактической средство, порой на все время беременности. Но злоупотреблять ими не следует, а тем более принимать самостоятельно без рекомендации врача, так как они могу способствовать образованию оксалатных камней при длительном непрерывном приеме, особенно если уже есть нарушения минерального обмена, как иногда говорят, «песок» в почках по УЗИ. Принимать их следует курсами с перерывами, длительность курсового приема определяется только врачом!
К сожалению, порой обычная антибиотикотерапия оказывается не эффективной (особенно при хронических процессах) и приходится прибегать к инвазивным методикам, таким как цистоскопия с последующими инстилляциями в мочевой пузырь. Цистоскопия, а также инстилляции в мочевой пузырь, проводятся только по строгим показаниям, только в тех случаях, когда без них действительно не обойтись! Но иногда приходится прибегать к этим методам при беременности, поэтому не следует удивляться, если врач вам будет назначать вышеописанные исследования и процедуры.
Подготовка к беременности при инфекционной патологии репродуктивной системы женщин
Внедрение современных технологий в клиническую практику позволило расширить исследования и показать, что отрицательное воздействие факторов внешней среды на микрофлору макроорганизма ведет к разнообразной патологии как воспалительного, так и невоспалительного генеза.
Несмотря на значительные успехи, достигнутые в диагностике, терапии и профилактике инфекций, передаваемых половым путем, их частота не имеет отчетливой тенденции к снижению. Последнее связано также с ростом иммунодефицитных состояний на фоне ухудшения экологической обстановки, неправильного питания, частых стрессов, фармакологического бума с бесконтрольным применением лекарственных средств, в первую очередь, антибиотиков и др. Чаще всего половая инфекция бывает обусловлена несколькими патогенными факторами — вирусами, микробами, грибами, простейшими, которые вызывают похожие по клиническому течению, но различные по патогенезу и методам лечения заболевания.
Участие в формировании воспалительных заболеваний органов малого таза, сопровождающихся не только дисбиозом влагалища, но и аналогичными изменениями со стороны желудочно-кишечного тракта и мочевыделительной системы; психоэмоциональные нарушения; формирование иммуно- и интерферонодефицитных состояний — вот далеко не полный перечень проблем, характерных для пациенток с урогенитальными инфекциями. Эти особенности одновременно являются предгравидарным фоном, который не в состоянии обеспечить развитие адекватных компенсаторно-приспособительных реакций, необходимых для гестационного процесса у большинства этих больных.
Однако работы, посвященные вопросам подготовки к беременности женщин с бактериальной и/или вирусной инфекцией, крайне малочисленны и направлены, как правило, на коррекцию отдельных звеньев патологического состояния.
Исходя из вышеизложенного, важнейшим и неотъемлемым этапом является правильная предгравидарная подготовка женщин. Поэтому проведение мероприятий по борьбе с инфекцией необходимо начинать до наступления беременности.
Этапы мероприятий по борьбе с инфекцией
3. Проведение комплексного лечения, которое должно включать как этиотропные виды терапии (комплекс антибактериального или противовирусного лечения), так и лечение сопутствующих заболеваний.
4. Планирование и подготовка к беременности.
При выявлении герпес-вирусной инфекции, проводится ее лечение с последующей профилактикой рецидивов.
При генитальной герпетической инфекции, независимо от уровня поражения репродуктивной системы, показано проведение как базисной (противовирусной) терапии, так и лечение сопутствующих заболеваний.
Базисные виды лечения
Наиболее современным и эффективным противовирусным препаратом является валацикловир. Валацикловир представляет собой пролекарство — L-валиновый эфир ацикловира. После всасывания в кровь валацикловир почти полностью превращается в ацикловир под влиянием печеночного фермента валацикловир-гидролазы.
а) Образовавшийся ацикловир проникает в пораженные вирусом клетки, где под влиянием вирусного фермента тимидинкиназы превращается в монофосфат, затем — в дифосфат и активный трифосфат. Трифосфат ацикловира угнетает ДНК-полимеразу и тем самым нарушает репликацию ДНК вируса простого герпеса. Следовательно, высокая избирательность валацикловира в отношении тканей, пораженных вирусом, объясняется тем, что первый этап цепи реакций фосфорилирования опосредуется ферментом, вырабатываемым самим вирусом. Валацикловир назначают по 0,5 г 2–3 раза в день в течение 5–10 дней. Длительность и дозу препарата подбирают индивидуально с учетом формы и тяжести вирусного заболевания.
б) На фоне блокады репликации вируса — стимуляция неспецифической резистентности организма в зависимости от показателей иммунного и интерферонового статуса больных (препараты иммуноглобулина, индукторы интерферона, энзимотерапия и др.).
в) Одновременное или последовательное использование специфического противогерпетического иммуноглобулина по 3,0 мл внутримышечно 1 раз в 3–5 дней, на курс 5 инъекций.
г) Стимуляция специфической резистентности организма (при условии увеличения межрецидивного периода в 1,5–2 раза) герпетической вакциной по 0,25 мл внутрикожно в руку 1 раз в 3 дня (всего 5 инъекций), после чего перерыв в лечении 2 недели и затем еще 5 инъекций по 0,25 мл 1 раз в 7 дней. Курс ревакцинации — через 6 месяцев.
д) Местное применение специфических мазей (зовиракс, алпизарин, мегосин, бонафтон).
При диагностике цитомегаловирусной инфекции проводится этиотропная противовирусная терапия. Четких рекомендаций по профилактике и лечению ЦМВ-инфекции нет. Идеальный противовирусный препарат должен иметь высокую клиническую эффективность, селективность по отношению к вирусу, полную безопасность для организма человека, вирусоцидное действие. Из-за отсутствия в настоящее время препаратов, которые полностью отвечали бы вышеуказанным требованиям по отношению к ЦМВ, профилактика и лечение данной инфекции представляет определенные трудности. Обязательной является коррекция показателей иммунитета, интерферонового статуса.
При ЦМВ-инфекции рекомендуют проводить курсовую пассивную иммунизацию противоцитомегаловирусным иммуноглобулином по 3 мл внутримышечно 1 раз в 3 дня, на курс 5 инъекций. Более эффективен нормальный человеческий иммуноглобулин по 0,25 г/кг через день внутривенно капельно, 3 введения на курс. Можно назначать иммуномодуляторы (Т-активин, циклоферон, иммунофан), критерием их эффективности служит положительная динамика показателей клеточного звена иммунитета. Применяют также цитотект (в виде 10% раствора иммуноглобулина с высоким содержанием анти-ЦМВ IgG) внутривенно капельно по 2 мл/кг каждые 2 дня до 8–10 раз под контролем серологических показателей.
Перспективно использование интерферонов — виферона по 0,5–1 млн. МЕ 2 раза в день в ректальных свечах в течение 15–20 дней. В профилактику и лечение ЦМВ-инфекции целесообразно включать системную энзимотерапию (вобэнзим по 5 драже 3 раза в день или флогэнзим по 2–3 таблетки 3 раза в день за 30 мин до еды в течение 1–1,5 месяца). Помимо лечения герпес-вирусной инфекции, показано проведение дополнительной терапии. Лечение скрыто протекающего хронического воспалительного процесса в эндометрии (вирусно-бактериальной этиологии) должно проводиться на фоне базисной терапии и быть этиотропным и патогенетически обоснованным. Учитывая превалирование анаэробно-аэробных ассоциаций, а также мико-, уреаплазменной и хламидийной инфекций, показано использование антибиотиков широкого спектра действия.
При обнаружении урогенитального хламидиоза, микоплазмоза и уреаплазмоза назначают: спирамицин по 1 таблетке (3 млн. МЕ) 3 раза в день в течение 5–7 дней; джозамицин по 500 мг 3 раза в сутки в течение 5–7 дней; азитромицин по 1 капсуле (250 мг) 1 раз в день в течение 6 дней.
Этиотропную терапию при инфекционной патологии репродуктивной системы целесообразно сочетать с использованием антиоксидантов — аскорбиновой кислоты (витамин С) по 50 мг и витамина Е по 100 мг 3 раза в сутки. Возможно также использование эфферентных методов лечения (плазмаферез, эндоваскулярное лазерное облучение крови).
Особое внимание следует уделять восстановлению микроэкологии половых путей, так как к осложнениям гестационного периода и родов, связанным с различными нарушениями микроценоза влагалища, относят угрозу прерывания, самопроизвольные выкидыши, преждевременные роды, хориоамнионит, несвоевременное излитие околоплодных вод, рождение детей с малой массой тела, хронической гипоксией и/или признаками внутриутробной инфекции, в послеродовом периоде возникновение раневой инфекции родовых путей, эндометрита.
Нарушение микроценоза влагалища наиболее часто связано с бактериальным вагинозом и/или кандидозной инфекцией. По данным литературы, 75% женщин репродуктивного возраста имеют, по крайней мере, один эпизод вагинального кандидоза. В настоящее время известно 196 видов грибов рода Candida. Из них со слизистых оболочек человека выделяют более 27 видов. По сводным данным, Candida albicans обнаруживают в кишечнике у 20–50% здоровых людей, на слизистой оболочке полости рта — у 20–60%, во влагалище — у 10–17% небеременных женщин.
Вагинальный кандидоз у беременных встречается в среднем в 30–40% случаев. Перед родами этот показатель может достигать 44,4%. Цель лечения бактериального вагиноза и вагинального кандидоза – восстановить нормальную микрофлору влагалища, задержать рост микроорганизмов, несвойственных этому микроценозу. Существует множество препаратов и схем лечения дисбиозов влагалища. Однако нет оптимального препарата, который бы отвечал всем требованиям и имел стопроцентную эффективность.
При бактериальном вагинозе применяют следующие препараты: далацин вагинальный крем (2% вагинальный крем, содержащий 100 мг клиндамицина фосфата) 1 раз в сутки в течение 3 дней или тантум роза — вагинальный душ — 2 раза в сутки в течение 7–10 дней.
Препараты для лечения вагинального кандидоза подразделяются на следующие группы:
1. Антибиотики (нистатин, леворин, натамицин, амфотерицин В).
2. Имидазолы (клотримазол, кетоконазол, миконазол).
3. Триазолы (флуконазол (Дифлюкан, Фунголон), итраконазол).
4. Комбинированные препараты (полижинакс, клион Д, пимафукорт, макмирор комплекс).
5. Другие препараты (дафнеджин, иодатполивинилпироллидон, гризеофульвин, флуцитозин, нитрофунгин).
При острой форме вагинального кандидоза антимикотики назначают по 1 влагалищной свече (таблетке) 1 раз на ночь в течение 6 дней, а при рецидиве хронической инфекции — в той же дозировке в течение 9 дней. Одновременно соблюдается половой покой в течение 2–3 недель, проводится лечение супруга (местно 1% мазь канизона или другое противогрибковое средство).
Эволюция новых антимикотиков идет по пути разработки более коротких курсов лечения. В связи с этим, новая эра в лечении микозов началась с внедрения в клиническую практику одно– или двукратно применяемых пероральных противогрибковых препаратов, активным веществом которых является флуконазол. Один из таких препаратов — Фунголон, который является одним из наиболее эффективных и высокобезопасных противогрибковых препаратов, ввиду его метаболической стабильности, быстрого всасывания за счет хорошей растворимости, минимального влияния на ферментные процессы в печени.
Фунголон относится к классу триазольных соединений, которые угнетают биосинтез стеролов мембраны грибов, нарушают синтез эргостерола, в результате чего ингибируется рост грибов. Установлено, что препарат активен при микозах, вызываемых условно-патогенными (оппортунистическими) грибами, в том числе рода Candida. При этом фунголон избирательно действует на клетку гриба и в отличие от других антимикотических средств не оказывает влияния на метаболизм гормонов, не изменяет концентрацию тестостерона в крови у мужчин и содержание стероидов у женщин, что исключает развитие побочных реакций.
Препарат принимают однократно в дозе 100–150 мг. В случае отсутствия эффекта через 5 дней назначают повторную дозу — 100–150 мг. Особо следует подчеркнуть, что в отличие от других антибикотиков, однократный прием фунголона перорально позволяет достичь терапевтического эффекта в 90–100% случаев.
Санация очагов экстрагенитальной инфекции проводится с учетом чувствительности возбудителей к антибактериальным препаратам.
Планирование и подготовка к беременности возможны только при стойкой и длительной (более 6 месяцев) ремиссии герпес-вирусной инфекции, а также после устранения нарушений в репродуктивной системе с учетом основных факторов прерывания беременности. Важным условием правильной подготовки к беременности является нормализация иммунного и интерферонового статусов пациенток с использованием энзимотерапии. Так как практически любая инфекция сопровождается нарушением процессов энергетики и метаболизма на клеточном, тканевом и органном уровнях человеческого организма, предгравидарная подготовка должна также включать метаболическую терапию. При этом используют комплекс препаратов, стимулирующих биоэнергетические процессы в клетках и тканях — рибофлавин-мононуклеотид, липоевая кислота, пантотенат кальция, токоферола ацетат, рибоксин, оротат калия, пиридоксальфосфат, фитин, троксевазин.
Метаболическую терапию назначают в течение 7 дней с 2–3-недельным перерывом, в виде комплексов. Показана также поливитаминная терапия с комплексом микроэлементов. Проведение ранней диагностики, профилактики и лечения инфекционной патологии репродуктивной системы женщин до наступления беременности, прегравидарная подготовка и планирование беременности позволяют снизить частоту осложнений гестационного периода, тяжесть течения (частоту и длительность рецидивов) инфекционного процесса при беременности, предупредить тяжелые формы неонатальной инфекции, уменьшить перинатальную заболеваемость и смертность.
Блокада репродукции вируса простого герпеса в режиме эпизодической или супрессивной терапии. Применяют ацикловир по 0,2 г 5 раз в сутки в течение 5 дней при легком течении инфекции (обострения 1 раз в 6–8 месяцев) и по 0,2 г 4 раза в сутки в непрерывном режиме в течение 2–2,5 месяцев — при ее частых рецидивах (обострения 1 раз в 30–90 дней).