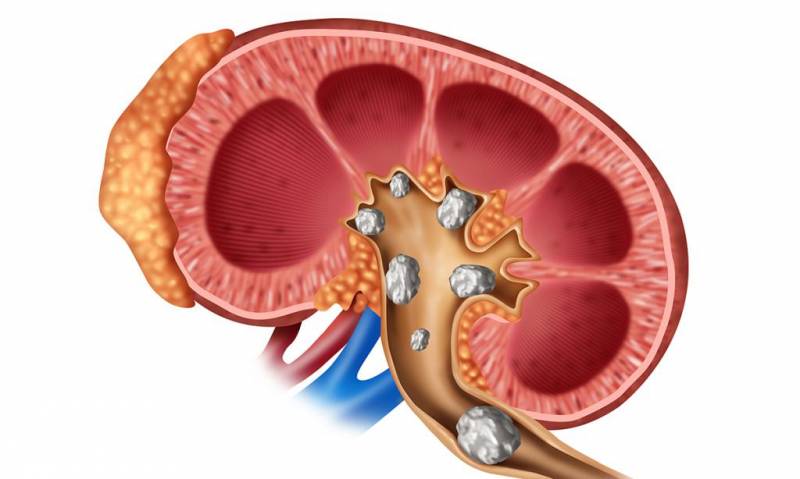
Профилактика и лечение инфекционных осложнений у дренированных пациентов
 | Т.С. Перепанова Д.м.н., профессор, зав. отд. инфекционно-воспалительных заболеваний и клинической фармакологии НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина – филиал «НМИЦ радиологии» Минздрава России (г. Москва) |
Тамара Сергеевна Перепанова, д.м.н., профессор НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина – филиал НМИЦр МЗ РФ в ходе 5й урологической интернет-конференции «Дренирование мочевых путей» дала подробное интервью по теме мероприятия. В беседе с научным редактором UroWeb.ru Викторией Анатольевной Шадеркиной, профессор рассказала об основных принципах профилактики и лечения инфекционно-воспалительных процессов при уходе за дренированными больными и перспективах развития этой области.
Тамара Сергеевна, наличие у пациентов тех или иных дренажей рассматривается как осложняющий фактор заболевания. Есть ли различия в ведении пациентов с нефростомами, дренажами, стентами, уретральными катетерами?
Т.С. Перепанова: Вы затронули самую актуальную тему в урологии, потому что развитие так называемых катетер-ассоциированных инфекций мочевых путей — бич всех без исключения больниц, не только российских. Уретральный катетер, конечно, более опасен, чем нефростома или цистостома. Он является фактором риска номер один не только для развития внутрибольничных инфекций мочевых путей, но и для развития уросепсиса. Порядка 70% септических осложнений связаны с установкой уретральных катетеров, стентов, нефростом и цистостом. Скажем, и врачи, и пациенты порой забывают об установленных стентах, и на этом фоне развивается синдром системной воспалительной реакции. Такое состояние ошибочно диагностируется как атака пиелонефрита, пневмония или что-то еще. На самом же деле стент или уретральный катетер являются тем очагом инфекции, который необходимо удалить до начала антимикробного лечения. Как только очаг инфекции удален, в течение 2–4х дней все нормализуется: и температура, и уровень лейкоцитов, и все прочие признаки системной воспалительной реакции. Это абсолютно типичная ситуация, и к нам регулярно поступают пациенты, которых месяцами лечили антибиотиками на фоне стента, стоявшего в течение нескольких месяцев.
Если мы говорим об уретральных катетерах, нефростомах и цистостомах, то первые из них, подчеркну, наиболее опасны. У мужчин при их использовании могут развиваться эпидидимит, орхит, простатит и так далее. К сожалению, с первых часов установки любого дренажа, особенно уретрального катетера, начинается его контаминация госпитальными штаммами микроорганизмов. Катетер, находящийся в организме пациента более семи дней, на 100% будет инфицирован.
Как вести таких пациентов? Конечно, обязательны асептические условия, стерильные перчатки, использование антисептического геля при установке. Раньше практиковалась ежедневная обработка антисептиками, сегодня уже показано, что это никакого значения не имеет, важны только антисептические гели при установке уретрального катетера. Главное — не промывать катетеры и дренажи. При промывании все биопленки на поверхности катетера, все микроорганизмы «загоняются» внутрь больного. При таком массивном поступлении микроорганизмов выделяются эндотоксины и развивается системная воспалительная реакция. В таком случае также важно понимать, что это не атака пиелонефрита, например, а попадание токсина в кровь, и здесь возможен эндотоксический шок.
Мы общаемся с врачами и пациентами в регионах и, к сожалению, видим, что промывание эпицистостом — распространенная практика.
Т.С. Перепанова: Единственным показанием для промывания является гематурия, тампонада мочевого пузыря, но даже в этом случае рекомендуется сменить цитостомический дренаж на стерильный и промывать уже через него.
Какие возбудители сейчас чаще всего становятся причиной воспалительной реакции?
Показано ли бактериальное исследование больным с уретральным катетером?
Т.С. Перепанова: Как рутина не рекомендуется. Если мы говорим о больных перед операциями — конечно, нужно удалить имеющийся катетер и поставить стерильный, если без него невозможно обойтись, или же поменять цистостомический дренаж, и только после этого взять посев мочи. Мы должны знать состав флоры, если возникнут какие-то осложнения после операции. Но рутинно это не требуется, потому что, по большому счету, не требуется никакого лечения: формируются биопленки, и сегодня не существует даже фиксированных периодов замены катетеров или дренажей.
В каких случаях показано назначение антибактериальных препаратов пациентам с дренажами?
Т.С. Перепанова: Если наблюдается лихорадка на фоне присутствия катетера или стента, если развился синдром системной воспалительной реакции, который может очень быстро перейти в острый пиелонефрит, сепсис и септический шок. Опять же, прежде чем начинать антибактериальную терапию, нужно убрать источник инфекции — катетер, при необходимости заменив его на стерильный. Стенты в большинстве случаев просто убирают безо всякой замены. Уже после этого начинается антибиотикотерапия. У пациентов с эпицистостомой — то же самое. Еще раз скажу, что промывать их нельзя.
Второе показание — у больных перед эндоскопическими вмешательствами, где предполагается инцизия слизистых. Опять повторю – после удаления инфицированного катетера или замены его на стерильный.
А показана ли антибактериальная терапия пациентам с нефростомами, или там все зависит от конкретной ситуации?
Т.С. Перепанова: Да, зависит, конечно, от клинической ситуации. Если, опять же, началась системная воспалительная реакция, поднялась температура, — меняем дренаж на стерильный и после этого начинаем антимикробное лечение в соответствии с посевом. Рутинно, для профилактики оно не назначается. Это, во-первых, бесполезно, во-вторых, вредно. Мы только селекционируем резистентные штаммы таким образом. Длительные антибактериальные курсы, особенно на фоне стентов, абсолютно не нужны.
Сегодня остается актуальной проблема биопленок. Появились ли какие-то препараты, которые воздействуют на них?
Т.С. Перепанова: Знание о биопленках мы получили относительно недавно, вместе с появлением электронных микроскопов. В мире, конечно, очень активно работают с биопленками, и мы тоже стараемся на них влиять. К сожалению, сама структура биопленок, в которую входят масса микроорганизмов и матрикс, препятствует этому. В биопленку могут проникать фторхинолоны и макролиды, но матрикс «выкидывает» антибиотики методом эффлюкса. Потом, все разрабатываемые антибиотики, рассчитанные на живые размножающиеся микроорганизмы, не действуют на микроорганизмы, находящиеся внутри биопленки, где они меняют свою форму, у них ослаблен метаболизм, поэтому на них существующие антибиотики и не влияют. Разрабатываются новые препараты неантимикробного действия, они проникают, например, в протеины. Мы, в свою очередь, начали работу с бактериофагами. Это российское достояние, Советский Союз и Россия были первыми на этом поле, и мы единственная страна, где налажен промышленный выпуск бактериофагов.
Недавно мы провели исследование: перед перкутанной нефролитотрипсией обрабатывали катетеры в течение получаса бактериофагом. Перед этим провели предварительную работу с Институтом микробиологии имени Н.Ф. Гамалеи, чтобы точно установить нужный отрезок времени. Было установлено, что бактериофаги действуют на раннюю сформировавшуюся биопленку — всего 6–8 часов. После 8–12 часов развивается зрелая биопленка, на которую не действуют уже и фаги. Интересно, что на катетерах, извлеченных через сутки, в 3х из 30-ти случаев в самой биопленке был обнаружен живой бактериофаг. Значит, он туда проник, и это уже обнадеживает. Мы пытаемся сейчас разработать, к примеру, гелевые формы бактериофагов, чтобы они лучше удерживалась на катетерах, но тут тоже не так все просто.
Какой механизм действия фагов?
Т.С. Перепанова: Бактериофаг запускает свою ДНК в бактерию. Дальше из составляющих бактерии — из митохондрий, из ядра — он начинает формировать свои вирионы, то есть развивается вирусная инфекция среди бактерий. Из содержимого клетки начинают формироваться «детеныши» фагов. В итоге клетка лизируется, из нее выходят новые вирионы и заражают соседние клетки. По большому счету, сам фаг внедряется и погибает, но из его ДНК развивается дальнейший процесс уничтожения бактерий.
Выглядит перспективно. Наверное, несправедливо, что в течение 10–20 лет фаги были забыты?
Т.С. Перепанова: Их открыли в 1918 году и в 30-е годы после всех экспериментальных исследований начали активно пробовать на людях. Но потом в 1938 году открыли пенициллин. Естественно, эффект был мощным. Думали, что им можно вылечить все, но, конечно, резистентность стала развиваться сразу же. Сегодня проблема антибиотикорезистентности в числе первых в мире. Даже новые дорогие антибиотики не успевают за ней. Поэтому фаги сейчас снова рассматриваются как перспективный метод.
Скажите, пожалуйста, Тамара Сергеевна, есть ли какие-то общие принципы ведения пациентов с урологическими дренажами?
Т.С. Перепанова: Главное — стараться дренажи/катетеры/стенты вообще не ставить, а при необходимости — как можно меньше держать. Понятно, что абсолютно обойтись без катетеров и дренажей в урологии мы не можем, но в части инфекционных осложнений у больных с нарушениями мочеиспускания более безопасна интермиттирующая катетеризация. У мужчин также возможно применение уропрезервативов. Затем, сама установка должна производиться в стерильных условиях и со стерильными перчатками. Общие принципы: не промывать, использовать антисептические гели только при установке, убирать при первой возможности, не кормить пациента антибиотиками и уросептиками без показаний.
В последнее время контроль над применением антибиотиков усилился, многие аптеки их уже не продают без рецепта. Что еще можно сделать в этом направлении?
Т.С. Перепанова: Хорошо, что Вы ведете свои интервью и программы на подобные темы. Мы тоже организовали школу по рациональной фармакотерапии в урологии. Уже было показано, что образовательные программы, особенно в том, что касается катетер-ассоциированных инфекций, имеют огромное значение. Уровень распространенности инфекций снижается на 70% после проведения образовательных программ среди медицинских работников, а также пациентов. Люди узнают о том, что не нужно промывать дренажи, о том, что их нужно убирать и менять на стерильные прежде, чем назначить антибиотик, и так далее.
Конечно, образовательный процесс должен быть беспрерывным. Постоянно появляются новые данные клинических исследований, нужно следить за ними.
Т.С. Перепанова: Совершенно верно. Сейчас мы обновляем федеральные клинические рекомендации 2019 года. Сделаем, наверное, отдельную вкладку по уходу за катетерами. Врачи не всегда могут уделить время чтению научных журналов, а так они увидят то, что нужно.
В целом какие перспективы Вы видите в ведении пациентов с дренажами?
Т.С. Перепанова: К сожалению, никакое покрытие, даже антимикробное, не дает страховки от инфекции. Катетеры с импрегнированным серебром чуть лучше себя показывают на сроках до семи дней, но после семи дней все едино, повышается риск развития инфекции. Со стороны катетеров нет защиты. Это не слизистая мочевых путей, в которой есть цитокины, антимикробные пептиды и так далее. У катетера нет иммунитета слизистых оболочек, поэтому начинается строительство биопленок. К тому же, большинство микроорганизмов вырабатывают уреазу — фермент, который разлагает мочевину мочи на аммиак и СО2. При этом рН меняется в щелочную сторону и начинают оседать кристаллы. Эти кристаллы выпадают на любое покрытие, и уже на них микробы начинают строить биопленку.
По большому счету и наши, и международные усилия сейчас привели к тому, что хотя бы после ТУР, после перкутанных вмешательств катетер на первые сутки удаляется. Это уже огромный прогресс, потому что раньше их держали до выписки.
Последний момент — мочеприемники. Катетер, собирательные трубки и мочеприемник — это единая система, которую нельзя нигде разъединять, особенно во время дежурства, грязными руками. Открывается только клапан мешка, чтобы слить мочу. Любое разъединение может привести к передаче инфекции. Если оно необходимо, нужно все делать в стерильных перчатках и потом мыть руки, прежде чем перейти к следующему больному, иначе переносятся госпитальные штаммы микроорганизмов. Самое главное — санитария и гигиена.
Спасибо за интервью!
Материал подготовила В.А. Шадеркина
научный редактор UroWeb.ru
Полную видеоверсию мероприятия можно посмотреть на Uro.TV
Статья опубликована в журнале «Дайджест урологии» №4-2019
Уход за нефростомой
Уход за нефростомой
Нефростома – специальная медицинская трубка, устанавливаемая пациентам после оперативного вмешательства на почках либо мочеточнике. Она вводится в просвет лоханки почки и выполняет функцию прямого отвода мочи из организма. Трубка позволяет выводить биологическую жидкость в обход естественного пути ее прохождения, когда мочевыводящая система еще не готова к нагрузкам.
Показания к установке мочевыводящей трубки
Устанавливают нефростому в почку при операции или путем прокола тканей во время пункции лоханки. Процедуру могут проводить только высококвалифицированные врачи. Самостоятельное введение трубки или с участием младшего медицинского персонала невозможно, так как процесс довольно сложен, а неправильные действия могут оказать вред больному.
Показанием к установке нефростомы в почку могут служить патологии:
Нефростомия может проводиться в диагностических целях для забора на анализ биоматериала из почечной лоханки, при гнойных воспалительных процессах.
На сколько ставится нефростома?
Мочевыводящая трубка устанавливается надолго. Нефростома при операции по удалению камней вводится на полгода. Больному на протяжении всего периода необходимо внимательно следить за трубкой и выполнять все рекомендации врача по уходу за ней. Особенно тяжело становится пожилым людям, которые обессилели во время операции и не в состоянии самостоятельно выполнять предписания.
Катетер при недостаточности мочеточника и частичной закупорке его проходов устанавливается всего на месяц, а иногда и меньше. Зачастую врачи в этом случае стараются всячески избежать ввода трубки в лоханку, подбирая менее радикальные способы лечения, чтобы не обременять пациентов.
Как правильно ухаживать за катетером?
Независимо от периода, на который устанавливается нефростома, уход за ней должен всегда быть качественным и регулярным. От правильности выполняемых действий зависит, насколько легким будет лечение и послеоперационная реабилитация.
Наши пансионаты:
Все процедуры по уходу за пациентом с нефростомой должны выполняться специалистом, чтобы избежать развития осложнений. В противном случае выздоровление может затянуться надолго или, что еще хуже, привести к летальному исходу.
Вероятные осложнения
Осложнения могут возникнуть как во время самого введения трубки, так и непосредственно в реабилитационный период. В первом случае врач может повредить почечную артерию в момент прокалывания мягких тканей и введения катетера. Неосторожность медиков чревата масштабным кровоизлиянием в брюшную полость с последующим образованием ретроперитонеальной гематомы. Она впоследствии способна поразиться инфекцией, что приведет к необходимости проведения операции.
Если врач проигнорирует гематоз и установит катетер, кровь может проникнуть в лоханку и будет выводиться через трубку. Это чревато неправильной диагностикой и назначением терапевтического курса.
Также возможен послеоперационный инфекционный процесс, который поражает почку, под названием пиелонефрит. Заболевание протекает агрессивно, невосприимчиво к стандартным антибиотикам. Препараты для лечения пиелонефрита стоят дорого, поэтому развитие болезни лучше не допускать.
Чтобы избежать осложнений и ускорить выздоровление, нужно обеспечить правильный послеоперационный уход за установленной мочевыводящей трубкой. Пенсионеры требуют большего внимания, так как нуждаются в дополнительной посторонней помощи с выполнением элементарных действий. Существуют специальные пансионаты для пожилых людей, где специалисты ухаживают за больными, всячески поддерживают их психологический и эмоциональный комфорт.
Специализированные центры престарелых имеют в распоряжении необходимое оборудование, а сотрудники обладают всеми навыками, для оказания грамотной помощи тяжелобольным людям. Госпитализация в пансионат облегчит жизнь не только пациенту, но и его родственникам, которые смогут снять со своих плеч груз забот о состояние близкого человека.
Гнойные воспаления почек: почему возникают и как лечить
Гной в почках — опасное явление, имеющее инфекционную природу. При несвоевременном обращении к урологу такие воспалительные процессы как пионефроз, паранефрит, карбункул, абсцесс приводят к сепсису и летальному исходу.
Причины возникновения гнойного воспаления в почке
Нагноение — следствие некоторых заболеваний почек и органов мочевыделительной системы (пиелонефрит и др.). Одной из причин возникновения воспалительных процессов является инфицирование почек болезнетворными организмами.
После поражения микробами на поверхности органа появляется инфильтрат, наполненный гноем. Если вовремя от него не избавиться, гнойный мешок может вызвать отмирание тканей почки. При его разрыве жидкость изливается в брюшную полость. Последствия в этом случае непредсказуемы.
Другой причиной гнойного воспаления почек может стать механическое повреждение органа (например, ножевые ранения, неверное введение катетера в мочевой пузырь и т.д.). Возникновение инфильтрата может вызвать и нестерильность во время проведения хирургических вмешательств.
Симптоматика
Гнойные заболевания почек могут иметь характерные проявления или проходить практически бессимптомно. Из-за того, что в некоторых случаях воспалительный процесс протекает в скрытой форме, постановка правильного диагноза затрудняется.
Чаще всего симптоматика довольно бурная:
Лабораторные исследования позволяют выявить высокий уровень лейкоцитов в крови, что указывает на воспалительный процесс в организме.
Особенно опасен гной в почках для беременных. Из-за гормональной перестройки организма и увеличения нагрузки на органы здоровье женщины в этот период становится очень уязвимым. На фоне воспалительного процесса у будущей мамы может развиться гестоз и анемия. Гнойная почка может стать причиной прерывания беременности, гипоксии и внутриутробного инфицирования плода, возникновения пороков развития плода, смерти матери и ребенка.
К группе риска относят также больных диабетом. Это заболевание является причиной глубоких нарушений гомеостаза. Из-за этого пациенты, страдающие сахарным диабетом, сталкиваются с гноем в почках в 4 раза чаще, чем люди с неосложненным анамнезом. Более того, после удаления инфильтрата у больных могут развиваться тяжелые осложнения (уросепсис, почечная недостаточность и др.), вызывающие летальный исход.
Методы лечения гноя в почке
Самолечение воспалительных процессов недопустимо. При появлении тревожных симптомов необходимо немедленно обратиться к врачу. Лечение заболевания производится строго в условиях стационара.
Консервативная терапия гнойной почки считается малоэффективной. Прогноз для пациентов условно неблагоприятный, так как длительное лечение воспалительного процесса может привести к серьезным осложнениям (поражению второй почки, уросепсису, прорыву гноя и т.д.). По этой причине наиболее эффективным методом признано хирургическое вмешательство. Гнойный очаг удаляется с последующим дренажом брюшной полости. В тех случаях, когда некротическое поражение слишком велико, врач может принять решение удалить больную почку.
После проведения операции пациентам показана интенсивная антибактериальная терапия, способствующая выведению токсинов из организма.
Если вы почувствовали недомогание, не стоит откладывать поход к врачу, так как малейшее промедление может стоить вам жизни. Врачи клиники урологии имени Р. М. Фронштейна Первого Московского Государственного Медицинского Университета имени И.М. Сеченова (Государственный центр урологии) окажут вам квалифицированную помощь и помогут сохранить здоровье.
НЕФРОСТОМА
Нефростома – это дренажный катетер у которого один конец фиксируется в почечной лоханке, а противоположный конец выводится наружу со стороны поясницы и соединяется с мочеприемником. Отток мочи происходит в мешок для сбора мочи.
Нефростому устанавливает уролог в ходе хирургической операции, которая проводится с помощью УЗИ или рентген-аппаратов для исключения риска повреждений почечной артерии или лоханки. Такая операция называется нефростомия.
Нефростомия может выступать как в роли временного решения проблем с выделением, так и паллиативной, т.е. постоянной постоперационной помощи, поддерживающей функционирование организма.
(использовано видео по материалам Мед2Мед.ру)
Мешок для нефростомы выбирают исходя из того, в каком состоянии находится пациент и какой образ жизни он намерен вести. Лежачим пациентам рекомендуют прикроватные изделия, а тем, кто может передвигаться – ножные, которые крепятся к бедру или голени.
Объем мочеприемника тоже зависит от положения: лежачим пациентам лучше ориентироваться на 1,5-2 литра, тем, кто передвигается в переделах квартиры или палаты – до 1,5 литров, а людям, которые продолжают вести активную жизнь – до 800 мл.
В любом случае его следует регулярно опорожнять – лучше всего, когда мешок наполняется на две трети. Если он будет слишком наполнен, то есть риск заброса мочи по трубке обратно в лоханку почки.
Самое частое осложнение, с которым сталкиваются пациенты после нефростомии – инфекции и воспаления из-за недостаточного ухода. В нашей клинике этим занимается медицинской персонал, но дома уход за нефростомой становится задачей пациента или его близких
Это следует делать регулярно, тщательно и правильным образом.
Уход за нефростомой: алгоритм действий:
• В положении стоя и при ходьбе мешок для сбора должен располагаться ниже области почек. Для этого мешок для сбора мочи можно закрепить липкой лентой на бедре или поместить его в специальную сумку.
• В положении лежа мешок для сбора мочи должен быть расположен ниже уровня положения тела. Для этого мешок для сбора мочи следует поместить сбоку от кровати. Располагать мешок для сбора мочи на полу нельзя.
• Контролируйте фиксацию нефростомы и следите за состоянием кожи вокруг нефростомы, а также за появлением выделений вокруг нефростомы.
• Вы можете принимать душ, но место вхождения трубки должно оставаться сухим. Повязку можно защитить полиэтиленовым покрытием (пакетом), таким образом ваша повязка будет полностью закрыта.
• Применяйте мешок для сбора мочи, который можно опустошать через пробку, расположенную в нижней части мешка. Опустошайте мешок для сбора каждые 4–5 часов, или по мере его заполнения.
• Меняйте мешок для сбора через 1–2 недели по мере необходимости. При повреждении мешка или в случае засора мешок следует менять чаще.
• Пейте не меньше 1,5–2 литров жидкости в день. Употребление большего количества жидкости способствует улучшению проходимости мочевых путей и нефростомы и препятствует появлению осадка и развитию воспаления.