Полный текст
Аннотация
Ключевые слова
Об авторах
Евгений Павлович Студенцов
Email: dens36@mail.ru
к. х. н., доцент, ведущий научный сотрудник кафедры химии и технологии синтетических биологически активных веществ
Станислав Михайлович Рамш
Email: sramsh@technolog.edu.ru
д. х. н., профессор, заведующий кафедрой химической технологии органических красителей и фототропных соединений
Наталия Григорьевна Казурова
Email: dens36@mail.ru
инженер кафедры химии и технологии синтетических биологически активных веществ
Ольга Владимировна Непорожнева
Email: dens36@mail.ru
младший научный сотрудник кафедры химии и технологии синтетических биологически активных веществ
Александр Васильевич Гарабаджиу
Email: gar-54@mail.ru
д. х. н., профессор, проректор по научной работе
Татьяна Александровна Кочина
Email: kochina@mail.ru
д. х. н., заведующая лабораторией кремнийорганических соединений и материалов
Михаил Григорьевич Воронков
Email: voronkov@isc.nw.ru
д. х. н., академик РАН, профессор, советник РАН, руководитель группы элементоорганических соединений при советнике РАН
Виктор Анатольевич Кузнецов
Email: Kuznetsov_VA@front.ru
к. х. н., заведующий лабораторией химического моделирования
Денис Викторович Криворотов
Email: Kuznetsov_VA@front.ru
к. х. н., старший научный сотрудник лаборатории химического моделирования
Список литературы
© Студенцов Е.П., Рамш С.М., Казурова Н.Г., Непорожнева О.В., Гарабаджиу А.В., Кочина Т.А., Воронков М.Г., Кузнецов В.А., Криворотов Д.В., 2013
Эта статья доступна по лицензии Creative Commons Attribution 4.0 International License.
Клиническая фармакология метапрота, нового противоастенического препарата с психоактивирующими свойствами
© П. Д. Шабанов
Военно-медицинская академия им. С. М. Кирова МО РФ, Санкт-Петербург Ключевые слова:
метапрот; гепатит А; хронические заболевания легких; ишемическая болезнь сердца; инсульт; гипоксия; энцефалопатия
В настоящее исследование включены клинические данные по влиянию метапрота, нового оригинального отечественного препарата, на течение вирусного гепатита А, хронических неспецифических заболеваний органов дыхания, по применению метапрота в комплексном лечении лучевой болезни, для лечения больных с нервно-мышечными заболеваниями, ишемической болезнью сердца, для профилактики ишемических и реперфузионных повреждений при аортокоронарном шунтировании, профилактики тугоухости, в качестве средства метаболической защиты головного мозга при острых нарушениях мозгового кровообращения, для коррекции послеоперационной диффузной гипоксически-ишемической энцефалопатии и гипоксии плода у рожениц. Приведены данные по фармакокинетике метапрота. Сделан вывод о высокой эффективности метапрота при рассматриваемых видах патологии. Библ. 65 назв.
Введение
Итак, метапрот относится к группе антиастенических средств с выраженными психоактивирующими свойствами. Он обладает ноотропной, антигипоксической, антиоксидантной, иммуномодулирующей активностью, способностью усиливать регенерацию и репарацию (Смирнов А. В., Криворучко Б. И., 1997; Зарубина И. В., Миронова О. П., 2002; Шабанов П. Д., 2002; Лукк М. В. и др., 2008; Евсеева М. А. и др., 2008; Новиков В. Е. и др., 2008; Зарубина И. В. и др., 2009; Шабанов П. Д. и др., 2009).
Механизм действия метапрота
Механизм действия препарата заключается в активации синтеза РНК, а затем белков, в том числе ферментных и имеющих отношение к иммунной системе. Происходит активация синтеза ферментов глюконеогенеза, которые обеспечивают утилизацию лактата (фактора, ограничивающего работоспособность) и ресинтез углеводов — источника энергии при интенсивных нагрузках, что ведет к повышению физической работоспособности. Усиление синтеза митохондриальных ферментов и структурных белков митохондрий обеспечивает увеличение энергопродукции и поддержание высокой степени сопряженности окисления с фосфорилированием. Сохранение высокого уровня синтеза АТФ при дефиците кислорода способствует выраженной антигипоксической и противоишемической активности. Метапрот усиливает синтез антиоксидантных ферментов и обладает выраженной антиоксидантной активностью. Повышает устойчивость организма к воздействию экстремальных факторов — физической нагрузке, стрессу, гипоксии, гипертермии. Особенностью препарата является то, что он повышает работоспособность при физической нагрузке и обладает выраженным антиастеническим действием, ускоряя процессы восстановления после экстремальных воздействий (Зарубина И. В., Миронова О. П., 2002; Зарубина И. В., Шабанов П. Д., 2003; Миронова О. П. и др., 2003; Зарубина И. В. и др., 2006; Шабанов П. Д. и др., 2005, 2006, 2009).
После приема внутрь метапрот хорошо всасывается из желудочно-кишечного тракта, активно метаболизируется в печени. После однократного приема обнаруживается в крови через 30 мин, максимальный эффект достигается через 1-2 ч, продолжительность действия 4-6 ч. Фармакокинетика метапрота (капсула 250 мг), исследованная на добровольцах методом высокоэффективной жидкостной хроматографии с УФ-детекцией, представлена на рисунках 1 и 2. Препарат детектировался в плазме крови здоровых добровольцев в концентрациях выше 4 нг/мл не дольше 10 ч. Как следует из литературных данных (Зарубина И. В., Шабанов П. Д., 2004), у части добровольцев наблюдался второй, менее выраженный, пик концентраций.
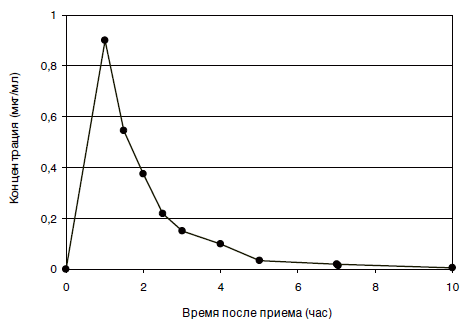 Рисунок 1. Средние фармакокинетические профили 2-этилтиобензимидазола гидробромида у здоровых добровольцев после однократного приема внутрь метапрота (250 мг) | 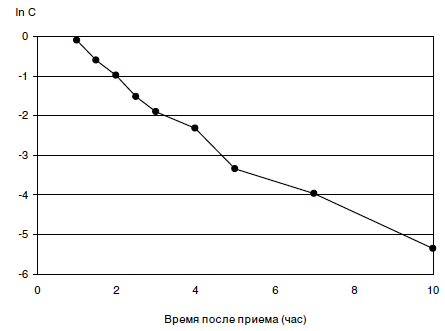 Рисунок 2. Ln-преобразованные средние фармакокинетические профили 2-этилтиобензимидазола гидробромида у здоровых добровольцев после однократного приема внутрь препарата метапрот (250 мг) |
На фоне курсового приема эффект обычно нарастает в первые 3-5 дней, затем устойчиво поддерживается на достигнутом уровне. При длительном курсовом непрерывном приеме, особенно в больших дозах, может отмечаться тенденция к кумуляции препарата с повышением его концентрации в крови к 10-12 дню применения.
Показаниями к применению метапрота являются повышение и восстановление работоспособности, в том числе в экстремальных условиях (тяжелые физические нагрузки, гипоксия, перегревание) (Зарубина И. В., 2002; Зарубина И. В., Миронова О. П., 2002; Зарубина И. В., Шабанов П. Д., 2002). Метапрот применяется в качестве средства повышения адаптации к воздействию различных экстремальных факторов (Гречко А. Т., 1994; Шабанов П. Д., 2002; Ганапольский В. П. и др., 2007). Незаменим для коррекции астенических расстройств различной природы (при неврастении, соматических заболеваниях, после перенесенных тяжелых инфекций и интоксикаций, пред- и послеоперационном периоде при хирургических вмешательствах) (Востриков В. В. и др., 2006; Шабанов П. Д. и др., 2006; Болехан А. В. и др., 2007).
Востребован в составе комплексной терапии, в частности, при перенесенной черепно-мозговой травме, менингите, энцефалите, нарушениях мозгового кровообращения, когнитивных расстройствах (Зарубина И. В. и др., 2005, 2006; Зарубина И. В., Шабанов П. Д., 2006; Шабанов П. Д. и др., 2005, 2007; Хабаров И. Ю. и др., 2007).
Безусловно, каждый препарат имеет свои недостатки. К противопоказаниям относятся возможная гиперчувствительность к приему препарата, гипогликемия (снижение уровня сахара в крови), период лактации (вскармливания), артериальная гипертензия, глаукома (повышение глазного давления).
Препарат назначают внутрь, после еды, по 0,25 г 2 раза в день. При необходимости суточную дозу повышают до 0,75 г (0,5 г утром и 0,25 г — после обеда), а лицам с массой тела свыше 80 кг — до 1 г (по 0,5 г 2 раза в день). Курс лечения — 5-6 дней, затем 2-дневный перерыв во избежание кумуляции препарата, и курс повторяют. Количество курсов зависит от эффекта и в среднем составляет 2-3 (реже 4-6) курсов (Шабанов П. Д. и др., 2009).
Для повышения работоспособности в экстремальных условиях препарат принимают за 40-60 мин до предстоящей деятельности в дозе 0,5-0,75 г При продолжении работы повторный прием производят через 6-8 ч в дозе 0,25 г. Максимальная суточная доза — 1,5 г, а в последующие сутки 1 г.
Для поддержания высокого уровня работоспособности в течение длительного времени (несколько недель) и для активации адаптационных процессов препарат назначают по схеме: 5-дневные курсы приема с 2-дневными перерывами в дозе 0,25 г 2 раза в сутки.
Учитывая, что инструктивные показания к применению метапрота ограничены, мы сочли необходимым привести более расширенные данные по клиническому использованию метапрота в разных областях медицины. Данные исследования были выполнены в разное время в основном в клиниках Военно-медицинской академии им. С. М. Кирова, Санкт-Петербург. Они, несомненно, имеют важное значение при назначении препарата по иным, не предусмотренным инструкцией, показаниям.
Клиническое исследование метапрота у разных категорий больных
В настоящее исследование включены оригинальные данные по влиянию метапрота на течение вирусного гепатита А, хронических неспецифических заболеваний органов дыхания, по применению метапрота в комплексном лечении лучевой болезни, для лечения больных с нервно-мышечными заболеваниями, ишемической болезнью сердца, для профилактики ишемических и реперфузионных повреждений при аортокоронарном шунтировании, профилактики тугоухости, в качестве средства метаболической защиты головного мозга при острых нарушениях мозгового кровообращения, для коррекции послеоперационной диффузной гипоксически-ишемической энцефалопатии. Применение метапрота в комплексной терапии и реабилитации больных вирусным гепатитом А
Заключение
В приведенном исследовании представлены данные о разнообразных эффектах метапрота, зарегистрированных при изучении его клинических эффектов. В целом, метапрот оказывает положительное действие в отношении многих патологических состояний, где патогенетическими компонентами выступают гипоксия, ишемия, снижение биосинтеза белка, дегенерация тканей. В основе клинических эффектов метапрота лежит его способность активировать синтезы РНК и белков в нервной и мышечной ткани, повышать микроциркуляцию важнейших органов (миокард, мозг, печень), оптимизировать энергопродукцию и энерготраты в основном за счет более экономного расходования энергии АТФ и стимуляции глюконеогенеза, усиливать репаративные процессы в тканях (Зарубина И. В. и др., 2001; Зарубина И. В., Шабанов П. Д., 2002; Шабанов П. Д. и др., 2009). Все это и определяет показания к применению метапрота, ориентированные на преодоление последствий ишемии и гипоксии, восстановление энергетики и стимуляцию репарации в различных тканях и органах.
Литература
Clinical pharmacology of metaprot, a new antiasthenic drug with psychoactivating properties
P. D. Shabanov Summary. The clinical data concerning the effects of metaprot, a new original Russian drug, on virus hepatitis A, chronic nonspecific diseases of the pulmonary system, in complex therapy of radial disease, neuromuscular diseases, ischemic heart disease, for prevention of ischemic and reperfusion disorders after aortocoronar schunting, hard hearing, as a metabolic defender of the brain in acute disorders of the brain blood flow, for the correction postoperational diffuse hypoxic and ischemic encephalopathy and fetus hypoxia in pregnant women are reviewed. The pharmacokinetics of metaprot is represented too. It is concluded that metaprot is an effective drug in pathology to be considered.
Key words: metaprot; hepatitis A; chronic diseases of the lung; ischemic heart disease; insult; hypoxia: encephalopathy.
Изыскание соединений с актопротекторной активностью среди производных аминоэтанола с кислотами цикла Кребса
Полный текст
Аннотация
Данное исследование проведено с учетом того, что продолжают оставаться актуальными поиск и внедрение в медицинскую практику препаратов для фармакологической коррекции утомления и восстановления физической работоспособности при астенических явлениях после перенесенных заболеваний, физических нагрузок у военнослужащих, спортсменов и лиц пожилого возраста.
В ходе исследования мы преследовали цель изучить влияние производных диметиламино- и диэтиламиноэтанола с интермедиатами цикла трикарбоновых кислот (производных аминоэтанола с кислотами цикла Кребса) на физическую работоспособность белых беспородных самцов мыши.
Исследование проводились на 490 беспородных мышах самцах массой 22–24 грамм. В качестве скрининговой модели для изучения влияния новых соединений на физическую работоспособность выбран тест предельного плавания с грузом.
Для выбора наиболее эффективного из синтезированных соединений был выполнен скрининг фармакологической активности влияния новых соединений, фумарового эфира диэтиламино- и диметиламиноэтанола с интермедиатами цикла Кребса, на физическую работоспособность самцов мыши.
Статистическую обработку полученных данных для установления различий между группами проводили, используя F-критерий дисперсионного анализа.
Как показали исследования, по своему влиянию на физическую работоспособность данные соединения превосходили препарат сравнения – деанола ацеглумат в оптимальной дозе 50 мг/кг.
В процессе разработки новых актопротекторных средств мы считаем целесообразным использовать способность кислот цикла Кребса усиливать антигипоксическую, актопротекторную и ноотропную активность базовых катионных групп в солях.
Ключевые слова
Полный текст
СОКРАЩЕНИЯ:
ГАМК – гамма аминомасляная кислота;
КА – коэффициент активности;
Ксэ – коэффициент сравнительной эффективности;
ЦНС – центральная нервная система;
ANOVA – метод дисперсионного анализа;
ФДЭС – соединение «Фумарат – ДЭАЭ – Сукцинат».
ВВЕДЕНИЕ
Физическая работоспособность является одним из наиболее информативных показателей состояния организма. Патологии и нарушения в работе печени [1], сердечно-сосудистой и дыхательной систем будут приводить к ее снижению. Еще одним фактором, влияющим на работоспособность, является состояние центральной нервной системы. Так, при различных травмах центральной нервной системы зачастую происходит не только снижение физической работоспособности, но и нарушение двигательной активности в целом [2].
Таким образом, физическая работоспособность является интегративным показателем здоровья организма в целом. Это делает тесты по оценке физической работоспособности важными в мониторинге наиболее значимых и распространенных заболеваний, являющихся наиболее частой причиной смерти и инвалидизации в развитых странах.
Актуальным является поиск и внедрение в медицинскую практику препаратов для фармакологической коррекции утомления и восстановления физической работоспособности при астенических явлениях после перенесенных заболеваний, физических нагрузок у военнослужащих, спортсменов и лиц пожилого возраста.
На сегодняшний день среди препаратов с актопротекторным действием одну из самых изученных групп составляют синтетические средства различных химических классов. Наиболее изучены производные имидазола: 2-этилтиобензимидазол («эталонный» актопротектор) и производные аминоадамантана – адамонтилбромфениламин [3]. Тем не менее, номенклатура современных актопротекторных средств крайне ограниченна, несмотря на высокую потребность в них личного состава военных формирований, сотрудников спасательных служб, спортсменов, пациентов при различных астенических состояниях.
Представляет интерес поиск новых актопротекторов среди средств неистощающего характера, которые по химической структуре близки к естественным метаболитам организма и способны повышать устойчивость организма к физическим нагрузкам без увеличения потребления кислорода и теплопродукции, повышая коэффициент полезного действия [3].
В качестве потенциальных средств с актопротекторной активностью большой интерес представляют производные аминоэтанола (этаноламина), обладающие широким спектром фармакологической активности, в том числе в отношении умственной и физической работоспособности [4, 5].
Поскольку фармакологическая коррекция процессов умственного и физического утомления имеет ряд общих принципов, то соединения, обладающие ноотропным и антиоксидантным действием, перспективны для изучения в качестве актопротекторов [6].
Заметной актопротекторной активностью обладают также активаторы главного энергетического механизма клеток – цикла Кребса, к которым, в частности, относятся янтарная, яблочная, фумаровая, альфа-кетоглутаровая кислоты и препараты их солей [6–8].
В исследованиях Г.А. Фрелих и Е.И. Маевского было показано, что интермедиаты цикла трикарбоновых кислот способствуют сохранению дыхания митохондрий и поддержанию трансмембранного потенциала ионов водорода [9, 10].
Важно, что на мировом фармацевтическом рынке отсутствуют препараты с актопротекторной активностью, разработанные на основе фумаровой кислоты. В связи с этим поиск таких новых препаратов с актопротекторной активностью среди соединений, состоящих из фумарового эфира диэтиламиноэтанола с интермедиатами цикла трикарбоновых кислот, является актуальным.
ЦЕЛЬ ИССЛЕДОВАНИЯ
Изучение влияния производных диметиламино- и диэтиламиноэтанола с интермедиатами цикла трикарбоновых кислот на физическую работоспособность белых беспородных самцов мыши.
МАТЕРИАЛЫ И МЕТОДЫ
Исследования проводились на 490 беспородных мышах-самцах массой 22–24 г и выполнялось в соответствии с приказом Минздрава России от 01.04.2016 г. №199н «Об утверждении правил надлежащей лабораторной практики», согласно утвержденному письменному протоколу. Животные были получены из питомника лабораторных животных «Рапполово», прошли необходимый карантин и содержались в стандартных условиях сертифицированного вивария на обычном пищевом рационе со свободным доступом к воде.
Объектами исследования были выбраны соединения – продукты взаимодействия диметиламино- и диэти- ламиноэтанола с некоторыми интермедиатами цикла трикарбоновых кислот (фумаровый эфир ДЭАЭ и ДМАЭ в виде солей: с фумаровой и янтарной кислотами, L-малатом, альфа-кетоглутаратам), которые синтезированы на кафедре органической химии Санкт-Петербургского государственного химико-фармацевтического университета Минздрава России.
В качестве препаратов сравнения использовали:
– производное аминоэтанола, 2-(диметиламино)этанол N-ацетил-L-глутаминовой кислоты (деанола ацеглумат, ООО «Экохим-инновации», Россия);
– этилтиобензимидазол (ЗАО «Фармпроект», Россия).
Выбор этилтиобензимидазола происходил на основании следующих критериев:
– наличие данных о применении вещества для фармакологической коррекции физической работоспособности;
– доступность на российском фармацевтическом рынке;
– возможность энтерального введения экспериментальным животным.
Деанол ацеглумат является ноотропным препаратом, по химической структуре близким к естественным метаболитам головного мозга (таким как гамма аминомасляная и глутаминовая кислота). Оказывает нейропротекторное действие, способствует улучшению памяти и процесса обучения, оказывает положительное влияние при астенических и адинамических расстройствах (повышая двигательную и психическую активность пациентов).
Выбор его для сравнения происходил на основании следующих критериев:
– сходство структуры с изучаемым веществом;
– наличие данных о применении вещества для фармакологической коррекции физической работоспособности;
– доступность на российском фармацевтическом рынке;
– возможность энтерального введения экспериментальным животным.
Оценка работоспособности лабораторных животных в данной работе осуществлялась с помощью теста «Вынужденное плавание» с грузом. Классическая методика теста «отчаяния» Порсолта («Вынужденного плавания») используется для испытания антидепрессивного действия веществ [11]. Однако она, в силу своей простоты, широко применяется для оценки эффектов стимуляторов работоспособности в условиях стресса. Тест принудительного плавания представляет собой комбинированный жесткий вид стресса, сочетающий физический и эмоциональный компоненты [12, 13, 14].
Модификация данной методики Научным центром биомедицинских технологий Федерального медико-биологического агентства позволяет применять его для оценки актопротекторных свойств. Для проведения теста животных (мышей) с дополнительным грузом 6% (аэробная нагрузка) или 10% (аэробно-анаэробная нагрузка) от массы тела, закрепленным на уровне крестца, помещали в резервуар с водой. Емкость для плавания, имеющую форму цилиндра (диаметр – 10 см, высота – 25 см) за сутки до исследования заполняли водой (22–24 °С) на треть объема таким образом, чтобы животное не имело возможности выпрыгнуть или достать до дна хвостом.
Исследование проводили в стандартных условиях (утренние часы, обычный уровень освещения). Животных накануне исследования на ночь оставляли без корма при свободном доступе к воде.
Лабораторным животным после взвешивания, за 45–60 минут до начала тестирования работоспособности зондом перорально вводили расчетную дозу исследуемого препарата. За 15–20 минут до начала тестирования работоспособности (для сглаживания возможной стресс-реакции) на животном фиксировали подобранный груз.
При начале исследования мышь без резких движений погружали в емкость с водой. Секундомер включали при первых плавательных движениях животного. Анализируемым показателем, отражающим физическую работоспособность лабораторных животных, было время предельного плавания животных (время до полного отказа от плавания) [15]. Увеличение длительности плавания мышей в минутах расценивали как повышение физической работоспособности животных.
Оценивали специфическую активность анализируемой субстанции, которая выражается в относительных единицах (по отношению к контролю, в безразмерном варианте или в процентном исчислении), на основе среднегрупповых значений по формуле:
КА – коэффициент активности;
Хпр – значение анализируемого показателя работоспособности при приеме препарата Х;
Хк – в контрольной группе.
Кроме того, определяли коэффициент сравнительной эффективности по формуле:
Хпр – значение анализируемого показателя в условиях тестирования работоспособности при приеме препарата;
Хэ – то же при приеме эталонного препарата.
Статистическую обработку полученных данных для установления различий между группами (например, опытной и контрольной) проводили, используя F-критерий дисперсионного анализа. Числовые данные, приводимые в таблице, представлены в виде:
среднее арифметическое (М) ± стандартная ошибка среднего (m).
Уровень доверительной вероятности был задан равным 95%.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
В процессе разработки новых актопротекторных средств мы считаем целесообразным использовать способность кислот цикла Кребса усиливать антигипоксическую, актопротекторную и ноотропную активность базовых катионных групп в солях. Такое свойство было показано в отношении янтарнокислых солей амтизола, гутимина, этилтиобензимидазола [16], 3-оксипиридина [17], ГАМК [18] и других соединений.
Мы предполагаем, что в химической структуре разрабатываемого перспективного актопротектора должны будут присутствовать следующие фармакофорные группировки:
Подобные структуры, но на основе янтарного эфира диметиламиноэтанола с отчетливым позитивным влиянием на работоспособность, устойчивость к гипоксии и стрессу, воздействию низких температур известны. В медицинской литературе описано антиастеническое действие диметиламиноэтилового эфира янтарной кислоты [19]. Как средство повышения физической работоспособности, особенно при воздействии низких температур, применялся препарат яктон (янтарная соль янтарного эфира диметиламиноэтанола) [20]. Адаптогенное и стресспротективное действие описано для сукцината моно[(2-диметиламино) этилового эфира] янтарной кислоты [21]. Так, при помещении животных на шесть часов в холодовую камеру (–15/–17 °С) применение сукцинатсодержащего препарата увеличивало их выживаемость. На модели двигательного стресса с использованием методики лишения экспериментальных животных сна, пищи и воды в медленно вращающемся барабане препарат показал выраженное защитное действие в отношении как показателей функциональной активности ЦНС, так и развития целого ряда патофизиологических проявлений стресс-синдрома [21].
Известно, что биологическую активность проявляют метильные и этильные производные аминоэтанола, которые являются предшественниками или аналогами холина (триметиламиноэтанола) и ацетилхолина, а также входят в состав фосфолипидов клеточных мембран. Именно эти производные и были использованы при разработке новых соединений.
К гидроксильному остатку аминоэтанола была присоединена фумаровая кислота с образованием фумарового эфира – соответствующего аминоэтанольного производного, ставшего катионной частью будущего соединения. В последующем были получены соли фумаровых эфиров аминоэтанола и кислот цикла Кребса (янтарной, яблочной, кетоглутаровой, фумаровой). На кафедре органической химии в Санкт-Петербургском государственном химико-фармацевтическом университете были синтезированы диэтиламиноэтанол (основание) и восемь соединений, являющихся солями кислот цикла Кребса аминоэтанольных производных фумаровой кислоты (табл. 1).
Для выбора наиболее эффективного из синтезированных соединений был выполнен скрининг фармакологической активности. В качестве скрининговой модели для изучения влияния новых соединений на физическую работоспособность выбран тест предельного плавания с грузом. Результаты выполнения животными этого теста зависят от их общего состояния и работоспособности, их эмоционального статуса, активности, устойчивости к гипоксии [12], что позволяет использовать данную методику в комплексе с другими биомедицинскими методиками для оценки нескольких направлений фармакологической активности, включая актопротекторную. Она стандартизирована и широко используется в биомедицинских исследованиях [15]. Скрининговое исследование выполнено на беспородных белых мышах, температура воды в бассейне 28 ± 1 о С, утяжеление – 6% от массы тела.
Так как для вновь синтезированных соединений не был известен рабочий диапазон доз, то в ходе скринингового исследования оценивалась также зависимость работоспособности животных от введенной дозы соединения. Исследовался диапазон доз от 10 до 75 мг/кг при однократном пероральном введении за час до проведения тестирования. Полученные результаты сопоставлялись не только с контрольной группой животных, которым вводилось эквиобъемное количество физиологического раствора, но и с препаратом сравнения – разрешенным к клиническому применению ноотропным средством аминоэтанольного ряда деанола ацеглуматом и этилтиобензимидазола гидрохлоридом. В каждой группе было по десять животных, что позволяло корректно проводить статистическую обработку данных.
Результаты скрининговой серии исследований представлены в табл. 2.
Анализ полученных данных показывает, что максимально высокую и статистически достоверную фармакологическую активность в скрининговом тесте показывают соединения «Фумарат – ДМАЭ – Фумарат» в дозе 75 мг/кг и «Фумарат – ДЭАЭ – Сукцинат» в дозе 10 мг/кг, а также сам диэтиламиноэтанол (ДЭАЭ основание) в дозе 50 мг/кг. По своему влиянию на работоспособность животных они превосходили препарат сравнения – деанола ацеглумат – в оптимальной дозе 50 мг/кг. Последний обеспечивал повышение времени предельного плавания животных на 74%, в то время как исследуемые соединения показали результаты +175%, +162% и +121% к контролю. Актопротекторная активность соединений «Фумарат – ДМАЭ – Фумарат» и «Фумарат –- ДЭАЭ – Сукцинат» сопоставима с эффектом этилтиобензимидазола гидрохлорида (доза 25 мг/кг).
Так как фармакологическая активность соединения обратно пропорциональна его дозе, вызывающей заданную степень эффекта, то по результатам скринингового исследования более активным может считаться вещество «Фумарат – ДЭАЭ – Сукцинат» (рис. 1).
В условиях аэробно-анаэробной физической работоспособности (плавание мышей с грузом 10%) ФДЭС был изучен в широком диапазоне доз от 1 мг/кг до 300 мг/кг (рис. 2).
Кривая «Доза-Эффект» для ФДЭС при тестировании физической работоспособности животных в тесте вынужденного плавания с грузом 10% представлена на рис. 2.
Доза ФДЭС 75 мг/кг дала наибольший прирост времени плавания. Несмотря на то, что он не достиг статистической значимости различий по сравнению с показателями группы плацебо-контроля, эта доза может быть выбрана для дальнейших исследований, так как в исследованиях других авторов она показала высокую нейротропную активность [22, 23, 24]. Отсутствие статистически значимых различий может быть обусловлено особенностями актопротекторного профиля действия соединения.
ВЫВОДЫ
Результаты проведенного исследования подтвердили, что на мировом фармацевтическом рынке отсутствуют препараты с актопротекторной активностью, разработанные на основе фумаровой кислоты. В связи с этим поиск таких препаратов среди соединений, состоящих из фумарового эфира диэтиламиноэтанола с интермедиатами цикла трикарбоновых кислот, является актуальным.
В процессе разработки новых актопротекторных средств мы считаем целесообразным использовать способность кислот цикла Кребса усиливать антигипоксическую, актопротекторную и ноотропную активность базовых катионных групп в солях.
Янтарная соль фумарового эфира диэтиламиноэтанола обладает актопротекторной активностью, увеличивая выносливость экспериментальных животных при однократном пероральном введении при аэробной и аэробно-анаэробной физической нагрузке.
Выраженность актопротекторного эффекта в условиях аэробной физической нагрузки янтарной соли фумарового эфира диэтиламиноэтанола (доза 10 мг/кг) сопоставима с таковым у этилтиобензимидазола гидро- хлорида (доза 25 мг/кг), но превосходит действие деанола ацеглумат (доза 50 мг/кг).
Актопротекторный эффект янтарной соли фумарового эфира диэтиламиноэтанола реализуется в дозе 75 мг/кг в условиях аэробно-анаэробной физической нагрузки.
Новые соединения фумарового эфира диэтиламино- и диметиламиноэтанола с интермедиатами цикла Кребса по своему влиянию на физическую работоспособность превосходили препарат сравнения – деанола ацеглумат в оптимальной дозе 50 мг/кг. Последний обеспечивал повышение времени предельного плавания животных на 74%, в то время как исследуемые соединения показали результаты +175%, +162%, +121% к контролю. Актопротекторная активность соединений «Фумарат – ДМАЭ – Фумарат» (доза 75 мг/кг) и «Фумарат – ДЭАЭ – Сукцинат» (доза 10 мг/кг) сопоставима с эффектом этилтиобензимидазола гидрохлорида (доза 25 мг/кг).




