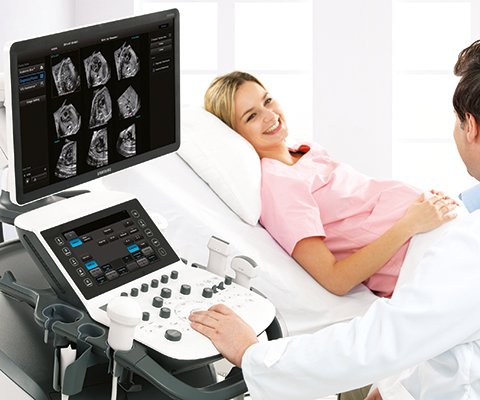
Ультразвук и медицина
УЗИ сканер WS80
Идеальный инструмент для пренатальных исследований. Уникальное качество изображения и весь спектр диагностических программ для экспертной оценки здоровья женщины.
Основные принципы метода и физические характеристики
Скорость ультразвуковых волн в мягких тканях тела человека в среднем составляет 1,540 м/сек и практически не зависит от частоты. Датчик является одним из основных компонентов диагностических систем, который конвертирует электрические сигналы в ультразвуковые колебания и производит электрические сигналы, получая отраженное эхо от внутренних тканей пациента. Идеальный датчик должен быть эффективен как излучатель и чувствителен как приемник, иметь хорошие характеристики излучаемых им импульсов со строго определенными показателями, а также принимать широкий диапазон частот, отраженных от исследуемых тканей.
В электронных датчиках ультразвуковые колебания возбуждаются благодаря подаче высоковольтных импульсов на пьезо-кристалы, из которых состоит датчик (пьезоэлектрический эффект был открыт Пьером и Марией Кьюри в 1880 году). Количество раз, сколько кристалл вибрирует за секунду, определяет частоту датчика. С увеличением частоты уменьшается длина волны генерируемых колебаний, что отражается на улучшении разрешения, однако, поглощение ультразвуковых колебаний тканями тела пропорционально возрастанию частоты, что влечет за собой уменьшение глубины проникновения. Поэтому датчики с высокой частотой колебаний обеспечивают лучшее разрешение изображения при исследовании не глубоко расположенных тканей, так же как низкочастотные датчики позволяют обследовать более глубоко расположенные органы, уступая высокочастотным качеством изображения. Это разногласие является основным определяющим фактором при использовании датчиков.
В ежедневной клинической практике применяются различные конструкции датчиков, представляющие собой диски с одним элементом, а также объединяющие несколько элементов, расположенных по окружности или вдоль длины датчика, производящие различные форматы изображения, которые необходимы или предпочтительны при проведении диагностики различных органов.
Эндоскопическое ультразвуковое исследование
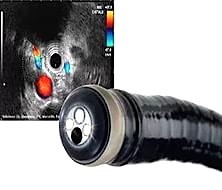
На отделении эндоскопии НМИЦ онкологии им. Н.Н. Петрова исследования проводится с помощью современного ультразвукового комплекса Hitachi-Pentax. Среди дополнительных возможностей этого прибора есть такие как эластография (технология оценки эластичности тканей), цветовой и энергетический допплер (позволяют проследить кровоток в органе). Отделение оснащено ультразвуковыми эндоскопами с датчиками 2-х разных типов: радиальным (используется в целях диагностики) и конвексным (применяется для лечебных процедур).
Показания для выполнения ЭУС:


Эндосонография позволяет визуализировать опухоли поджелудочной железы небольших размеров (менее 3 см), недоступные для стандартного УЗИ и методов компьютерной диагностики, и более точно, чем ангиография, определить инвазию опухоли в сосудистые структуры, что крайне важно для определения возможности хирургического лечения.
Специалисты нашего отделения выполняют эндоУЗИ панкреато-билиарной области не только при доброкачественных или злокачественных новообразованиях, но также и кистах (с целью дифференциальной диагностики с кистозными неоплазиями), остром и хроническом панкреатите (при неясной клинической ситуации и невозможности с помощью прочих методов отличить воспалительные изменения от опухолевых).
Речь идет о дифференциальной диагностике образований желчного пузыря (полипы, аденомиоз, билиарный сладж, конкременты, воспалительные изменения стенки желчного пузыря) и выявлении патологии внепеченочных желчных протоков (опухоли, доброкачественные сужения, конкременты). Метод особенно важен для диагностики поражений терминальных отделов желчного и панкреатического протоков и Фатерова сосочка. Эти зоны малодоступны для других методов диагностики, а новообразования этой области (как доброкачественные, так и злокачественные) встречаются не редко.
Противопоказания для выполнения ЭУС:
Крайне тяжелое общее состояние пациента, которое не дает возможности проводить эндоскопическое исследование верхних отделов пищеварительного тракта без угрозы угнетения дыхания и сердечной деятельности.
Выраженные изменения свертывающей системы крови (если планируются оперативные манипуляции).
Технические ограничения для выполнения ЭУС
Если Вам выполнялись оперативные вмешательства на органах желудочно-кишечного тракта, а также имеются анатомические особенности строения пищевода или желудка, сообщите об этом доктору заранее и покажите выписные справки.
Как осуществляется исследование
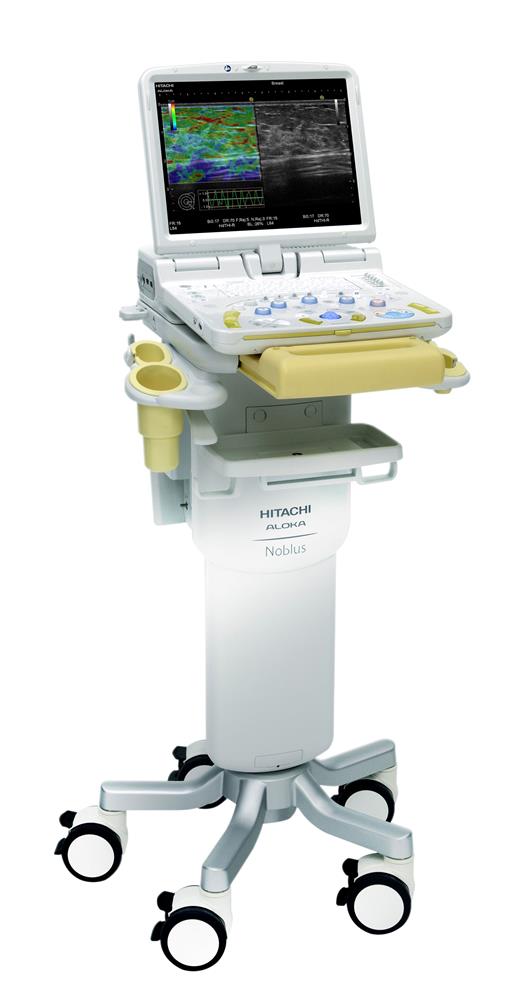
Специалисты нашего отделения рекомендуют выполнять процедуру эндоУЗИ под общей анестезией, препараты для которой вводятся внутривенно, т.к. беспокойное поведение пациента может значительно затруднить работу врача и отрицательным образом повлиять на результат обследования.
После процедуры, выполняемой под наркозом, в течение одного часа у Вас может ощущаться сонливость, вялость. Когда вы полностью восстановитесь, врач обсудит с Вами результаты процедуры.
Оперативные вмешательства под эндоУЗИ-контролем
Как и другие эндоскопические процедуры, эндоУЗИ является безопасным исследованием и хорошо переносится. Однако, как и при других медицинских процедурах иногда возникают осложнения. Частота осложнений при эндоУЗИ без проведения тонкоигольной биопсии составляет около 1 случая из 2000 исследований, что сравнимо с частотой осложнений при ФГС.
Основными серьезными осложнениями могут быть:
Специалисты отделения эндоскопии настоятельно рекомендуют выполнять диагностическое исследование под внутривенной анестезией. Оперативные вмешательства под эндоУЗИ-контролем выполняются под наркозом в обязательном порядке. Для выполнения некоторых лечебных вмешательств может потребоваться госпитализация в стационар.
Для решения вопроса о выполнении оперативного вмешательства под эндоУЗИ-контролем необходима консультация заведующего отделением эндоскопии Ткаченко О.Б.
Синдром недостаточности кровотока в артериях вертебробазилярной системы
Статья посвящена проблеме синдрома недостаточности кровотока в артериях вертебробазилярной системы. Представлены методы диагностики и лечения вертебробазилярной недостаточности, которое должно быть направлено на предупреждение ее прогрессирования, улучшение кровоснабжения мозга, коррекцию отдельных синдромов и симптомов.
Самостоятельное клиническое понятие «синдром недостаточности кровотока в артериях вертебробазилярной системы» сформировалось в 1950-х гг., в период пересмотра взглядов на патогенез ишемических нарушений мозгового кровообращения (НМК) и становления концепции о ведущей роли при этом сосудистой мозговой недостаточности [1].
Особенности строения и функций этой артериальной системы, обеспечивающей питание жизненно важных структур мозга, и своеобразие клинической симптоматики при нарушениях кровотока в ней обусловили выделение ее в последней версии международной классификации в самостоятельный симптомокомплекс — «синдром вертебробазилярной артериальной системы» в рамках «преходящих транзиторных церебральных ишемических приступов (атак) и родственных синдромов» (Международная классификация болезней 10-го пересмотра, G45.0).
Еще раньше группой экспертов Всемирной организации здравоохранения «вертебробазилярная недостаточность» определялась как «обратимое нарушение функции мозга, вызванное уменьшением кровоснабжения области, питаемой позвоночными и базилярной артериями». Подчеркивались ишемическая природа и обратимый характер нарушений, однако не указывалась длительность неврологической симптоматики, что ранее не позволяло отнести их к транзиторным ишемическим атакам (ТИА) и что стало возможным в настоящее время. Нарушения кровотока в артериях вертебробазилярной системы составляют около 70% всех ТИА. Инсульт с локализацией очаговых изменений в областях мозга, получающих кровь по артериям этой системы, развивается в 2,5 раза реже, чем в регионах, относящихся к бассейнам артерий каротидной системы [1].
Причины синдрома недостаточности кровотока в артериях вертебробазилярной системы
Для подключичного «синдрома обкрадывания» характерен феномен, когда у больного во время интенсивной работы руки (кровоснабжаемой ретроградно из контралатеральной позвоночной артерии) возникают стволовые симптомы — чаще всего головокружение.
Определенный вклад в развитие синдрома недостаточности кровотока в вертебробазилярной системе могут вносить изменения реологических свойств крови (повышение уровня фибриногена, вязкости крови, агрегации тромбоцитов и гематокрита, увеличение ригидности эритроцитов), приводящие к ухудшению микроциркуляции.
Диагностика недостаточности кровотока в артериях вертебробазилярной системы
Субъективные данные
Диагноз недостаточности кровотока в артериях вертебробазилярной системы основывается на характерном симптомокомплексе, объединяющем несколько групп клинических симптомов, встречающихся у больных АС и АГ. Это зрительные и глазодвигательные расстройства, нарушения статики и координации движений, вестибулярные нарушения. При этом предположительный диагноз определяется на основе не менее двух из указанных симптомов. Они кратковременны и нередко проходят сами по себе, хотя являются признаком нарушений кровотока в артериях этой системы, что требует клинического и инструментального обследования. Особенно необходим тщательный анамнез для уточнения обстоятельств возникновения тех или иных симптомов [1, 2].
Зрительные нарушения включают в себя ощущение неясности видения, фотопсии, скотомы, изменения полей зрения, снижение остроты зрения и связаны с преходящей ишемией затылочных долей мозга. Неясность видения в форме пелены перед глазами и затуманивания зрения нередко возникает на высоте головной боли. Фотопсии проявляются в виде вспышек цветных точек, чаще всего красных или зеленых, черных, со светлым ореолом, а также пятен, огненных молний, линий, колец, зигзагов. От радужных кругов, характерных для глаукомы, фотопсии отличаются тем, что их появление не связано с внешним источником света; они возникают и при закрытых глазах. Изменение полей зрения наблюдается обычно в форме
их концентрического сужения. Снижение остроты зрения часто развивается после появления головной боли и прогрессирует; зрение заметно ухудшается в период приступов головной боли и после них.
Глазодвигательные нарушения проявляются в виде преходящей диплопии с негрубыми парезами мышц глаза и нарушенной конвергенцией. У большинства больных эти нарушения относятся к начальным проявлениям заболевания, а у четверти из них служат одной из главных жалоб при вертебробазилярной недостаточности.
Статическая и динамическая атаксия относится также к числу постоянных симптомов, которые проявляются жалобами больных на неустойчивость и пошатывание при ходьбе и стоянии. Координация движений нарушена значительно меньше, стойкое изменение ее встречается, как правило, при инфарктах мозжечка.
Вестибулярные нарушения проявляются в виде внезапного головокружения — системного, для которого характерно ощущение «вращения предметов», «перевернутой комнаты», и несистемного с ощущением «укачивания», тошнотой, реже рвотой. Обнаруживается также спонтанный нистагм, иногда только после специальных проб с поворотами головы в сторону и фиксацией ее в этих позах (проба Де Клейна). Развитие головокружения связывают с ишемией или преддверно-улиткового органа, или вестибулярных ядер и их связей. Вестибулярные ядра наиболее чувствительны к ишемии и гипоксии.
При этом головокружение как моносимптом может расцениваться в качестве признака нарушения кровотока в артериях вертебробазилярной системы только в сочетании с другими признаками его нарушения у больных с относительно стойким отоневрологическим симптомокомплексом. Менее известны, хотя встречаются нередко, оптико-вестибулярные расстройства. К ним относятся симптомы «колеблющейся тени» и «конвергентного головокружения», при которых больные испытывают головокружение или неустойчивость при мелькании света и тени или при взоре, направленном вниз.
Характерными симптомами являются приступы внезапного падения без потери сознания («дроп-атаки»), возникающие обычно при резких поворотах или запрокидывании головы. Описан синкопальный вертебральный синдром Унтерхарншайдта, при котором наблюдаются утрата сознания и гипотония мышц при отсутствии данных за эпилепсию и другие пароксизмальные состояния.
К проявлениям диэнцефальных расстройств относятся резкая общая слабость, непреодолимая сонливость, нарушения ритма сна и бодрствования, а также различные вегетативно-висцеральные нарушения, внезапное повышение артериального давления (АД), нарушения сердечного ритма. Эти нарушения связаны с ишемией структур ретикулярной формации ствола мозга.
Описанный симптомокомплекс дополнен в настоящее время другими признаками, которые в сочетании с ними также позволяют судить о недостаточности кровотока в артериях вертебробазилярной системы. На различных стадиях вертебробазилярной недостаточности больные нередко предъявляют жалобы на снижение памяти («забывчивость»), расстройства концентрации и неустойчивость активного внимания. Чаще всего снижается память на имена, числа, недавно происшедшие события. Снижается способность к запоминанию нового материала, становится труднее удерживать в памяти прочитанное, забывается то, что намечено к осуществлению, возникает необходимость записывать. Больным становится трудно осмыслить большое количество информации, что приводит у лиц, занятых умственным трудом, к определенному снижению работоспособности, ограничению творческих возможностей. В то же время профессиональная память и память на прошлые события сохраняются. Это больше относится к оперативной памяти, чем к логической. Нередко снижение памяти и работоспособности расценивается окружающими как результат переутомления, а не как проявление сосудистой мозговой недостаточности. При нейропсихологическом исследовании отмечаются сохранность уровня обобщения, соответствие суждений общеобразовательному и культурному уровню, сохранность запаса представлений и навыков.
Нарушения когнитивных функций существенно снижают качество жизни, а также оказывают влияние на прогрессирование сосудистой мозговой недостаточности.
Снижение памяти на текущие события у больных с вертебробазилярной недостаточностью связано с хронической ишемией медиальных частей височных долей, прежде всего гиппокампа и сосцевидных тел. При вертебробазилярной недостаточности отмечаются и приступы транзиторной глобальной ишемии, при которой на несколько часов нарушается оперативная память (способность к запоминанию новой информации). Больной выглядит рассеянным, он дезориентирован в пространстве и времени, иногда возбужден, настойчиво пытается выяснить у окружающих, где находится, как оказался здесь, но будучи не в состоянии запомнить ответы, постоянно задает одни и те же вопросы. С возвращением способности к запоминанию восстанавливается и ориентация, амнезируется лишь сам эпизод.
Причиной острой амнезии может служить и острое НМК в бассейнах обеих задних мозговых артерий. В этом случае амнезии могут сопутствовать ограничение полей зрения (односторонняя или двусторонняя гемианопсия), зрительная агнозия, алексия, амнестическая афазия, нарушение чувствительности.
Сочетание ряда характерных симптомов позволяет диагностировать синдром недостаточности кровотока в артериях вертебробазилярной системы, хотя при этом определяются лишь ишемический характер НМК и локализация очага ишемии, а не причины, обусловившие этот характер.
Объективные данные
Наиболее доступными и безопасными для определения недостаточности кровотока в артериях вертебробазилярной системы являются неврологический осмотр и ультразвуковые методы исследования сосудистой системы мозга.
Среди объективных признаков, выявляемых при неврологическом осмотре, следует прежде всего назвать нистагм, статическую и динамическую атаксию. В пробе Ромберга больной отклоняется в сторону. Ходьба с закрытыми глазами выявляет у пациента с недостаточностью кровотока в вертебробазилярной системе шаткость и стойкое отклонение в одну из сторон. При проведении пробы Унтербергера пациента просят маршировать на одном месте с закрытыми глазами в течение 1–3 мин. В норме он остается на месте или незначительно смещается относительно исходной точки либо слегка поворачивается вокруг оси. Патологическими считаются смещение вперед более чем на 1 м и поворот более чем на 40–60° (после 50 шагов на месте). Подобным образом интерпретируют результаты пробы Бабинского — Вейля («звездная проба»). Пациента просят с закрытыми глазами сделать два шага вперед, развернуться на 180° и сделать два шага назад. Любые отклонения в сторону или ротация указывают на нарушение функции вестибулярного лабиринта. Если пациента просят пройти в прямом и обратном направлении несколько раз, то в результате отклонения в одну из сторон траектория его движения напоминает очертания звезды (отсюда название пробы).
Необходимо также измерить АД на обеих руках в положении сидя и лежа. К объективным признакам синдрома относятся разница пульса и АД на руках и шум в надключичной области. При значительном снижении систолического АД (более 20 мм рт. ст.) в вертикальном положении симптоматику, напоминающую недостаточность кровотока в вертебробазилярной системе, следует отнести за счет ортостатической гипотензии. Для подключичного «синдрома обкрадывания» характерен феномен, когда у больного на фоне интенсивной работы рукой возникают стволовые симптомы — чаще головокружение.
Ультразвуковая допплерография позволяет получать данные о кровотоке в позвоночных артериях, линейной скорости и направлении потоков крови в них. Компрессионно-функциональные пробы дают возможность оценить состояние и ресурсы коллатерального кровообращения, кровоток в сонных, височных, надблоковых и других артериях. Дуплексное сканирование позволяет определить состояние стенки артерий, строение и поверхность атеросклеротических бляшек, стенозирующих эти артерии. Транскраниальная допплерография с фармакологическими пробами имеет значение для определения церебрального гемодинамического резерва. Исключительно информативны данные о состоянии магистральных артерий головы (МАГ) и интрацеребральных артерий, получаемые при КТ и МРТ в режиме ангиографии. При рентгенографии шейной части позвоночника могут быть получены данные о состоянии структур вокруг позвоночных артерий и воздействии этих структур на позвоночные артерии и кровоток в них; при этом используются функциональные пробы.
Особое место в ряду инструментальных методов занимает отоневрологическое исследование, особенно если оно подкрепляется электронистагмографическими и электрофизиологическими данными о слуховых вызванных потенциалах, характеризующих состояние структур ствола мозга, а также МPТ этих структур.
Алгоритм применения перечисленных инструментальных методов исследования определяется логикой построения клинического диагноза.
Лечение вертебробазилярной недостаточности
Заключение
Следует подчеркнуть, что своевременно начатое и систематически проводимое лечение может предотвратить прогрессирование сосудисто-мозговой недостаточности и значительно улучшить качество жизни пациентов. Особое значение приобретают адекватность и эффективность приема цитиколина (Нейпилепта). Адекватность терапии подразумевает курсовой прием препарата, а также сотрудничество пациента и лечащего врача при назначении и проведении лечения, целями которого являются сохранение трудоспособности и поддержание качества жизни пациента. Могут быть рекомендованы следующие направления оценки эффективности лечения вертебробазилярной недостаточности (уже через 6–12 мес. от начала лечения): уменьшение или исчезновение церебральных жалоб, улучшение когнитивных функций (в первую очередь памяти).
Что такое акустический доступ затруднен на узи
Печень выполняет в организме ряд важных функций, является главным метаболическим центром для поддержания гомеостаза. Около 300 биллионов гепатоцитов здоровой печени функционируют как железы смешанной секреции, в них происходят тысячи биохимических реакций. Основными функциями печени являются: пищеварительная, белково-синтетическая, обменная (участие в обмене углеводов, липидов, витаминов, пигментов, белков), регуляция гемокоагуляции, иммунитета, барьерная функция, метаболизм гормонов [1].
По данным Всемирной организации здравоохранения (ВОЗ), в последние годы отмечается увеличение числа заболеваний печени в общей структуре хронических заболеваний, среди которых первые позиции занимает неалкогольная жировая болезнь печени (НАЖБП). Анализ литературных источников показал, что ее распространенность может составлять от 20 % до 40 %. В Российской Федерации частота выявления НАЖБП выросла в 1,5–2,0 раза [2]. НАЖБП включает в себя следующие клинико-морфологические формы: стеатоз, неалкогольный стеатогепатит и цирроз печени. Важным отличительным признаком неалкогольного поражения печени является отсутствие употребления пациентом алкоголя в гепатотоксической дозе: для мужчин это более 40 г/сут. чистого этанола, для женщин более 20 г/сут. [2].
Учитывая клиническую значимость НАЖБП, малосимптомность начальных стадий, важность своевременного лечения, необходимо сказать о современных методах диагностики заболеваний печени и правильной интерпретации данных. Среди прочих прижизненных методов диагностики патологии печени одно из главных мест занимает ультразвуковое исследование (УЗИ) как наиболее доступный, неинвазивный скрининговый метод.
Все вышесказанное определило цель данного обзора – описание современных возможностей ультразвукового метода и сонографических критериев диагноза НАЖБП, так как на фоне возросшей частоты фиброзно-цирротических поражений печени актуализируются вопросы своевременного выявления и лечения НАЖБП.
Все известные методы диагностики и верификации стеатоза печени, играющего значимую роль в патогенезе цирроза, можно разделить на инвазивные (биопсия печени), малоинвазивные (биохимические, серологические) и неинвазивные (ультразвуковая и компьютерная диагностика).
Стеатоз печени характеризуется повышенным накоплением жира в гепатоцитах, отличается от стеатогепатита отсутствием некроза гепатоцитов и воспалительной инфильтрации в строме. Анализ литературы позволил нам выделить несколько групп патогенных факторов, имеющих первостепенное значение в развитии патологии печени и влияющих на состояние ее паренхимы:
1) токсические факторы;
2) алиментарные факторы;
3) метаболические нарушения;
4) хроническая гипоксия [4].
При этом повреждение может проявляться в форме неалкогольного стеатоза или стеатогепатита.
По мнению ряда авторов, стеатоз развивается постепенно и в своем развитии проходит несколько стадий:
1) первоначальное накопление жиров в цитоплазме гепатоцита, которое не приводит к деструкции клетки, сохраняется ее внутренняя дифференциация;
2) развитие некробиоза клеток печени;
3) перестройка архитектоники печени и нарушение ее дольковой структуры [2, 4].
По данным морфологических исследований, возможно развитие мелкокапельной и крупнокапельной жировой дистрофии гепатоцитов. Более тяжелой формой является мелкокапельное повреждение, когда в цитоплазме клетки накапливаются включения фосфолипидов. Ядро клетки не смещается к периферии. При этом цитоплазма имеет пенистый вид. Такая перестройка клетки приводит к нарушению процессов окисления в митохондриях, дефициту энергии, некрозу клетки [5].
Наиболее частой формой повреждения гепатоцитов при стеатозе является крупнокапельная дистрофия, когда в цитоплазме появляются одна или две крупные капли нейтрального жира, смещающие ядро клетки к периферии. Такая морфологическая картина при отсутствии других признаков является основанием для постановки диагноза стеатоза. Морфологическая градация степени тяжести стеатоза осуществляется полуколичественным методом по количеству пораженных гепатоцитов в биоптате: 0 – менее 5 %; 1 – от 5 % до 33 %; 2 – от 33 % до 66 %; 3 – более 66 % [5, 6].
Применение биопсии печени целесообразно только в том случае, когда риск проведения данной манипуляции не превышает ее пользу для пациента. Безусловной альтернативой в данном случае являются неинвазивные методики.
Ультразвуковое исследование, выполненное на современном аппарате и включающее допплерографию сосудов печени с использованием цветового допплеровского картирования, импульсноволнового допплера, тканевой гармоники, может быть эффективным диагностическим методом в 70 % случаев [7].
Нужно отметить, что по данным УЗИ дифференцировать стеатоз и стеатогепатит нельзя, как и стеатогепатит алкогольный и неалкогольный [7].
В специальной литературе существует традиционное описание сонографической картины здоровой печени, когда неизмененная паренхима представляет собой мелкозернистое однородное изображение, по всей поверхности визуализируемого среза лоцируются мелкие трубчатые структуры, являющиеся протоками и сосудами печени. Крупная зернистость паренхимы печени может рассматриваться как вариант нормы при условии сохранения ее однородности.
Известным эталоном нормальной эхогенности паренхимы печени является таковая в корковом слое почки. В некоторых случаях изменение данной эхографической характеристики может рассматриваться как норма (например, гиперэхогенность в области ворот печени или гипоэхогенность хвостатой доли) [8]. Важным критерием сонографического заключения является также звукопроводимость, которая в норме позволяет визуализировать глубокие слои печени и диафрагму. При наличии стеатоза это становится невозможным, возникает эффект затухания эхосигнала к периферии [7, 8].
Основными ультразвуковыми показателями при исследовании печени являются следующие нормальные характеристики: косой вертикальный размер (КВР) правой доли печени, по данным разных авторов, в норме до 15 см (заключение о наличии гепатомегалии делают при увеличении данного показателя более 17 см), КВР левой доли печени в норме до 6–8 см; диаметр воротной вены в норме 0,8–1,2 см, до 1,3 см; диаметр нижней полой вены до 1,8 см; диаметр холедоха до 0,3–0,5 см. Признаком портальной гипертензии является диаметр воротной вены более 1,4 см. Диаметр селезеночной вены в норме 0,6–0,8 см, диаметр верхней брыжеечной вены в норме до 0,8–1,1 см, на выдохе 0,4–0,6 см, если на выдохе диаметр верхней брыжеечной вены уменьшается вдвое и более, то портальная гипертензия отсутствует [8].
При описании структуры печени для диагностики жировой дистрофии учитывают следующие сонографические характеристики: наличие гепатомегалии, округлый контур нижнего края печени, однородность структуры, гиперэхогенность, сглаженность зернистости при уменьшении звукопроводимости, обеднение и сглаженность сосудистого рисунка [8, 9].
Общими ультразвуковыми признаками стеатоза при проведении рутинного исследования с применением серошкальной шкалы являются следующие:
1) гепатомегалия, форма печени не нарушена, контур четкий, ровный, закругленный;
2) диффузное уплотнение паренхимы печени с повышением ее эхогенности и снижением звукопроводимости, что пропорционально степени выраженности стеатоза;
3) обеднение и сглаженность сосудистого рисунка, что связано с повышением эхогенности паренхимы печени; сначала затруднена визуализация мелких сосудов, а затем и более крупных;
4) появление эффекта дистального ослабления эхосигнала [9].
Анализ литературы по теме исследования показывает, что изменения, характерные для стеатоза, могут диффузно распространяться по всей поверхности печени или же образовывать изолированные участки жировой инфильтрации (очаговая форма).
На основании вышесказанного выделяют сонографические степени выраженности стеатоза:
I степень – незначительное диффузное увеличение эхо-сигналов в паренхиме печени, нормальная визуализация границ диафрагмы и внутрипеченочных сосудов;
II степень – уплотнение паренхимы печени с повышением ее эхогенности, выраженное обеднение сосудистого рисунка; визуализация крупных сосудов, границ диафрагмы; эффект дорсального затухания эхосигнала;
III степень – структура печени значительно уплотнена; выраженное обеднение сосудистого рисунка, при котором даже крупные сосуды печени просматриваются очень плохо; диафрагма не визуализируется; выраженный эффект дорсального затухания эхосигнала, при котором нижний край печени практически не визуализируется [9, 10].
По данным литературы, метод УЗИ является высокочувствительным в диагностике тяжелой степени стеатоза и имеет наименьшую эффективность при выявлении легкой степени стеатоза.
Ультразвуковыми признаками цирроза являются следующие:
1) увеличение краниокаудального размера печени более 15 см;
2) косо-вертикальный размер больше 17 см;
3) толщина левой доли более 8 см;
4) толщина хвостатой доли более 2 мм, ее краниокаудальный размер более 8 см;
5) заостренный нижний край печени;
6) бугристость контура за счет узловой регенерации паренхимы (специфичность этого признака при крупноузловом циррозе составляет 98 %);
7) гиперэхогенность паренхимы, неоднородность зернистости печени и отсутствие мелкососудистого рисунка по периферии;
8) четкое прослеживание контура диа- фрагмы;
9) отсутствие эффекта дистального затухания эхосигнала [10].
При допплерографии отмечаются замедление кровотока, обратный ток крови в воротной вене, увеличение скорости и объема кровотока в печеночной артерии.
В последние годы возрастает потребность в неинвазивных методах диагностики заболеваний печени, патогенез которых составляют прогрессирующий склероз и фиброз паренхимы. Определение эластичности ткани возможно с применением ультразвуковых систем с функцией различных видов эластографии:
1) статической или компрессионной;
2) динамической с оценкой показателей распределения сдвиговых волн.
Статическая эластография позволяет провести оценку эластичности ткани при помощи компрессии ультразвуковым датчиком, которую осуществляет врач-оператор с частотой 2 раза в секунду. Этот метод не дает возможности получить числовые показатели модуля упругости в килопаскалях (кПа) и числовые показатели эластичности печени.
Цветное картирование зоны интереса в данном случае может показать различную плотность паренхимы и является удобным при скрининге локальных образований в печени. Для оценки диффузных поражений при фиброзе данный метод неэффективен. Оценить эластичность печени можно при помощи динамической (транзиентной) эластографии, которую проводят с использованием аппарата Fibroscan (Echosens, Франция) [11]. Методика описана в специальной литературе, поэтому в рамках данной статьи мы не будем подробно останавливаться на вопросах проведения процедуры. Основой метода является механическая вибрация, которая генерирует упругие поперечные волны, скорость их распространения выражается в килопаскалях, при этом она прямо коррелирует с упругостью ткани: чем больше плотность ткани, тем быстрее распространяется поперечная волна.
Согласно отчетам Европейской федерации обществ ультразвука в медицине и биологии (EFSUMB), референсные значения выше 1,5–5,8 кПа говорят об отсутствии фиброза; 5,9–7,2 кПа соответствуют 1-й степени фиброза; 7,3–9,5 кПа – 2-й степени фиброза; 9,6–12,5 кПа – 3-й степени; более 12,5 кПа – 4-й степени, имеется цирротическое поражение [11]. Ограничениями к применению данной методики являются тяжелые степени ожирения пациента и асцит.
Необходимость доступной количественной оценки жесткости ткани, выраженной как модуль Юнга (кПа) или скорость сдвиговой волны (м/с), привела к созданию современных ультразвуковых систем, применение которых позволяет получить значение эластичности ткани печени в режиме реального времени. Значение скорости сдвиговой волны можно переводить в значения модуля Юнга по следующей формуле: E ≈ 3ρcs 2 (Па) где E – модуль Юнга (Па), ρ – плотность ткани (≈1000 кг/м3), сs – скорость сдвиговой волны (м/с). Повышение значений модуля Юнга или скорости сдвиговой волны говорит о высокой жесткости ткани [12].
Эластометрия с применением форсированного импульса акустической радиации (ARFI) с помощью системы Acuson S2000™ (Siemens, Германия) – это метод эластографии, интегрированный в стандартные ультразвуковые аппараты. Для получения результата требуется 10 валидных измерений, из которых рассчитывается среднее значение скорости сдвиговой волны (см/сек). Эластометрия с применением ARFI имеет более низкую частоту ошибок измерений, чем транзиентная эластография [11, 12].
В мировой и отечественной практике существуют современные аппаратные ультразвуковые системы, которые, помимо традиционного сканирования в В-режиме, обладают функцией эластометрии и двухмерной сдвиговолновой эластографии для определения степени фиброза печени, оценки коэффициента затухания для количественного анализа степени выраженности стеатоза [12, 13]. Измерение степени выраженности стеатоза проводится в соответствии с морфологической шкалой и выражается в дБ/см.
Значение до 2,2 дБ/см – стеатоз отсут- ствует;
1-я степень – от 2,2 до 2,32 дБ/см;
2-я степень – от 2,33 до 2,9 дБ/см;
3-я степень – более 2,91 дБ/см [13].
Таким образом, применение неинвазивных методик оценки эластичности паренхимы печени в сочетании со сканированием в В-режиме и допплерографией становится частью стандартного обследования пациентов с НАЖБП, так как инвазивные диагностические методики при помощи биопсии не всегда применимы. Возросшая потребность в скрининге и мониторировании пациентов с болезнями печени актуализирует вопросы разработки и внедрения новых информативных и доступных методов неинвазивной диагностики стеатоза и фиброза печени. В настоящее время идет активное изучение сразу нескольких методик визуализации печени: магнитно-резонансной и транзиентной эластографии, УЗИ с контрастным усилением и др. Это расширяет возможности своевременной прижизненной диагностики болезней печени с определением показателей клинического прогноза. Указанные методики могут занять полноправное место в ряду многочисленных диагностических мероприятий.