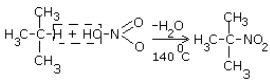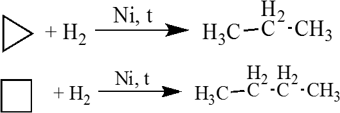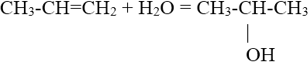Лекции 20, 21 Углеводороды: алканы, алкены, алкены, арены



В основе названия углеводородов по систематической заместительной номенклатуре лежат принципы отраженные в схеме:

|
|
|
 |  |
 |  |

|
|
|
|
|

алканы алканы алкены алкины
2. Название насыщенных углеводородов, которые берутся для основы названия всех остальных органических соединений ( корни греческих числительных выделены):
Таблица 1.
| Число атомов С | Название | Число атомов С | Название | Число атомов С | Название |
| С1 | Мет ан | С7 | Гепт ан | С13 | Тридек ан |
| С2 | Эт ан | С8 | Окт ан | С20 | Эйкоз ан |
| С3 | Проп ан | С9 | Нон ан | С21 | Генэйкоз ан |
| С4 | Бут ан | С10 | Дек ан | С22 | Докоз ан |
| С5 | Пент ан | С11 | Ундек ан | С30 | Триаконтан |
| С6 | Гекс ан | С12 | Додек ан | С40 | Тетраконтан |
Таблица 2. Название греческих числительных, при помощи которых указывается число одинаковых заместителей
Таблица 3. Названия заместителей
3) Последовательность действий при составлении названий органических углеводородов и их производных.
A. Названия углеводородов с неразветвленной цепью.
1. Названия алканов приведены в таблице 1.
2. В основу названий алкенов и алкинов положены названия алканов, в которых суффикс –ан заменен соответственно на суффикс –ен или суффикс –ин. В конце указываем арабской цифрой положение кратной связи.
B. Названия углеводородов с разветвленной цепью.
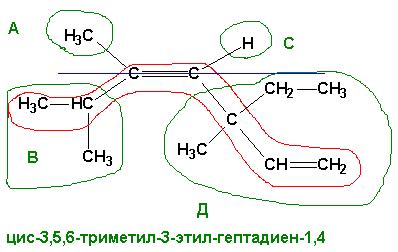
1. Находим главную цепь:
2) Включает двойную, тройную связь,
2. Нумеруем с того конца, к которому ближе
1) 
2) Двойная связь приоритет возрастает
3) 
4) В алфавитном порядке указываем при помощи арабских цифр положение заместителей (названия см. в таблице 3).
5) Предпочтение отдаем варианту, в котором первая отличающаяся цифра наименьшая.
6) При помощи приставки (см. таблицу 2) указываем число одинаковых заместителей.
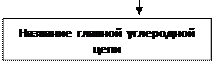
7) Добавляем название главной цепи в соответствии с числом атомов углерода, содержащихся в ней (см. выделенные корни в таблице 1)
8) В случае алкенов и алкинов в конце названия прибавляем соответствующий суффикс –ен или –ин.
9) Указываем арабской цифрой положение кратной связи (предпочтение отдаем варианту, в котором цифра наименьшая).
C. Между цифрой и буквой ставим дефис, между цифрами – запятую. Основой названия ароматических углеводородов является название простейшего представителя – бензола.

АЛКАНЫ,АЛКЕНЫ, АЛКИНЫ И АЛКАДИЕНЫ
3.1 Алканы: определениек,изомерия и номенклатура
Для предельных углеводородов характерна структурная изомерия. Изомеры этого типа отличаются друг от друга порядком связей между отдельными атомами в молекуле (структурой углеродной цепи).

Способы получения алканов
Главным природным источником предельных углеводородов является нефть, а для первых членов гомологического ряда – природный и попутный газы.
Выделение индивидуальных соединений из нефти или продуктов ее крекинга – задача весьма трудоемкая, поэтому приходится прибегать к синтетическим методам получения.
1. Алканы могут быть получены при восстановлении алкенов или алкинов водородом в присутствии катализаторов. Катализаторами гидрирования и дегидрирования чаще всего используют специальным образом обработанные металлические платину, палладий или никель.
2. Самые разнообразные производные алканов могут быть восстановлены при высокой температуре восстановителями или водородом на катализаторе. Обычно эта реакция используется для восстановления галогенопроизводных:
бромистый этил этан
3. Предельные углеводороды образуются при действии воды на металлоорганические соединения:
бромистый этилмагний этан
4. В лабораторной практике алканы получают сплавлением солей карбоновых кислот со щелочами:
ацетат натрия метан
5. При действии металлического натрия на моногалогенопроизводные (реакция Вюрца):
2 CH3─CH2─J 
Если в реакции Вюрца участвуют два типа галогенопроизводных, то образуется смесь трех различных алканов, так как вероятность встречи в реакционном комплексе молекул одинаковых или разных равна:
6. Электролиз солей карбоновых кислот (реакция Кольбе):
Анионы кислотного остатка окисляются на аноде с образованием свободных радикалов:
которые объединяются в молекулы предельных углеводородов:
Физические свойства
Согласно теории химического строения А.М.Бутлерова, физические свойства алканов, как и других органических соединений, определяются их составом и строением.
В гомологическом ряду предельных углеводородов четыре первых члена при обычной температуре – газы, далее следуют жидкости и, начиная с С16Н34 – твердые вещества.
Алканы – вещества неполярные и труднополяризуемые. Растворимость их в воде ничтожна. Атомы в молекулах предельных углеводородов соединены только σ-связями. Расстояния между соседними углеродными атомами 0,154 нм. В коротких цепях по С-С связям возможно свободное или почти свободное вращение.
ЯМР-спектры алканов трудно расшифровываются, так как химические сдвиги различным образом расположенных протонов имеют близкие значения (около 0,5 – 2 м.д.)
Химические свойства
Химические превращения предельных углеводородов могут происходить либо за счет разрыва цепи углеродных атомов, либо за счет отрыва атомов водорода с последующим замещением их другими атомами или группами. Поэтому для предельных углеводородов характерны реакции расщепления и замещения.

Процессы расщепления связей С-С или С-Н с образованием свободных радикалов требуют большой энергии активации и поэтому при обычной температуре идут только в присутствии катализаторов.
Место вступления заместителя в молекулу алкана определяется в первую очередь вероятностью образования того или иного радикала, т.е. прочностью связей водородного атома с углеродом и стабильностью возникающего радикала.
Радикальное галогенирование
Замещение водородных атомов на галоген – одна из наиболее характерных реакций предельных углеводородов. С F2 реакция идет со взрывом, а с J2 – процесс ограничен равновесием, т.к. йодистый водород восстанавливает образующиеся йодистые алкилы. Следовательно, скорость галогенирования с одной стороны зависит от природы галогена (F>>Cl>Br>J), а с другой от строения углеводорода. Общеизвестно, что легче всего галогенирование протекает по третичному углеродному атому, а труднее всего – по первичному.
Галогеном можно заместить как один атом водорода в молекуле, так и все.
Галогенирование алканов на свету или под действием высоких температур протекает по цепному радикальному механизму и является типичным примером радикального замещения (SR).
На первой стадии под влиянием света происходит гомолитический разрыв связи в молекуле брома и она распадается на два радикала:
Br2 
Атом или молекула подобного типа, содержащие неспаренный электрон, называются свободными радикалами и, как правило, существуют лишь доли секунды, так как мгновенно реагируют с присутствующими веществами.
Поэтому на следующей стадии реакции радикал Br • атакует молекулу метана, образуя бромистый водород и углеводородный радикал – метил:
Образовавшийся органический радикал атакует молекулу брома и регенерирует радикал галогена:
Этот процесс может продолжаться бесконечно долго, но на практике течение цепных реакций ограничивается так называемыми процессами обрыва цепи, при которых радикалы, реагируя один с другим, выбывают из процесса:
Кроме того, они могут взаимодействовать с примесями или со стенками сосуда.
Нитрование
Концентрированная азотная кислота при обычной температуре почти не действует на предельные углеводороды, а при нагревании действует как окислитель. М. И. Коновалов предложил проводить нитрование предельных углеводородов разбавленной азотной кислотой при нагревании (около 140 о С). По механизму реакция нитрования является свободно радикальным процессом:
В случае разветвленной молекулы алкана легче всего замещается водород у третичного углеродного атома. В промышленных условиях нитрование осуществляют оксидами азота.
39. Органическая химия  Читать 0 мин.
Читать 0 мин.
39.190. Углеводороды – алканы, алкены, циклоалканы
Алканы и циклоалканы
Алканы
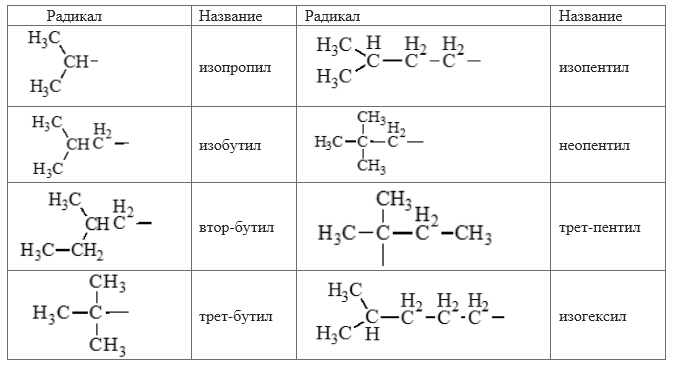
Ряд метана
Таблица изомеров и название радикалов
Изомерия алканов и циклоалканов:
1. Углеродного скелета
Пространственные изомеры могут быть у циклоалканов:
Конформеры находятся в динамическом равновесии и превращаются друг в друга через нестабильные формы. Неустойчивость плоских циклов вызвана значительной деформацией валентных углов. При сохранении тетраэдрических валентных углов для циклогексана C 6 H 12 возможны две устойчивые конформации: в форме кресла и в форме ванны:
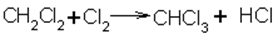
Химические cвойства алканов:
СH 4 +Cl 2 =CH 3 Cl+HCl
С 5 H 12 +8O 2 =5CO 2 +6H 2 O
Это свойство используется при получении синтетических моющих средств.
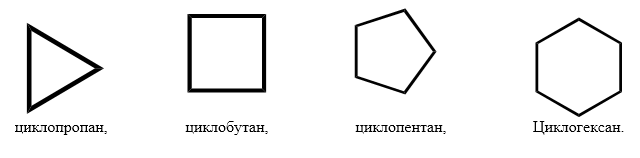
Химические свойства циклоалканов:
Наиболее устойчивыми являются 6-членные циклы, в которых отсутствуют угловое и другие виды напряжения.
1. Малые циклы (С 3 — С 4 ) довольно легко вступают в реакции гидрирования:
Циклопропан и его производные присоединяют галогены и галогеноводороды:
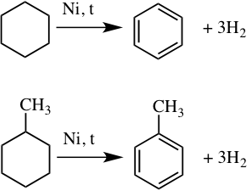
В других циклах (начиная с С 5 ) угловое напряжение снимается благодаря неплоскому строению молекул. Поэтому для циклоалканов (С 5 и выше) вследствие их устойчивости характерны реакции, в которых сохраняется циклическая структура, т.е. реакции замещения.
2. Эти соединения, подобно алканам, вступают также в реакции дегидрирования, окисления в присутствии катализатора и др.
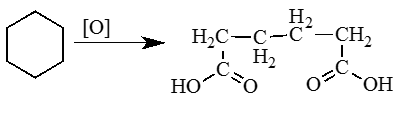
3. Окисление циклоалканов (циклогексан).
Алкены
Алкены
Ряд этилена
Виды изомерии:
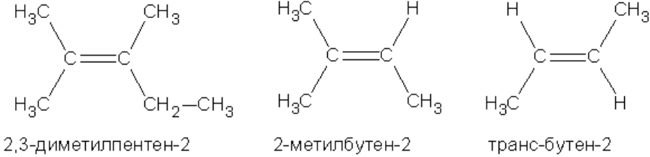
Помимо изомерии, связанной со строением углеродной цепи, в ряду олефинов наблюдается изомерия положения двойной связи. Кроме того, у олефинов имеет место пространственная (геометрическая) или цис-транс-изомерия.
Для изучения материала по названному виду изомерии необходимо просмотреть анимационный фильм “Цис-транс-изомерия в ряду алкенов”. Обращаем внимание на то, что текст, сопровождающий этот фильм. в полном объеме перенесен в данный подраздел и ниже следует.
Цис-транс-изомерия в ряду алкенов
Наряду с изомерией, связанной со строением углеродного скелета и положением двойной связи, в ряду алкенов имеет место геометрическая или цис-транс-изомерия. Ее существование обусловлено отсутствием свободного вращения атомов, связанных двойной связью.
Химические свойства алкенов:
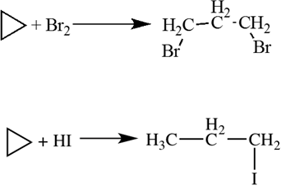
1. Присоединение галогенов.
CH 2 =CH-CH 3 +Cl 2 →CH 2 Cl-CHCl-CH 3
2. Присоединение водорода.
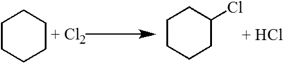
3. Присоединение галогенводородов.
Присоединение протекает по правилу Марковникова (водород присоединяется к наиболее гидрогенизированному атому углерода).
4. Присоединение воды.
5. Окисление перманганатом калия в нейтральной или слабощелочной среде (реакция Вагнера).
Что такое алкины алканы алкены алкины
томский государственный университет
кафедра органической химии
Лекция № 2. Алкены, алкадиены, алкины (ненасыщенные углеводороды).
К ненасыщенным (непредельным) углеводородам относятся алкены (СnH2n), алкадиены (CnH2n-2) и aлкины (CnH2n-2), содержащие кратные связи углерод-углерод. Алкены содержат ОДНУ двойную связь С = С, углероды при двойной связи находятся в состоянии гибридизации sp2. Двойная связь образована перекрыванием:
а) sp2- гибридизованных орбиталей атома углерода (s-связь) и
б) перекрыванием негибридизованных р-орбиталей (p-связь). Алкадиены содержат ДВЕ кратные связи в молекуле. В зависимости от взаимного расположения кратных связей одна относительно другой, различают:
а) кумулированные диены:
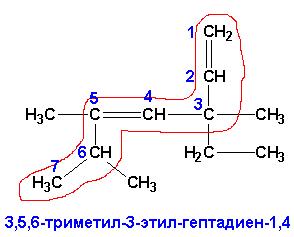
СН3-СН = С = СН-СН2-СН2-СН3 ( гептадиен-2,3 ) или СН3-СН2-СН2-СН = С = СН2 ( гексадиен-1,2 ) (кратные связи расположены по соседству);б) сопряженные алкадиены (или просто диены, кратные связи расположены через одну простую):СН3-СН = СН-СН = СН-СН2-СН3 ( гептадиен-2,4 )в) изолированные диены (кратные связи разделены более, чем одной простой):СН2 = СН-СН2-СН2-СН = СН-СН3 ( гептадиен-1,5 )Все три типа диенов различаются по химическим свойствам. Только изолированные диены ведут себя как обыкновенные алкены, поскольку кратные связи не оказывают взаимного влияния в их молекулах. Номенклатура алкенов Номенклатура алкенов весьма сходна с номенклатуроой алканов за тем исключением, что при наименовании за основу выбирается наиболее длинная цепь углеродных атомов, ВКЛЮЧАЮЩАЯ в себя КРАТНУЮ связь (выделена красным), цепь нумеруется с того края, к которому ближе расположена(ы) кратная(ые) связь(и):
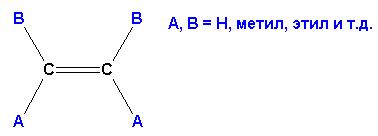
Если требование выполняется, то пространственные изомеры имеются. Если хотя бы у одного из углеродов при кратной связи имеются ОДИНАКОВЫЕ заместители, пространственная изомерия невозможна. В приведенном выше соединении возможно следующее пространственное расположение атомов и групп:
Если основная цепь углеродов расположена ПО ОДНУ СТОРОНУ от оси кратной связи, то такой изомер является ЦИС- изомером, если основная цепь пересекает ось кратной связи (располагается по обе стороны от оси) – это ТРАНС- изомер. Изомерию в данном случае обеспечивает кратная связь между 4 и 5 атомами углерода, в то время как кратная связь между 1 и 2 атомами углерода не может давать различного пространственного расположения заместителей при ней (одинаковые атомы водорода при С1).
Общие свойства ненасыщенных (непредельных) углеводородов
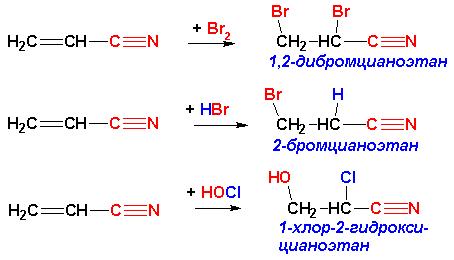
Это правило, справедливое лишь для реакций электрофильного присоединения к алкенам, имеет современное обоснование, позволяющее объяснить аномальное присоединение в случае электроноакцепторных заместителей при кратной связи:
Другие реакции алкенов и алкинов.
Реакции окисления. При взаимодействии с растворами KMnO4 на холоду происходит образование двухатомных спиртов (гликолей) из алкенов:
При взаимодействии с горячими растворами KMnO4, а также с энергичными окислителями происходит разрыв молекулы по месту кратной связи и образуются карбоновые кислоты, вне зависимости от того, двойная это была или тройная связь:
Озонирование с последующей обработкой продуктов (озонидов) водой приводит к образованию альдегидов и кетонов (в случае алкенов) или карбоновых кислот (алкины):
Отличительные реакции алкинов.
Вследствие того, что sp-гибридизованный углерод алкинов является более электроотрицательным, водород при атоме углерода с тройной связью обладает значительно более кислыми свойствами, чем водород при sp2-гибридизованном углероде в алкенах и еще значительней- чем водород при sp3-гибридизованном углероде алканов. В связи с этим для алкинов с концевой тройной связью характерны реакции замещения водорода :
Если замещение на атомы щелочных металлов происходит только при действии очень сильных оснований (NaNH2, NaH, бутил-натрий и т.п.), то замещение тяжелыми металлами (Cu, Ag, Hg) протекает очень легко, в водных растворах при комнатной температуре. Ацетилениды тяжелых металлов в сухом состоянии неустойчивы и разлагаются со взрывом.
В промышленности важным источником непредельных соединений являются продукты крекинга и пиролиза нефтяных фракций, а также газы коксования (этилен, пропилен).
С той же целю часто применяются способы дегидрогенизации алканов на катализаторах:
Катализатором этого процесса обычно является специальным образом приготовленная окись хрома Cr2O3 при 300 оС.
1. Обычным способом получения алкенов в лабораторных условиях является дегидратация спиртов :
Катализаторами дегидратации служат минеральные кислоты. Процесс дегидратации протекает по следующему механизму:
На этапе отщепления молекулы воды образуется карбкатион. Образовавшийся карбкатион очень часто претерпевает изомеризацию (в результате гидридного или алкильного сдвига), при этом может даже измениться углеродный скелет молекулы.
Карбкатион отщепляет протон и превращается в алкен. Обычно существует два возможных варианта отщепления протона (от одного из соседних с заряженным атомом углерода положений), поэтому получается два разных продукта. В качестве основного продукта образуется наиболее устойчивый алкен (правило Зайцева). Наиболее устойчивыми являются транс-изомеры максимально замещенных алкенов, с минимальными стерическими затруднениями, создаваемыми соседними группировками.
2. Алкены получают дегидрогалогенированием (отщеплением галогеноводорода) галоидных алкилов :
3. Метод ДЕГАЛОГЕНИРОВАНИЯ вицинальных (“рядом стоящих”) дигалогеналкилов является способом получения чистых алкенов. Полученных продукт содержит кратную связь в том месте, где находились галогены:
4. В редких случаях алкены получают гидрированием более доступных алкинов :
Методы получения алкинов
1. Наиболее часто алкины получают дегидрогалогенированием дигалоидных алканов (вицинальных или геминальных):
Как и в случае алкенов, реакцию ведут в спиртовых растворах щелочей. Вначале отщепляется одна молекула галогеноводорода. Образующийся галоидзамещенный алкен отщепляет вторую молекулу галогеноводорода с гораздо бОльшим трудом, чем первую. Для получения алкинов отщепление второй молекулы галогеноводорода требует применения твердой щелочи при нагревании или более сильного основания, такого, как амид натрия NaNH2.
2. Алкилированием ацетилена могут быть получены многие другие алкины (гомологи ацетилена). Реакция проводится в две стадии. Вначале получают ацетиленид щелочного металла:
Полученные металлорганические производные ацетилена алкилируют галоидными алкилами:
Операции можно повторить и заместить таким образом второй атом водорода у ацетилена, но обычно получить в чистом виде моноалкилацетилены невозможно, так как получается смесь моно- и дизамещенных ацетиленов.






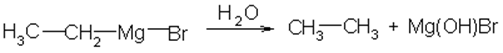






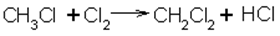


 Читать 0 мин.
Читать 0 мин.