Общее понятие
Аллотропия проявляется, благодаря разному составу микрочастиц простой материи и координируется вариантом размещения молекул и атомов в кристаллической решетке. Вещество кристаллизуется в нескольких модификациях, при этом два параметра простой ячейки совпадают. Изменение состояния происходит из-за отличия третьего показателя, который учитывает расстояние между сопредельными слоями.
Явление часто обнаруживается в структурах, которые равнозначны гексагональному и кубическому расположению атомов. Соседняя атомная среда представляет эквивалентное окружение, а различия проявляются на удаленных сферах. Энергетические характеристики решеток приблизительно равны, поэтому физические свойства разных состояний одного элемента остаются похожими.
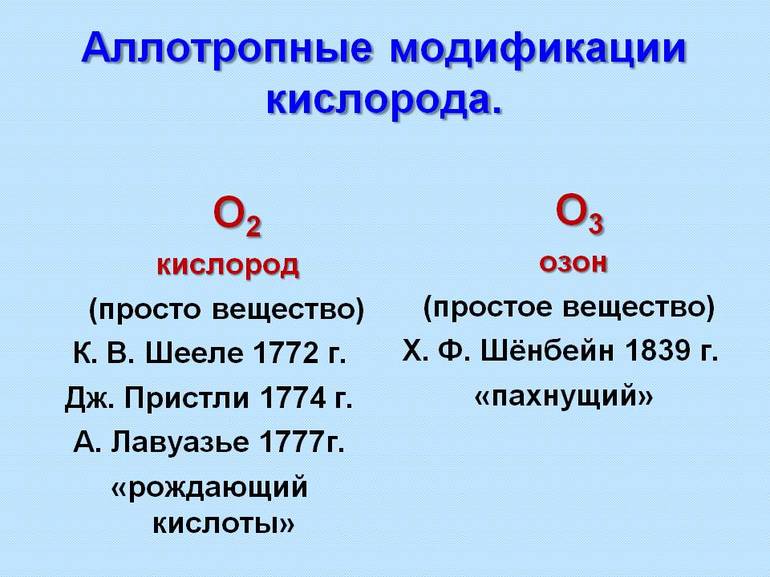
Первые примеры аллотропных модификаций показал шведский минералог и химик Берцелиус середине XIX века для выделения различных форм нахождения элемента. Через 2 десятка лет была принята гипотеза итальянского химика А. Авогадро о многоатомных молекулах и стало видно, что от строения частиц зависит проявление элемента в материи. Например, О3 — озон, а О2 — кислород.
В 1912 году ученые определили, что различия в структуре простых элементов, например, фосфора или углерода, относятся к первопричинам существования двух и более состояний. В настоящее время аллотропией называется видоизменение простых материй, независимо от агрегатного вида. Изменения в твердых состояниях сложных и простых веществ имеет название полиморфизма. Два определения совпадают, если речь идет о простых материалах в твердом виде (железо, сера в кристаллах, фосфор).
Реорганизация веществ
Продолжаются открытия видов простых материалов, способных к аллотропии, несмотря на то, что список образовательных веществ уже превышает 400 материалов. Типы химических связей в элементарных частицах зависят от строения атома, вместе эти характеристики определяют возможность вещества образовывать разные аллотропные формы.
Компоненты, которые могут изменять показатель координационного числа и стадии окисления, образовывают большее количество аллотропных состояний. Важным фактором разнообразия форм является способность элемента к образованию гомоцепных решеток (состоящих из однотипных атомов).
Преобразование простых элементов
Более выраженными являются аллотропные модификации неметаллов, но среди веществ этой группы имеются исключения, например, благородные газы и галогены. Некоторые состояния отличаются температурной стабильностью, другие характеризуются фазовой динамикой. Такие различия объясняются затратами некоторой энергии при изменении кристаллической решетки в результате плавления.
Примеры реорганизации неметаллов:
Разные состояния одного компонента обозначаются строчными литерами греческой латиницы для написания в формулах. Низкотемпературные формы отмечаются буквой α, следующие состояния по показателям обозначаются β и дальше по такому принципу.
Модификации полупроводников
К этой группе относятся элементы, располагающиеся в таблице на переходе от металлов к неметаллам. У материалов присутствует кристаллическая ковалентная решетка, чаще они характеризуются проводимостью по типу металлов. Иногда материалы работают как полупроводники.
Примеры трансформации неметаллов:
К особенностям относится слабое сочетание зоны проводимости и валентной области. Это обеспечивает электропроводность до того времени, пока температура не снизится до 0ºС. Нагревание способствует увеличению электронных дырок (обладателей тока), но видоизменение идет слабо. Положительные квазичастицы в полуметаллах активно двигаются при малой полезной массе. По этой причине материалы больше других веществ подходят для изготовления фазовых переходов в магнитных полях большой силы, наблюдения квантовых и классических размерных эффектов.
Особенности видоизменения металлов
Металлы образовывают различные состояния при увеличении давления или в случае технологической обработки. Аллотропной модификацией металлов называется возможность материала в твердой форме образовывать различные виды кристаллических решеток. Процесс перехода от одной структуры к другой рассматривается в виде превращения.
Обследование структуры производится способом микроанализа, делается ультразвуковая, магнитная и рентгеновская дефектоскопия.
Микроанализ проводится на основе снятия микрошлифов, которые перед исследованием полируются до блеска. Вывод о структуре делается после рассмотрения срезов под микроскопом после травления. Шлифы показывают границы зерен из-за неодинаковой обработки основного слоя и рельефных выступов. Анализ выявляет форму и размеры частиц, инородные включения.
Рентген дает понятие об атомном строении материала, типе кристаллической структуры, дефектах решеток. Для исследования используется свойство рядов отражать гамма-лучи. При магнитном способе поверхность металла намагничивается и покрывается железным порошком. После размагничивания слой показывает очертания решетки.
Ультразвук применяется для эффективного обнаружения качественного преобразования металла в требуемую аллотропную модификацию. Волновое излучение распространяется внутрь и отражается от элементов решетки.
Примеры аллотропии
При нагревании металлов в процессе превращения поглощается тепло, при этом изменение решеточной конструкции происходит при одной и той же температуре. Аллотропным модификациям подвергаются многие металлы, например, титан, железо, олово и др. Железо при нагревании до +1390ºС характеризуется гранецентрированной решеткой. Повышение температуры до +1540ºС ведет к перестройке до центрировано-кубической структуры.
Аллотропные модификации металлов:
Определенные свойства твердых элементов зависят не только от строения решетки и дефектов, но и от структуры микрочастиц, их состава, размера и формы. Конструкция кристаллов оказывает влияние на физические характеристики тела и предопределяет пределы деформационной пластики, твердость материала.
Обратимые и непоправимые переходы
В случае изменения температурных показателей и параметров давления твердые материалы переходят из одной структуры в другую без перемены количественного состава элементов. Предпосылками является подвижность частиц решетки и перенос некоторого количества вещества, вызванный дефектами строения твердого состояния.
Примеры переходов:
Проводят разработанную методику трехфазной реакции для направленного получения требуемой решеточной структуры. Выбор нагревательного режима и продолжительность повышения температуры ускоряет рост кристаллов до больших зерен, что улучшает качество. Изменение способа обработки направляется иногда на снижение активности катализаторов в результате процесса рекристаллизации.
Энантиотропное видоизменение возникает при нулевой температуре и выбранном давлении. Иногда аллотропное преобразование относится к необратимым и одно из состояний материала является неустойчивым в термическом плане. Эта фаза сохраняется на всем температурном интервале от абсолютного нуля и называется монотропным. При получении серого олова из белого происходит обратимое преобразование, а превращение алмаза в графит становится необратимым.
Отличие этих типов превращений — в технологических особенностях проведения. Энантиотропные переходы модификации А чаще получаются методом постепенного охлаждения сплава. Сначала масса кристаллизуется в виде состояния Б, которое затем видоизменяется в устойчивую фазу к низким температурам.
При монотропном переходе в случае охлаждения сплава образуется только вещество в состоянии А. Требуется особый технологический режим со строгим дозированием понижения температуры и давления для получения модификации Б. Примером служит получение стабильного черного фосфора из белого путем нагревания до + 200ºС и повышения давления до 1,25 ГПа. После помещения полученного образца в нормальные условия обратного преобразования не происходит.
Что такое аллотропия и почему она важна
В таблице Менделеева более сотни элементов, которые могут связываться друг с другом. Однако даже соединения, состоящие из одного химического элемента могут быть разнообразны.
Каждый химический элемент в таблице Менделеева — это определенный вид атомов со своими уникальными свойствами. Однако в природе существует не так много веществ, которые состоят из скоплений атомов. Кислород, углекислый газ, вода и множество другие соединений представляют собой молекулы.
Атом кислорода и молекула кислорода сильно отличаются друг от друга по своим свойствам. Так или иначе, в природе атомы кислорода склонны объединяться и образовывать молекулы, потому что это энергетически более выгодно. Но один химический элемент может образовывать сразу несколько видов молекул. Например, если соединить два атома кислорода, можно получить молекулу O2, а если соединить три атома, то получится уже озон O3.
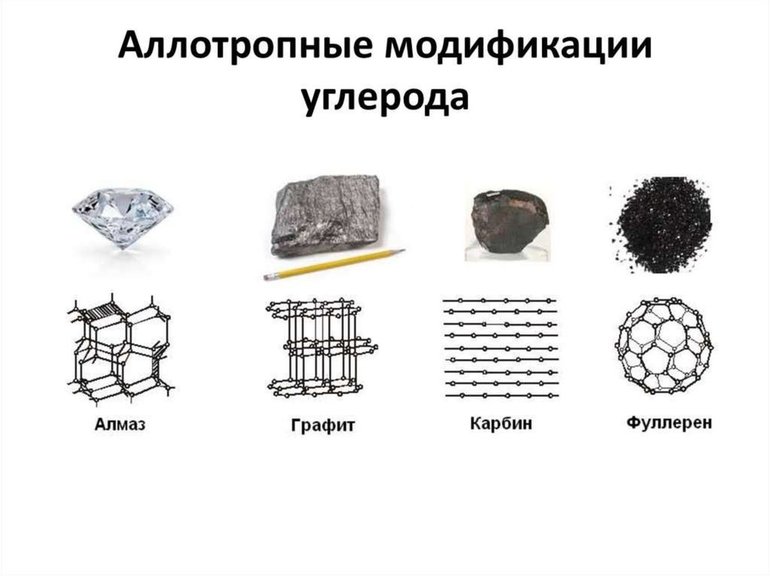
Явление образования множества химических веществ из одного химического элемента называется аллотропией, а эти вещества — аллотропными модификациями. Самый известный пример, иллюстрирующий это явление — углерод. Этот элемент может принимать форму не только «беспорядочного» угля и уложенного в слои графита, но и графена, нанотрубок и фуллеренов, похожих на футбольные мячи.
Аллотропия позволяет сильно увеличить количество доступных человеку соединений. Многие модификации углерода сегодня используются в исследованиях для создания сенсоров, средств адресной доставки лекарств, а также упрочнения существующих конструкционных материалов.
Аллотропия
Полезное
Смотреть что такое «Аллотропия» в других словарях:
аллотропия — аллотропия … Орфографический словарь-справочник
АЛЛОТРОПИЯ — (от греч. allos иной, и trepein обращать). Свойство некоторых химических веществ принимать различные формы, вместе с различными свойствами; напр., углерод, являющийся в виде алмаза, графита, угля. Словарь иностранных слов, вошедших в состав… … Словарь иностранных слов русского языка
АЛЛОТРОПИЯ — (от алло. и греч. tropos поворот свойство), существование химических элементов в виде двух или более простых веществ. Может быть обусловлена образованием молекул с различным числом атомов (напр., кислород O2 и озон O3) либо кристаллов различных … Большой Энциклопедический словарь
АЛЛОТРОПИЯ — АЛЛОТРОПИЯ, свойство некоторых химических элементов, позволяющее им существовать в двух или более различных физических формах. Каждая форма (называемая аллотропом) может иметь различные химические свойства, но способна превратиться и в другой… … Научно-технический энциклопедический словарь
АЛЛОТРОПИЯ — полиморфизм элементов (углерод, сера и др.). Геологический словарь: в 2 х томах. М.: Недра. Под редакцией К. Н. Паффенгольца и др.. 1978 … Геологическая энциклопедия
АЛЛОТРОПИЯ — (от греч. allos иной и tropos образ), свойство некоторых хим. элементов существовать в нескольких видоизменениях, различных по физ. и хим. свойствам. Причины А.: полимерия (см.) различное число атомов в молекуле (напр., у О, S, Р), различное… … Большая медицинская энциклопедия
аллотропия — Существование одного и того же химич. элемента в виде двух или нескольких простых вещ в, разных по строению и свойствам, т.н. аллотропич. модификаций. А. м. б. результатом образования разных кристаллич. форм (напр., фа фит и алмаз, a Fe и y Fe)… … Справочник технического переводчика
АЛЛОТРОПИЯ — свойство некоторых хим. элементов в свободном виде существовать в нескольких видоизменениях (модификациях), различных по строению кристаллической решетки, физ. и хим. свойствам, напр. углерод существует в виде угля, графита и алмаза … Большая политехническая энциклопедия
Аллотропия — Алмаз и графит аллотропические формы углерода, отличающиеся строением кристаллической решётки Аллотропия (от др. греч … Википедия
аллотропия — и; ж. [от греч. allos другой и tropos поворот, направление]. Существование одного и того же химического элемента в виде двух или нескольких простых веществ, различных по строению и свойствам. ◁ Аллотропический, ая, ое. Графит и алмаз являются… … Энциклопедический словарь
АЛЛОТРОПИЯ — существование химических элементов в двух или более молекулярных либо кристаллических формах. Например, аллотропами являются обычный кислород O2 и озон O3; в этом случае аллотропия обусловлена образованием молекул с разным числом атомов. Чаще… … Энциклопедия Кольера
Что такое аллотропия и почему она важна
Каждый химический элемент в таблице Менделеева — это определенный вид атомов со своими уникальными свойствами. Однако в природе существует не так много веществ, которые состоят из скоплений атомов. Кислород, углекислый газ, вода и множество другие соединений представляют собой молекулы.
Атом кислорода и молекула кислорода сильно отличаются друг от друга по своим свойствам. Так или иначе, в природе атомы кислорода склонны объединяться и образовывать молекулы, потому что это энергетически более выгодно. Но один химический элемент может образовывать сразу несколько видов молекул. Например, если соединить два атома кислорода, можно получить молекулу O2, а если соединить три атома, то получится уже озон O3.
Явление образования множества химических веществ из одного химического элемента называется аллотропией, а эти вещества — аллотропными модификациями. Самый известный пример, иллюстрирующий это явление — углерод. Этот элемент может принимать форму не только «беспорядочного» угля и уложенного в слои графита, но и графена, нанотрубок и фуллеренов, похожих на футбольные мячи.
Аллотропия позволяет сильно увеличить количество доступных человеку соединений. Многие модификации углерода сегодня используются в исследованиях для создания сенсоров, средств адресной доставки лекарств, а также упрочнения существующих конструкционных материалов.
Что такое аллотропия
Аллотропия – что это?
Явление аллотропии подразумевает возможность создания из одного и того же элемента определенного количества различных веществ. Например, кислород и озон в своем составе содержат только лишь оксиген. Вопрос о том, как это вообще возможно, на протяжении длительного периода времени интересовал многих людей. На сегодняшний момент ученые легко могут объяснить все особенности этого процесса.
Определение понятия
Под аллотропией подразумевается существование нескольких простых веществ, в основе которых присутствует один и тот же единственный химический элемент. Впервые такое явление описал известный шведский химик и минеролог Йенс Берцелиус.
Аллотропия по своей сути имеет довольно много общего с кристаллическим полиморфизмом. В связи с этим у ученых на протяжении длительного периода времена существовали достаточно серьезные споры. Это связанно с тем, что часть специалистов считали, что аллотропия и кристаллический полиморфизм – это одно и то же явление.
В настоящее же время от этой теории большинство ученых отошло. Мировое научное сообщество пришло к выводу о том, что кристаллический полиморфизм может касаться только лишь твердых тел, тогда как аллотропия – газов и жидкостей.
Причины возникновения аллотропии
Далеко не все элементы способны образовывать несколько разных простых веществ. Такая способность напрямую зависит от структуры молекул. Чаще всего подобное явление наблюдается у элементов, которые имеют переменные окислительные степени. Это касается таких групп, как:
Причины аллотропии могут быть нескольких типов. К наиболее вероятным из них ученые относят такие факторы, как:
Для того чтобы наглядно понять, каким образом может существовать явление аллотропии, необходимо рассмотреть несколько наиболее примечательных примеров, широко встречающихся в природе.
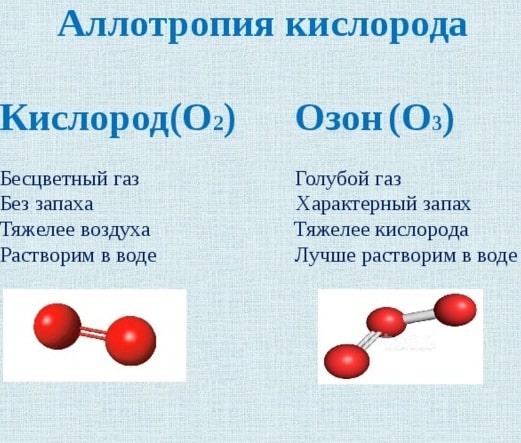
Кислород и озон
Аллотропия кислорода и озона – это вариант того, как различное количество атомов может существенно влиять не только на физические, но и на химические свойства простых веществ. Для того чтобы понять это, необходимо разобраться в особенностях каждого из этих газов:
Аллотропия оксигена была исследована из-за своего распространения одной из первых.
Алмаз и графит
Молекула углерода отличается тем, что она имеет постоянное количество атомов. При этом из последних могут образовываться самые разнообразные простые вещества. Это касается, к примеру, алмаза и графита. Их отличия заключаются в следующем:
Аллотропия алмаза и графита – один из примеров того, как из одного и того же химического элемента из-за разной кристаллической решетки образуются существенно отличающиеся друг от друга простые вещества.
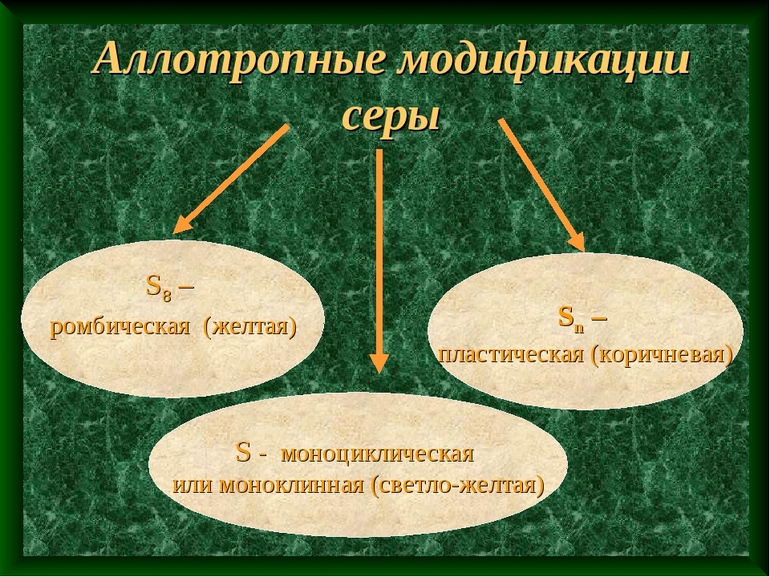
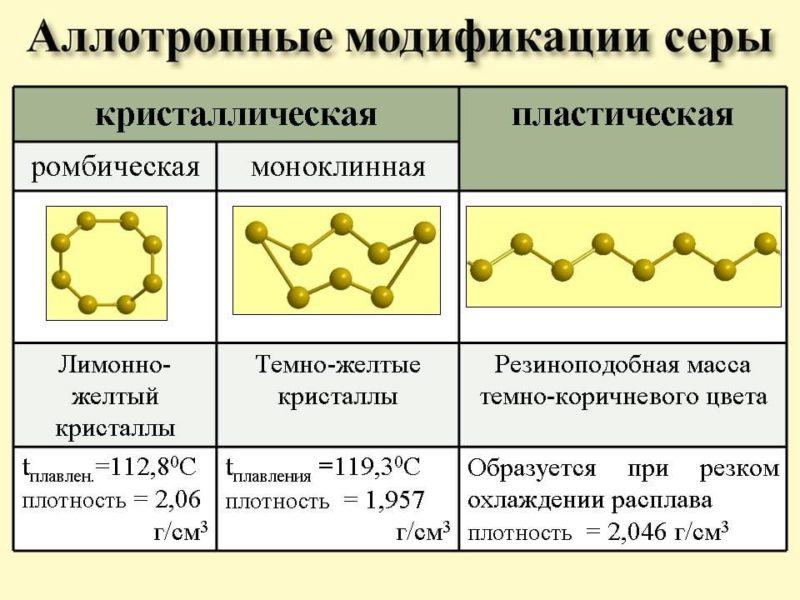
Внутренняя структура молекул серы может быть различной. Вследствие этого происходит образование различных простых веществ, среди которых стоит выделить такие:
Аллотропия серы – еще один пример влияния внутренней структуры молекул на создание разных по своим свойствам простых веществ.
Фосфор
На сегодняшний момент известно около 11 видов фосфора. Это обусловлено аллотропией, причина которой связана с кристаллической решеткой молекул этого химического элемента. Для того чтобы изменить внутреннее строение, необходимо создать определенные условия.
К примеру, белый фосфор может быть выделен посредством испарения мочи. Такое вещество будет очень активным, вследствие чего при повышении температурных показателей окружающей среды до 40 градусов по Цельсию оно воспламенится из-за реакции с кислородом.
Для получения красного фосфора достаточно всего лишь увеличить давление и температуру в атмосфере двуокиси углерода. Это вещество отличается средней активностью. Вследствие этого оно не светится в темноте. При нагревании красный фосфор преобразовывается в пар. Это можно наблюдать при зажигании спичек.
Аллотропия – это образование нескольких отличающихся друг от друга веществ из одного и того же химического элемента. Наблюдать такое явление можно преимущественно у неметаллов. Его основные причины заключаются, как в разном количестве атомов, что образовывают молекулу, так и в изменениях кристаллической решетки.