Аморфные тела
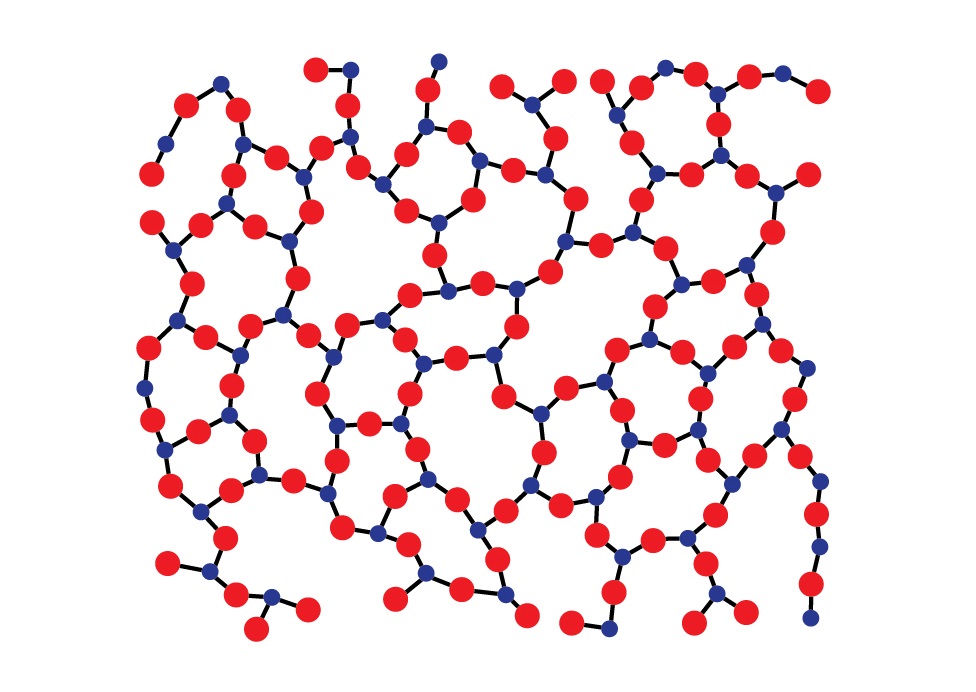
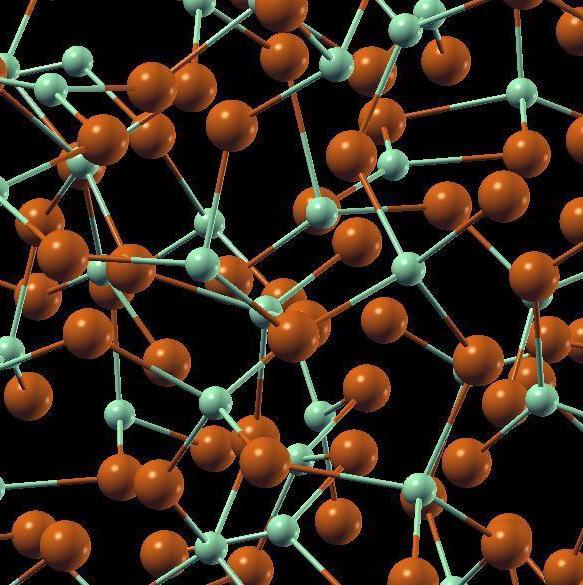
Аморфные тела (структура диоксида кремния)
Твердые тела разделяют на аморфные и кристаллические, в зависимости от их молекулярной структуры и физических свойств.
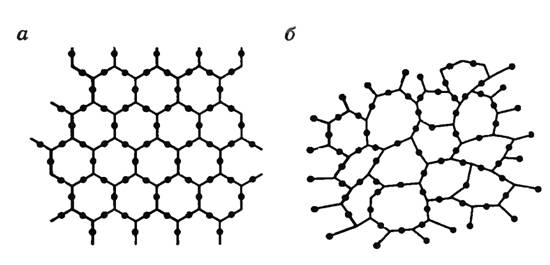
В отличие от кристаллов молекулы и атомы аморфных твердых тел не формируют решетку, а расстояние между ними колеблется в пределах некоторого интервала возможных расстояний. Иначе говоря, у кристаллов атомы или молекулы взаимно расположены таким образом, что формируемая структура может повторяться во всем объеме тела, что называется дальним порядком. В случае же с аморфными телами – сохраняется структура молекул лишь относительно каждой одной такой молекулы, наблюдается закономерность в распределении только соседних молекул – ближний порядок. Наглядный пример представлен ниже.
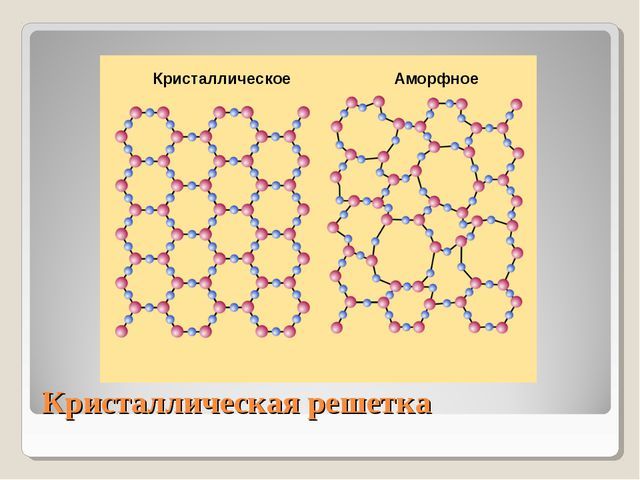
На рисунке слева (а) изображена решетка молекул кварца, а справа (б) расположение молекул кварцевого стекла, которое является аморфным телом.
К аморфным телам относится стекло и другие вещества в стеклообразном состоянии, канифоль, смолы, янтарь, сургуч, битум, воск, а также органические вещества: каучук, кожа, целлюлоза, полиэтилен и др.
Свойства аморфных тел
Особенность строения аморфных твердых тел придает им индивидуальные свойства:
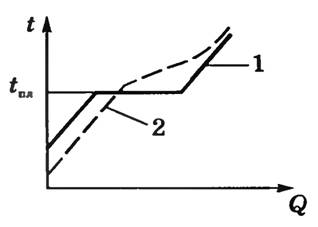
График перехода аморфного тела в жидкое состояние изображен пунктирной линией (2), а график перехода обычного твердого тела в жидкое состояние – сплошной (1).
Стеклообразное состояние
В природе существуют жидкости, которые практически невозможно перевести в кристаллическое состояние посредством охлаждения, так как сложность молекул этих веществ не позволяет им образовать регулярную кристаллическую решетку. К таким жидкостям относятся молекулы некоторых органических полимеров.
Материалы по теме
Жидкие кристаллы
Однако, при помощи глубокого и быстрого охлаждения, практически любое вещество способно перейти в стеклообразное состояние. Это такое аморфное состояние, которое не имеет явной кристаллической решетки, но может частично кристаллизироваться, в масштабах малых кластеров. Данное состояние вещества является метастабильным, то есть сохраняется при некоторых требуемых термодинамических условиях.
При помощи технологии охлаждения с определенной скоростью вещество не будет успевать кристаллизоваться, и преобразуется в стекло. То есть чем выше скорость охлаждения материала, тем меньше вероятность его кристаллизации. Так, например, для изготовления металлических стекол потребуется скорость охлаждения, равная 100 000 – 1 000 000 Кельвин в секунду.
В природе вещество существует в стеклообразном состоянии возникает из жидкой вулканической магмы, которая, взаимодействуя с холодной водой или воздухом, быстро охлаждается. В данном случае вещество зовется вулканическим стеклом. Также можно наблюдать стекло, образованная в результате плавления падающего метеорита, взаимодействующего с атмосферой – метеоритное стекло или молдавит.
Молдавит, естественное стекло, образованное ударом метеорита, из Беседин, Богемия, Чехия.
Аморфные тела
Амо́рфные вещества́ (тела́) (от др.-греч. ἀ «не-» и μορφή «вид, форма») — конденсированное состояние вещества, атомарная структура которых имеет ближний порядок и не имеет дальнего порядка, характерного для кристаллических структур. В отличие от кристаллов стабильно-аморфные вещества не затвердевают с образованием кристаллических граней, и, (если не были под сильнейшим анизотропным воздействием — сжатием или электрическим полем, например) обладают изотропией свойств, то есть не обнаруживают различных свойств в разных направлениях. И не имеют определённой точки плавления: при повышении температуры стабильно-аморфные вещества постепенно размягчаются и выше температуры стеклования (Tg) переходят в жидкое состояние. Вещества с высокой скоростью кристаллизации, обычно имеющие (поли-)кристаллических структуру, но сильно переохлаждённые при затвердевании в аморфное состояние, при последующем нагреве незадолго до плавления рекристаллизуются (в твёрдом состоянии с небольшим выделением тепла), а затем плавятся как обычные поликристаллические.
Получаются при высокой скорости затвердевания(остывания) жидкого расплава или конденсацией паров на охлаждённую заметно ниже температуры ПЛАВЛЕНИЯ(не кипения!) подложку(любой предмет). Соотношение реальной скорости охлаждения (dT/dt) и характеристической скорости кристаллизации определяет долю поликристаллов в аморфном объёме. Скорость кристаллизации — параметр вещества, слабо зависящий от давления и от температуры (около точки плавления — сильно). И сильно зависящий от сложности состава — для металлов порядка долей-десятков миллисекунд; а для стёкол при комнатной температуре — сотни и тысячи лет (старые стёкла и зеркала мутнеют).
Кварц (SiO2) также имеет низкую скорость кристаллизации, поэтому отлитые из него изделия получаются аморфными. Однако природный кварц, имевший сотни и тысячи лет для кристаллизации при остывании земной коры или глубинных слоев вулканов, имеет крупнокристаллическое строение, в отличие от вулканического стекла, застывшего на поверхности.
К стабильно-аморфным веществам принадлежат стекла (искусственные и вулканические), естественные и искусственные смолы, клеи, парафин, воск и др. Аморфные вещества могут находиться либо в стеклообразном состоянии (при низких температурах), либо в состоянии расплава (при высоких температурах). Аморфные вещества переходят в стеклообразное состояние при температурах заметно ниже температуры стеклования Tg. При температурах намного выше Tg аморфные вещества ведут себя как расплавы, то есть находятся в расплавленном состоянии(если не разлагаются от перегрева и не сгорают, конечно). Вязкость аморфных материалов — непрерывная функция температуры: чем выше температура, тем ниже вязкость аморфного вещества.
Структура
Исследования показали, что структуры жидкостей и аморфных тел имеют много общего. В аморфных и жидких телах наблюдается ближний порядок в упаковке частиц (атомов или молекул). По этой причине принято считать аморфные тела очень густыми/вязкими (застывшими) жидкостями.
Также бывают промежуточные полуаморфные (полукристаллические) состояния.
Свойства
Все физические свойства аморфного и поликристаллического состояний одного и того же вещества заметно (иногда сильно) отличаются (кроме плотности).
Электрические и механические свойства аморфных веществ ближе к таковым для монокристаллов, чем для поликристаллов из-за отсутствия резких и сильно загрязнённых примесями межкристаллических переходов(границ) с зачастую абсолютно другим химическим составом.
Немеханические свойства полуаморфных состояний обычно являются промежуточными между аморфным и кристаллическим и изотропны. Однако отсутствие резких межкристаллических переходов заметно влияет на электрические и механические свойства, делая их похожими на аморфные.
При внешних воздействиях аморфные вещества обнаруживают одновременно упругие свойства, подобно кристаллическим твердым веществам, и текучесть, подобно жидкости. Так, при кратковременных воздействиях (ударах) они ведут себя как твёрдые вещества и при сильном ударе раскалываются на куски. Но при очень продолжительном воздействии (например растяжении) аморфные вещества текут. Например, аморфным веществом также является смола (или гудрон, битум). Если раздробить её на мелкие части и получившейся массой заполнить сосуд, то через некоторое время смола сольётся в единое целое и примет форму сосуда.
В зависимости от электрических свойств, разделяют аморфные металлы, аморфные неметаллы, и аморфные полупроводники.
Аморфные тела

Всего получено оценок: 238.
Всего получено оценок: 238.
Твердые тела существуют в двух основных состояниях, отличающихся своим внутренним строением, что приводит различию их физических свойств. Это — кристаллическое и аморфное состояния твердых тел. Основным признаком кристаллов является строгий, повторяющийся порядок расположения атомов. Аморфные вещества (от греческого слова “аморфос” — бесформенный) не имеют упорядоченной, кристаллической структуры.
Структура аморфных тел
В телах, находящихся в аморфном состоянии, отсутствует четкий порядок расположения атомов. Существует только, так называемый ближний порядок, когда ближайшие атомы располагаются относительно упорядоченно. По своей структуре аморфные вещества похожи на жидкости.
Аморфное состояние вещества, в отличие от кристаллического, не является устойчивым. По прошествии некоторого времени аморфное вещество постепенно переходит в кристаллическое. Правда, это время измеряется годами и десятилетиями.
В аморфном состоянии могут находиться и такие вещества, которые обычно имеют кристаллическую структуру. Например, кристалл кварца SiO2 если его расплавить (при температуре 1700 0 С), при охлаждении образует плавленый кварц, имеющий меньшую плотность, чем кристаллический, и обладающий свойствами одинаковыми по всем направлениям, притом сильно отличающимися от свойств кристаллического кварца.
Примеры аморфных тел
Аморфными являются огромное количество веществ. Вот только некоторые, хорошо известные вещества: парафин, воск, сургуч, эбонит, шоколад, канифоль, смола, стекло, плексиглас, каучук, стекло, различные пластмассы.

Свойства аморфных тел
В силу своего строения, в отличие от кристаллических тел, аморфные тела обладают следующими основными свойствами:
Рис. 3. Графики перехода аморфного и кристаллического тел в жидкое состояние.
Есть вещества, обладающие одновременно свойствами и жидкости и кристалла, а именно текучестью и анизотропией. Такое состояние вещества называется жидкокристаллическим. В основном жидкими кристаллами являются органические вещества, молекулы которых имеют форму плоских пластин или нитевидную форму. Эти вещества являются основой для жидкокристаллических экранов телевизоров.
Что мы узнали?
Итак, мы узнали, что из себя представляют твердые тела в аморфном состоянии. Структура этих веществ не имеет упорядоченного порядка размещения атомов. Физические свойства аморфных тел не зависят от направления воздействия и ориентации тела.
Аморфные тела
В предыдущем параграфе мы узнали, что некоторые твёрдые тела (например, соль, кварц, металлы и другие) являются моно- или поликристаллами. Познакомимся теперь с аморфными телами. Они занимают промежуточное положение между кристаллами и жидкостями, поэтому их нельзя однозначно назвать твёрдыми.
Проделаем опыт. Нам понадобятся: кусок пластилина, стеариновая свеча и электрический обогреватель. Поставим пластилин и свечу на равных расстояниях от обогревателя. Вскоре часть свечи расплавится, часть останется в виде твёрдого тела, а пластилин «обмякнет». Некоторое время спустя весь стеарин расплавится, а пластилин постепенно «расплывётся», став совсем мягким.
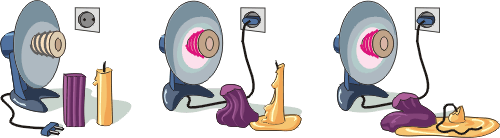 |
Подобно стеарину, существуют и другие кристаллические вещества, которые при нагревании не размягчаются, и во время плавления всегда можно видеть как жидкость, так и ещё не расплавившуюся часть тела. Это, например, все металлы. Но существуют и аморфные вещества, которые при нагревании постепенно размягчаются, становятся всё более текучими, поэтому невозможно указать температуру, при которой тело превращается в жидкость (плавится).
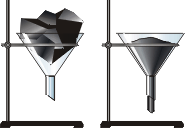 |
Аморфные тела при любой температуре обладают текучестью. Подтвердим это опытом. В стеклянную воронку бросим кусок аморфного вещества и оставим в тёплой комнате (на рисунке – смола гудрон; из неё делают асфальт). Через несколько недель окажется, что смола приняла форму воронки и даже начала вытекать из неё наподобие «струи». То есть аморфное тело ведёт себя как очень густая и вязкая жидкость.
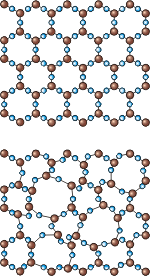 |
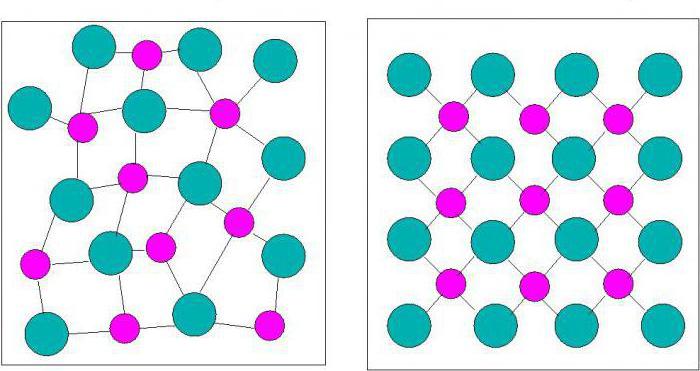
Строение аморфных тел. Исследования электронным микроскопом и рентгеновскими лучами показывают, что в аморфных телах не наблюдается строгого порядка в расположении их частиц. В отличие от кристаллов, где существует дальний порядок в расположении частиц, в строении аморфных тел наблюдается только ближний порядок – некая упорядоченность расположения частиц сохраняется лишь вблизи каждой отдельной частицы (см. рисунок). Сверху изображено расположение частиц в кристаллическом кварце, снизу – в аморфной форме кварца. Эти вещества состоят из одних и тех же частиц – молекул оксида кремния SiO2.
Как и частицы любых тел, частицы аморфных тел непрерывно и беспорядочно колеблются и чаще, чем частицы кристаллов, могут перескакивать с места на место. Этому способствует то, что частицы аморфных тел расположены неодинаково плотно, местами создавая сравнительно большие промежутки. Однако это не то же самое, что «вакансии» в кристаллах (см. § 7-е).
Кристаллизация аморфных тел. С течением времени (недели, месяцы) аморфные вещества самопроизвольно переходят в кристаллическое состояние. Например, сахарные леденцы или мёд, оставленные в покое на несколько месяцев, становятся непрозрачными. В этом случае говорят, что мёд и леденцы «засахарились». Разломив такой леденец или зачерпнув такой мёд ложкой, мы увидим образовавшиеся кристаллики сахара, прежде существовавшего в аморфном состоянии.
Самопроизвольная кристаллизация аморфных тел свидетельствует, что кристаллическое состояние вещества более устойчиво, чем аморфное. МКТ объясняет это так. Силы притяжения и отталкивания «соседок» перемещают частицы аморфного тела в такие положения, где потенциальная энергия минимальна (см. § 7-г). При этом возникает более упорядоченное расположение частиц, что и означает, что происходит самостоятельная кристаллизация.
Аморфные тела: характеристика, описание и свойства
Нужно помнить, что не все тела, которые существуют на планете Земля, имеют кристаллическое строение. Исключения из правила получили название «аморфные тела». Чем же они отличаются? Исходя из перевода данного термина – аморфный – можно предположить о том, что такие вещества отличаются от других своей формой или видом. Речь идет об отсутствии так называемой кристаллической решетки. Процесс расщепления, при котором появляются грани, не происходит. Аморфные тела также отличаются тем, что не зависят от окружающей среды, и их свойства постоянны. Такие вещества называются изотропными.
Небольшая характеристика аморфных тел
Из школьного курса физики можно вспомнить то, что аморфные вещества имеют такое строение, при котором атомы в них расположены в хаотичном порядке. Определенное место могут иметь лишь структуры-соседи, где такое расположение является вынужденным. Но все же проводя аналогию с кристаллами, аморфные тела не обладают строгой упорядоченностью молекул и атомов (в физике такое свойство получило название «дальний порядок»). В результате исследований было выяснено, что по своей структуре данные вещества схожи с жидкостями.
Некоторые тела (в качестве примера можно взять диоксид кремния, чья формула SiO2) могут одновременно находиться в аморфном состоянии и иметь кристаллическую структуру. Кварц в первом варианте обладает структурой неправильной решетки, во втором – правильного шестиугольника.
Свойство №1
Как уже говорилось выше, аморфные тела не обладают кристаллической решеткой. Их атомы и молекулы имеют ближний порядок размещения, что и будет первым отличительным свойством данных веществ.
Свойство №2
Текучестью данные тела обделены. Для того чтобы лучше объяснить второе свойство веществ, можно сделать это на примере воска. Ни для кого не секрет, что если налить воду в воронку, то она просто выльется из нее. То же самое будет и с любыми другими текучими веществами. А свойства аморфных тел не позволяют им проделывать такие «трюки». Если воск поместить в воронку, то он предварительно растечется по поверхности и лишь потом начнет стекать с нее. Это связано с тем, что молекулы в веществе перескакивают из одного положения равновесия в абсолютно другое, не имея основного местоположения.
Свойство №3
Пора поговорить о процессе плавления. Следует запомнить тот факт, что аморфные вещества не имеют определенной температуры, при которой начинается плавление. Во время поднятия градуса тело постепенно становится мягче и затем превращается в жидкость. Физики всегда делают упор не на температуре, при которой данный процесс начал происходить, а на соответствующем температурном интервале плавления.
Свойство №4
О нем уже было сказано выше. Аморфные тела изотропны. То есть их свойства в любом направлении неизменны, даже если условия пребывания в местах различны.
Свойство №5
Хоть раз каждый человек наблюдал, что с течением определенного промежутка времени стекла начинали мутнеть. Это свойство аморфных тел связно с повышенной внутренней энергией (она в разы больше, чем у кристаллов). Из-за этого данные вещества спокойно сами могут перейти в кристаллическое состояние.
Переход к кристаллическому состоянию
Спустя определенный промежуток времени любое аморфное тело переходит в кристаллическое состояние. Это можно наблюдать в привычной жизни человека. Например, если оставить леденец или мед на несколько месяцев, то можно заметить, что они оба потеряли свою прозрачность. Обычный человек скажет, что они просто засахарились. И правда, если разломать тело, то можно заметить наличие кристаллов сахара.
Итак, говоря об этом, необходимо уточнить, что самопроизвольное превращение в другое состояние связано с тем, что аморфные вещества неустойчивы. Сравнивая их с кристаллами, можно понять, что последние в разы «мощнее». Объяснить факт можно благодаря межмолекулярной теории. Согласно ей, молекулы постоянно перескакивают с одного места на другое, тем самым заполняя пустоты. Со временем образуется устойчивая кристаллическая решетка.
Плавление аморфных тел
Процессом плавления аморфных тел называется момент, когда с поднятием температуры все связи между атомами рушатся. Именно тогда вещество превращается в жидкость. Если условия плавления таковы, что давление одинаково на протяжении всего периода, то температура также должна быть фиксированной.
Жидкие кристаллы
В природе существуют тела, которые имеют жидкокристаллическую структуру. Как правило, они входят в перечень органических веществ, а их молекулы обладают нитевидной формой. Тела, о которых идет речь, обладают свойствами жидкостей и кристаллов, а именно текучестью и анизотропией.
В таких веществах молекулы располагаются параллельно друг другу, однако, между ними нефиксируемое расстояние. Они движутся постоянно, но ориентацию менять несклонны, поэтому постоянно находятся в одном положении.
Аморфные металлы
Аморфные металлы больше известны обычному человеку под названием металлические стекла.
Еще в 1940 году ученые заговорили о существовании данных тел. Уже тогда стало известно, что специально полученные вакуумным напылением металлы, не имели кристаллических решеток. И лишь через 20 лет было произведено первое стекло такого типа. Особого внимания у ученых оно не вызвало; и только спустя еще 10 лет о нем заговорили американские и японские профессионалы, а потом уже корейские и европейские.
Аморфные металлы отличаются вязкостью, достаточно высоким уровнем прочности и стойкостью к коррозии.