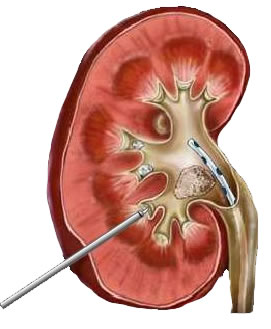
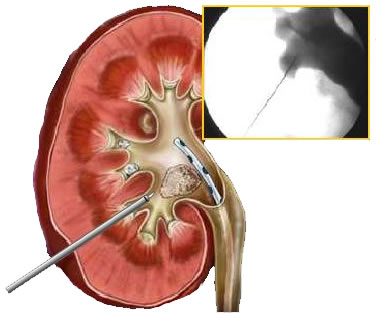
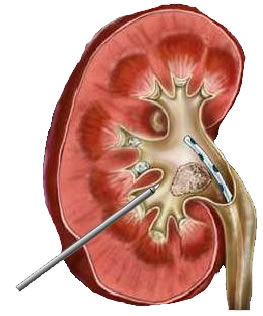
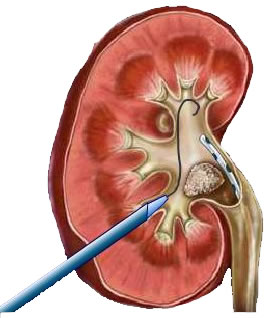
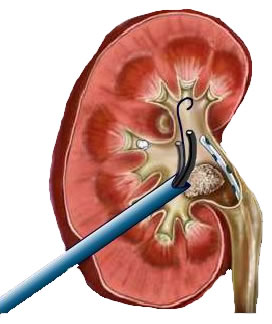
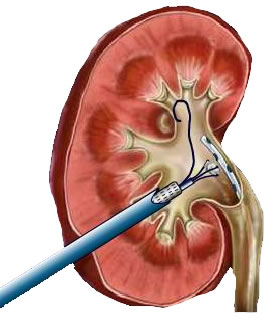
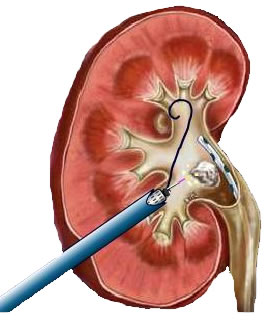
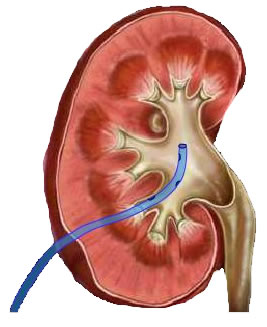
Амплац оболочка для перкутанного доступа
Амплац-оболочка для перкутанной хирургии. Диаметр оболочки 30 Ch/Fr. Длина 17 или 19 см.
Амплац-оболочка 30 Ch/Fr для перкутанного доступа. Используется для создания рабочего хода при операциях на почке. По амплац-оболочке в почечную лоханку заводятся инструменты, литоэкстракторы, лазерные волокна.
Изготовлена из медицинского пластика.
Поставляется в стерильном виде.
| Артикул | Наименование | Количество |
| RF3017 | Амплац-оболочка 30 Ch/Fr, длина 17 см | 1 |
| RF3019 | Амплац-оболочка 30 Ch/Fr, длина 19 см | 1 |
Для физических лиц
Оплата выставленного счета в офисах банка или через банковское мобильное приложение на расчетный счет ООО «Уромед М». Мы не принимаем к оплате наличные денежные средства и банковские карты! Обращаем Ваше внимание, что срок зачисления денежных средств на расчетный срок может занимать 1-3 дня.
Для юридических лиц
Оплата Товара производится путем перечисления денежных средств на расчетный счет ООО «Уромед М» в соответствии с выставленным счетом. Оплата счета означает согласие Покупателя с условиями и сроками поставки Товара, указанными в коммерческом предложении. Товар отпускается по факту прихода денежных средств на расчетный счет Поставщика.
Отгрузка и доставка Товара в соответствии с выставленным счетом осуществляется после поступления денежных средств на расчетный счет ООО «Уромед М».
Подробнее информация на странице Доставка и оплата
Размышления о бездренажной (tubeless) чрескожной нефролитотрипсии
 | Николай Александрович Григорьев Д.м.н., профессор кафедры урологии Первый МГМУ им. И.М. Сеченова Минздравсоцразвития России grigoriev.nikolay@gmail.com |
Чрескожная нефролитотрипсия сегодня является хорошо известной методикой лечения крупных и коралловидных камней почек. Она существует уже около 40 лет и прекрасно зарекомендовала себя, как эффективный и малоинвазивный метод оперативного лечения мочекаменной болезни. Известно, что традиционная чрескожная нефролитотрипсия завершается дренированием чашечно-лоханочной системы оперированной почки нефростомической трубкой. Вместе с тем мы знаем, что существуют бездренажные варианты этой операции, которые в нашей стране не имеют должного распространения. Попробуем это обсудить.
В зарубежной литературе можно найти довольно много работ, касающихся бездренажной чрескожной нефролитотрипсии. Ряд из них включает достаточно большое количество наблюдений успешных операций. В 2010 г проведен анализ наиболее значимых исследований по без- нефростомной чрескожной нефролитотрипсии (tubeless) за последнее 10-летие и было доказано, что это эффективная и безопасная операция.
Здесь следует сделать очень важную оговорку. Все вышеописанные рассуждения касаются неосложненной чрескожной нефролитотрипсии, доступ для которой выполнен правильно, т. е. через чашечку, и при этом во время операции нет кровотечения. Любое интраоперационное осложнение исключает возможность безнефростомного завершения операции, так же как и выраженные ретенционные изменения чашечно-лоханочной системы и явная опасность развития острого пиелонефрита.
Безнефростомное завершение операции никогда не должно быть самоцелью. Хирург всегда должен поступать осознанно. И конечно нельзя не отметить, что практиковать безнефростомную чрескожную нефролитотрипсию может только опытный эндоуролог. В результате исследований D. Allen et al. (2005) и O. Tanriverdy et al. (2007) было показано, что для освоения чрескожной нефролитотрипсии необходимо выполнить не менее 60 операций, а очень хорошие навыки приобретаются после выполнения 115 вмешательств. Только такой опыт может позволить правильно оценить клиническую и интраоперационную ситуацию, что необходимо при выборе наиболее безопасного и наименее дискомфортного для больного метода дренирования верхних мочевых путей после чрескожной нефролитотрипсии.
В большинстве наблюдений решение вопроса о безнефростомном завершении операции принимается после того, как извлекаются основные инструменты (амплац-трубка или сам тубус нефроскопа) из нефростомического хода. Если кровотечение отсутствует или оно минимально, то антеградно устанавливается катетер-стент и операция завершается. Но так бывает чрезвычайно редко и, как правило, после повторных вмешательств, когда нефростомический ход уже был сформирован. В подавляющем большинстве наблюдений после удаления инструментов возникает кровотечение и часто весьма обильное, ведь почка кровоснабжается очень интенсивно. Видя активное кровотечение, хирург скорее предпочтет нефростомию, чем откажется от нее. Этим можно объяснить то, что безнефростомное завершение операции даже в крупных лечебных центрах едва ли достигает 10 % от общего количества нефролитотрипсий.
В урологической клинике Первого МГМУ им. И.М. Сеченова на сегодняшний день выполнено 24 безнефростомных чрескожных нефролитотрипсии. Следует отметить, что половина этих операций проведена в течение только последнего года, и мы предполагаем, что их количество будет расти. Связано это, как ни странно, с внедрением необычного, транслюмбального способа удаления стента после безнефростомной чрескожной нефролитотрипсии. В 2007 г. в журнале «Эндоурология» (J Endourology) группой урологов из Лос-Анджелеса во главе с доктором А Shpall был описан этот способ удаления стента путем его вытягивания по ходу бывшего нефростомического свища за лигатуру, фиксированную во время нефролитотрипсии к проксимальному концу стента. Авторы идеи удаляли таким образом стенты без каких-либо осложнений в сроки от 3 до 12 дней после операции. Мы применили эту методику у 18 из 24 пациентов, кому осуществлена безнефростомная нефролитотрипсия. Она заслуживает подробного описания.
Очень важно то, что методика транслюмбального удаления стента позволяет смело прибегать к безнефростомному завершению операции и при этом не подвергать опасности здоровье пациента. Это обеспечивает фиксированная к стенту лигатура, которая постоянно поддерживает надежную связь с чашечно-лоханочной системой. В любой момент, в случае необходимости, может быть установлена нефростома. Пока мы не сталкивались с такой ситуацией ни в одном из 18 наших наблюдений, но потенциальная возможность легкого доступа в чашечнолоханочную систему при этой методике делает ее для нас методом выбора при безнефростомном завершении операции.
Во всех наших наблюдениях при этой методике стенты были удалены в сроки от 3 до 6 дней после операции. Никаких осложнений, связанных с безнефростомным завершением операции и такой методикой удаления стента, не отмечено. Сам процесс удаления стента практически безболезненный, занимает несколько секунд и не требует специального помещения и расходов в отличие от традиционной методики удаления стента из мочевого пузыря. Кроме того, и это очень важно именно сегодня, при транслюмбальной методике удаления стента нет угрозы инфицирования.
В 2 наблюдениях потребовалось рестентирова- ние верхних мочевых путей. В одном из них это было связано с необходимостью предотвращения развития острого пиелонефрита вследствие появления дилатации чашечно-лоханочной системы, что обусловлено окклюзией мочеточника сгустком из-за слишком раннего удаления стента (на 5-е сутки). Через 2 недели пациентка была здорова, стент удален.
В другом наблюдении, у пациентки, оперированной по поводу камня лоханки верхней половины удвоенной почки, рестентирование потребовалось из-за возникновения затека мочи из раны почки после удаления стента на 6-е сутки. Через 2 месяца пациентка была здорова без следов мочевого затека, стент удален.
Безнефростомная чрескожная нефролитотрипсия безусловно заслуживает внимательного к себе отношения. Требуется больший опыт применения этой методики для того, чтобы точнее представлять все ее нюансы, определять необходимые для каждого пациента сроки удаления стента и т. д. Мы верим в то, что скоро количество безнефростомных нефролитотрипсий в нашей практике достигнет такого уровня, когда мы сможем сделать все необходимые аргументированные заключения на основе доказательной медицины.
Буду рад дискуссии и любому сотрудничеству.
УРОЛОГИЯ В ОМСКЕ
ТЕЛЕФОН «ГОРЯЧЕЙ ЛИНИИ» +79095377482
ОПЕРАТИВНАЯ И КОНСЕРВАТИВНАЯ ПОМОЩЬ НА БЕРЕЗОВОЙ
Основные моменты операции дробления камня в почке. Продолжение.
Уретеропиелография.
Этот этап необходим для пункции полостной системы почки через нижнюю группу чашечек и заключается в введении контрастного вещества в мочеточниковый катетер. Выполняется катетеризация почки при помощи катетеризационного цистоскопа. Ретроградная уретеропиелография проводится с использованием круглого типа катетера.
Ориентиры:
Локализация камней и особенности анатомии чашечно-лоханочной системы могут быть изучены с использованием экскреторной урографии.
Пункция полостной системы почки под УЗ-контролем:
Под ультразвуковым контролем производится пункция нижней чашечки почки. После удаления внутренней части (стилета) пункционной иглы, в полостную систему вводится смесь рентгеноконтрастного вещества и физиологического раствора. Многие западные хирурги добавляют в раствор метиленовую синь. Локализация пункционной иглы четко видна при помощи рентгеноскопии.
Проведение иглы в полостную систему почки под рентгеновским контролем:
Следующие рентгенологические признаки позволяют судить о локализации иглы в чашечно-лоханочной системе почки. Их можно использовать при сложностях пункции почки под УЗ-контролем. Но, как правило, пункция полостной системы почки производится лишь с использованием ультразвукового аппарата. Рентгеноскопия используется лишь для контроля локализации иглы и контрастирования чашечно-лоханочной системы почки. В мочеточниковый катетер вводится раствор метиленовой сини, рентгеноконтрастного вещества и физиологического раствора.
Рентгенологические признаки:
— Смещение почки, когда игла касается её капсулы.
— Деформация чашечки, когда игла касается стенки нижней чашечки почки.
— Деформация стенок чашечки при смещении иглы.
Стилет иглы удаляется. Выделение метиленовой сини говорит о локализации иглы в полостной системе почки.
Создание пункционного хода.
Этот этап может осуществляться при помощи следующих инструментов:
— Металлические телескопические дилятаторы.
— Пластиковые дилятаторы.
— Баллонный дилятатор.
— Телескопические металлические дилятаторы. Эта техника наиболее эффективна. Рекомендуем пользоваться металлическими телескопическими дилятаторами при чрезкожной нефролитолапаксии. Проведение дилятаторов проводится под рентгеновским контролем. Каждый последующий дилятатор больше по диаметру, проводится в полостную систему почки вращательными движениями.
— Пластиковые дилятаторы. При этом варианте дилятации производится последовательная смена дилятаторов на большие по диаметру.
— Баллонные дилятаторы.
Последним вводится полый тефлоновый кожух « Amplatz » диаметром 28 по Шарьеру. По « Amplatz » трубке вводится нефроскоп и производится осмотр лоханки. Обнаружение камня возможно лишь в условиях непрерывной перфузии жидкости. Для ирригации примеяется физиологический раствор и(или) раствор фурацилина (1 : 50000). Во время нефроскопии, при необходимости, можно воспользоваться ренген-телевизионным экраном, для уточнения локализации конкремента и расположение нефроскопа по отношению к нему.
Визуализация камней почки:
На первом этапе производится аспирация или удаление сгустков крови через нефроскоп. Обычно конкремент виден сразу после удаления сгустков крови. В том случае, если конкремент не виден, необходимо воспользоваться рентгеноскопией. Иногда применяется гибкий эндоскоп.
Фрагментация конкрементов:
Нефростомический дренаж:
Среди осложнений, возникающих при нефролитолапаксии, встречаются: перфорация лоханки, потеря доступа в почку, кровотечение, возникновение урогематомы.
Аккуратное манипулирование инструментами, отказ от форсированных движений, выполнение контактной литотрипсии только «на глаз» без соприкосновения зонда литотриптора со стенкой лоханки, а так же надежное дренирование почки и достаточный опыт хирурга, – основные пути профилактики и ликвидации подобных осложнений.
Главное меню
Главное меню
Лазерная трипсия: контролируемый разлом мочевых камней DOI: Doi 10.29188/2222-8543-2018-9-1-36-39
Эндоскопическая хирургия мочекаменной болезни практически вытеснила ранее применяемые открытые оперативные вмешательства [1]. Однако десятилетие ее применения выявили недостатки, одним из которых является осложнение контактной лазерной литотрипсии – развитие инфекционно-воспалительного процесса в почках из-за бактериальной диссеминации флоры из биопленок камней [2]. Кроме того, мелкие осколки камней и остатки биопленок после перкутанных вмешательств служат основой для рецидива камнеобразования в почках [3]. Даже при стерильной моче микроорганизмы в камне обнаруживаются по данным разных авторов в 25-41% случаев [4,5].
Лазеры на иттриево-алюминиевом гранате, активированном ионами Ho3+ (Ho:YAG) с ламповой накачкой, уже более 20 лет применяются для литотрипсии [6,7]. В основе механизма разрушения камня импульсами свободной генерации этих лазеров лежит взрывная вапоризация камня [6]. Это приводит к бесконтрольному разлому камня на мелкие фрагменты с последующей диссеминацией бактерий по полостной системе почки, что обуславливает развитие в послеоперационном периоде синдрома системной воспалительной реакции и сепсиса почти у 30% пациентов [8,9].
Один из путей профилактики послеоперационных инфекционновоспалительных осложнений – новые подходы к антибактериальной профилактике, разработка адекватных режимов ее проведения [10]. Другой путь – поиск новых методик дробления камней, предполагающих контролируемую крупнооскольчатую их фрагментацию. С учетом неуклонного роста антибиотикорезистентности уропатогенной флоры, второй путь, на наш взгляд, является перспективным и целесообразным. Для реализации этого метода необходимо использовать импульсы меньшей энергии (чем в Ho:YAG лазере с ламповой накачкой), которые не могут привести к разрыву камня на мелкие фрагменты, но способны за счет высокой частоты повторения обеспечить послойную абляцию и разрез камня.
Настоящая работа направлена на исследование нового варианта лазерного воздействия на почечные камни, который подразумевает использование импульсно-периодического режима лазерной генерации с малой импульсной энергией (единицы – десятки мДж), но высокий частотой повторения импульсов (от сотен герц до десятков килогерц). Такой режим лазерного воздействия может позволить обеспечить аккуратный разрез камней на несколько крупных фрагментов, которые затем могут быть извлечены из почки механически через кожух – амплац, что позволит не толькоминимизировать возможное инфицирование мочевой системы, но и предотвратить потерю мелкихфрагментов камня, которые являются источником резидуального камнеобразования.
Цель – поиск режима лазерной литотрипсии, который обеспечит эффективную фрагментацию почечных конкрементов, исключая их неконтролируемый мелкооскольчатый разлом.
МАТЕРИАЛЫ И МЕТОДЫ
В исследование включали камни от пациентов с калькулезным пиелонефритом и наличием лейкоцитурии. Изучен эффект лазерного дробления 25 камней еx vivo. Выполнено дробление камней после нефролитоэкстракций и пиелолитотомий, нефрэктомий. В эксперименте исследовали лишь целиком удаленные камни, которые до момента дробления помещали в физиологический раствор. Для перфорации камня насквозь в первой серии экспериментов использован лазер на кристалле Ho:YAG с накачкой излучением тулиевого волоконного лазера. Ho:YAG лазер генерировал на длине волны 2098 нм импульсы (длительностью 20-40 нс) с частой повторения, варьируемой от 5 до 40 кГц, при среднеймощности до 35 Вт (энергия в импульсах варьировалась в пределах 0,5-3,0 мДж) [11].
Во второй серии экспериментов использовался лазер на керамике Tm:Lu2O3 с накачкой излучением эрбиевого волоконного лазера с рамановским сдвигом длины волны (на 1670 нм). Этот лазер на керамике генерировал в импульсно-периодическом режиме (импульсы длительностью 30-40 нс с частотой повторения, варьируемой в пределах 1425 кГц), излучение на длине волны 1967 нм (средняя мощность излучения изменялась от 100 мВт до 10 Вт) [12]. Оба используемых лазера были созданы в ИПФ РАН (Н. Новгород) и имели выходные пучки высокого качества (с расходимостью, близкой к дифракционному пределу).
Рентгеновскую микроструктурную плотность камней еx vivo измерялиметодомкомпьютерной томографии в единицах Хойнсфилда (ед. HU). Для применяемых режимов экспериментов с разными длинами волн камни отбирали методом случайной выборки.
Методика эксперимента: Камни извлекали из физиологического раствора, помещали на оптический столик. Излучение лазера фокусировали на камень линзой с (эффективным) фокусным расстоянием, варьируемым от 21 мм до 200 мм (оценочный диаметр лазерного пучка на камне составлял от 0,1 до 1ммпо уровню интенсивности e-2 )(рисунок 1а). Измерялось время перфорации камня насквозь (до прохождения лазерного излучения через камень). Контроль полученного канала камня осуществляли визуально и при микроскопии в проходящем свете (микроскоп Leica DMLS, объектив х10, окуляр х10).
Рис.1. Воздействие лазерным лучом на камни: А, Б перфорация; В, Д линейный разлом (указан стрелкой), Г, Е фрагменты камней
РЕЗУЛЬТАТЫ
Диаметр целиком удаленных камней, в которых выполняли перфорации лазером, колебался от 8 до 20 мм. Микроструктурная плотность изученных камней в представленном эксперименте составила от 127 до 1933 ед. HU. Время перфорации камня насквозь составило от 2 до 300 секунд и зависело от его плотности, размера по длине и химического состава. Результаты лазерного воздействия и микроструктурная плотность конкрементов представлены в таблице 1. Положительный эффект дробления с контролируемым разломом, согласно полученным в эксперименте результатам, при длине волны 2097 нм, частоте повторения 10 и 30 кГц, энергии импульса от 0,17 до 2,3 мДж получен в 8 случаях из 9 (табл. 1). Микроструктурная плотность этих камней составила от 161 ед. HU до 1566 ед. HU.
Таблица 1. Параметры и результаты лазерного воздействия на камни почек еx vivo
| Параметры | Режим воздействия | ||||||||
|---|---|---|---|---|---|---|---|---|---|
| Длина волны | |||||||||
| 2097 | 1967 | ||||||||
| Частота повторения (кГц); | 30 | 10 | 1 | 0,2 | 15 | 15 | |||
| Линза с эффективным фокусным расстоянием (F) мм | 21 | 21 | 21 | 21 | 21 | 150 | 21 | 200 | 150 |
| Энергия импульса (мДж), | 0,17 | 0,18 | 0,1 | 1,0 | 2,3 | 0,45-0,55 | 40-50 | 0,45-0,55 | 0,45-0,55 |
| Количество конкрементов (n) | n-3 | n-1 | n-1 | n-1 | n-3 | n-1 | n-8 | n-1 | n-6 |
| HU | 127-477 | 1004 | 1566 | 245 | 169-546 | 1305 | 311-1498 | 1305 | 1305 |
| Размер камня по длине (мм) | 4-10 | 20 | 17 | 12 | 7-10 | 14 | 7-17 | 14 | 10-11 |
| T (сек) | 2-138 | >300 | 7 | 4 | 4-300 | >300 | 5-40 | >300 | 15-75 |
| раздроблен (+) не раздроблен (-) | + | – | + | + | + | – | + | – | +(n-3) -(n-3) |
Режим работы при длине волны 1967 нм, частоте повторения 15 кГц, энергии импульса 0,4-0,6 мДж оказался не эффективным в 4 случаях из 7. Микроструктурная плотность камней составила от 401ед. HU до 1933 ед. HU
Визуальный контроль полученного перфоративного канала показал, что трещины на конкрементах отсутствовали. В проходящем свете под микроскопом были выявлены неровности контура каналов, разломы отсутствовали (рис. 2).
Рис. 2. Исследование каналов камней микроскопией в проходящем свете (об. х10, ок. х10)
ОБСУЖДЕНИЕ
Проблема развития осложнений при эндоскопическом лечении мочекаменной болезни на фоне возросшей антибиотикорезистентности становится все более актуальной. Ведущим способом удаления конкрементов из чашечно-лоханочной системы почки является перкутанная нефролитолапаксия. При этом стандартный размер нефростомического хода– 24-30 Ch. В последние годы наблюдается тенденция к уменьшению доступа до 14-18 Ch (miniperc). Однако преимущества кожухов меньшего размера при стандартной чрескожной пункционной нефролитотрипсии не доказаны. Известно, что инструменты меньшего калибра несут риск повышения внутрипочечного давления, удлиняется время выполнения операции [13].
Как отмечалось выше, в настоящее время для литотрипсии традиционно используется излучение Ho:YAG лазеров с ламповой накачкой и энергией в пачках импульсов свободной генерации 0,5-2 Дж, следующих с низкой частотой повторения 5-15 Гц [14,15]. Механизм разрушения конкремента при использовании гольмиевого лазера с импульсно-периодической ламповой накачкой,генерирующего длину волны 2140 нм, состоит в вапоризации камня. Жидкость испаряется во время лазерного импульса с большой энергией, а за счет увеличения и схлопывания пузырьков образуется ударная волна. Дальнейшая передача энергии происходит с паром через образовавшиеся полости.
Сравнительно недавно начали применяться тулиевые волоконные лазеры с длиной волны излучения
1940 нм с пиковой мощностью до 500 Вт в импульсах длительностью в сотни микросекунд [16]. По данным исследования авторов, камни мочевой системы на этой длине волны имеют большее поглощение, чем на длине волны 2120 нм из-за близкого локального максимума поглощения воды. Причем высокая энергия в импульсах также приводит к полному разрушению камня и образованию мелких осколков в чашечно-лоханочной системе почки.
В проведенных нами экспериментах использованы режимы воздействия на камни мочевой системы при длине волны 2097 и 1967 нм. Результаты показали, что оптимальным режимом генерации лазера (на длине волны 2097 нс) для выполнения режима контролируемого разлома камня является частота повторения импульсов 200-1000 Гц длительностью 20-30 нс и энергией импульса 45-55 мДж. То есть режим лазерной генерации со сравнительно малой импульсной энергией (единицы – десятки мДж), но высокой частотой повторения импульсов (сотни герц – десятки килогерц) позволяет обеспечить деструкцию конкрементов на фрагментыс определенным/достаточным для извлечения его через кожух – амплац размером.
Полученные результаты показали, что с точки зрения скорости дробления камней лазер на кристалле Ho:YAG с волоконно-лазерной накачкой (генерирующий на длине волны 2097 нм) значительно превосходит лазер на керамике Tm:Lu2O3 (на длине волны 1967 нм). Однако представляется, что это превосходство связано в основном с большей импульсной энергией лазера на кристалле Ho:YAG (достигающей десятков мДж) по сравнению с импульсной энергией в 0,40,6 мДж лазера на керамике. С другой стороны, длина волны генерации лазера на керамике Tm:Lu2O3 – 1967 нм обеспечивает больший коэффициент поглощения водой, чем излучение Ho:YAG лазера на длине волны 2097 нм. Поэтому при достижении аналогичной импульсной энергии (в десятки мДж) на длине волны 1967 нм следует ожидать более эффективного воздействия на камни, чем излучением на длине волны 2097 нм. Фактором, влияющим на результаты проведенных нами экспериментов, является их выполнение в атмосферном воздухе, хотя камни доставались из раствора и были сырыми к моменту лазерного воздействия. Лазерное дробление камней в жидкой среде (воде или моче) может несколько изменить скорость их разрушения что требует дальнейшего проведения экспериментальной работы.
ВЫВОДЫ
Вариантом профилактики инфекционно-воспалительного процесса в почке после нефролитотрипсии может стать контролируемая деструкция без разбрасывания содержимого конкрементов по полостной системе почки, что возможно обеспечить подбором режимов лазерного воздействия при контактной литотрипсии.
Применение импульсно-периодического Ho:YAG лазера на длине волны 2097 нм с энергией импульсов 2-55 мДж, длительностью 2040 нс и частотой повторения 0,2-10 кГц позволяет выполнять контролируемый разлом камня до фрагментов, дающих возможность осуществить их удаление из почки путем чрескожной пункционной нефролитоэкстракции и, соответственно, профилактировать инфекционновоспалительные процессы в почках за счет минимальной микробной диссеминации тканей. В зависимости от типа камня варьируется энергия импульсов, требуемая для перфорации.
ЛИТЕРАТУРА
1. Мартов А.Г. Мочекаменная болезнь. Прошлое и настоящее. Урология сегодня. URL: http://urotoday.ru/system/files/urologia-1-2010-to-web.pdf;2010;(1): 1,3с.
2. Диденко Л.В., Перепанова Т.С., Толордава Э.Р. и др. К вопросу об инфекционном генезе камней почек (электронно-микроскопическое исследование). Урология 2012;(3):4–7.
3. Чухловин А.Б., Эмануэль Ю.В. Роль локальных инфекций в генезе мочекаменной болезни. Нефрология 2011;15(3):11-16.
4. Палагин И.С., Сухорукова М.В., Дехнич А.В., Эйдельштейн М.В., Шевелев А.Н., Гринев А.В., и др. Современное состояние антибиотикорезистентности возбудителей внебольничных инфекций мочевых путей в России: результаты исследования «ДАРМИС» (2010-2011). Клиническая микробиология и антимикробная химиотерапия 2012;14(4):280-302.
5. Margel D, Ehrlich Y, Brown N, Lask D, Livne P M, Lifshitz DA. Clincal implication of routine stone culture in percutaneous nephrolithotomy-a prospective study. Urology 2006;67(1):26-9. doi: 10.1016/ j.urology.2005.08.008
6. Гольмиевый лазер в медицине. [Под ред. С.В. Грачева]. М.: «Триада-Х», 2003. – 240 с.
7. Pierre S, Preminger GM. Holmium laser for stone management. World J Urol 2007;25(3): 235-9. doi: 10.1007/s00345-007-0162-y
8. Koras O1, Bozkurt IH, Yonguc T, Degirmenci T, Arslan B, Gunlusoy B, et al. Risk fac-tors for postoperative infectious complications following percutaneous nephrolithotomy: a pro-spective clinical study. Urolithiasis 2015;43(1):55-60. doi: 10.1007/s00240-014-0730-8.
9. Yang T, Liu S, Hu J, Wang L, Jiang H. The Evaluation of Risk Factors for Postoperative Infectious Complications after Percutaneous Nephrolithotomy. Biomed Res Int 2017;2017:4832051. doi: 10.1155/2017/4832051.
10. Раджабов У.А., Перепанова Т.С. Метафилактика инфекционных камней почек после перкутанной нефролитотрипсии. Экспериментальная и клиническая урология 2015;(2):80-83
11. Antipov OL, Eranov ID, Kositsyin RI. 36 W Q-switched Ho:YAG laserat 2097 nm pumped by Tm fiber laser: evaluation of different Ho3+doping concentrations. Laser Phys Lett 2017;14(1), 015002.
12. Antipov O, Novikov A, Larin S, Obronov I. Highly efficient 2 μmCWandQ-switchedTm3+:Lu2O3 ceramics lasers in-band pumped by a Raman-shifted erbium fiber laserat 1670 nm. Optics Letters 2016;41(10):2298-2301
13. Tepeler A, Akman T, Silay MS, Akcay M, Ersoz C, Kalkan S, et al. lComparison of intrarenal pelvic pressure during micro-percutaneous nephrolithotomy and conventional percutaneous nephrolithotomy Urolithiasis 2014;42(3): 275-279. doi: 10.1007/s00240-014-0646-3.
14. Zilberman DE, Lipkin ME, Ferrandino MN, Simmons WN, Mancini JG, Raymundo ME, et al.e digital flexible ureteroscope: in vitro assessment of optical characteristics. J Endourol 2011;25(3):519–22. doi: 10.1089/end.2010.0206.
15. Van Cleynenbreugel B, Kılıç Ö, Akand M. Retrograde intrarenal surgery for renal stones – Part 1. Turk J Urol 2017;43(2):112-121. doi: 10.5152/tud.2017.03708.