Амины
Классификация аминов
По числу углеводородных радикалов амины подразделяются на первичные, вторичные и третичные.
Запомните, что основные свойства аминов выражены тем сильнее, чем больше электронной плотности присутствует на атоме азота. Однако, у третичных аминов три углеводородных радикала создают значительные затруднения для химических реакций.
Таким образом, у третичных аминов основные свойства выражены слабее, чем у вторичных аминов. Основные свойства возрастают в ряду: третичные амины (слабые основные свойства) → первичные амины → вторичные амины (основные свойства хорошо выражены).
Номенклатура и изомерия аминов
Названия аминов формируются путем добавления суффикса «амин» к названию соответствующего углеводородного радикала: метиламин, этиламин, пропиламин, изопропиламин, бутиламин и т.д. В случае если радикалов несколько, их перечисляют в алфавитном порядке.
Общая формула предельных аминов CnH2n+3N. Атомы углерода находятся в sp3 гибридизации.
Для аминов характерна структурная изомерия: углеродного скелета, положения функциональной группы и изомерия аминогруппы.
Получение
В основе этой реакции лежит замещение атома галогена в галогеналканах на аминогруппу, при этом образуются амин и соль аммония.
При такой реакции нитрогруппа превращается в аминогруппу, образуется вода.
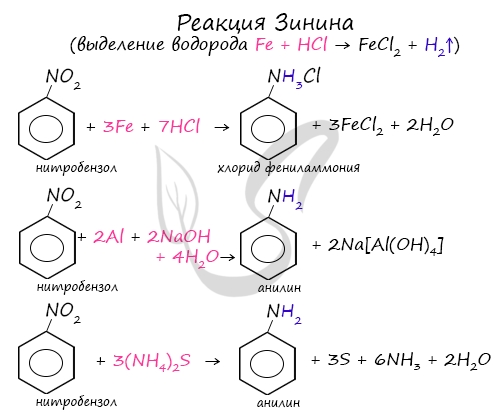
Знаменитой является предложенная в 1842 году Н.Н. Зининым реакция получения аминов восстановления ароматических нитросоединений (анилина и других). Она возможна в нескольких вариантах, главное, чтобы в начале реакции выделился водород.
Реакция сопровождается разрушением карбонильной группы и отщеплении ее от молекулы амида в виде воды.
В промышленности амины получают реакцией аммиака со спиртами, в ходе которой происходит замещение гидроксогруппы на аминогруппу.
В ходе реакции галогеналканов с аммиаком, аминами, становится возможным получение первичных, вторичных и третичных аминов.
Химические свойства аминов
Как и аммиак, амины обладают основными свойствами, их растворы окрашивают лакмусовую бумажку в синий цвет.
В реакции с водой амины образуют гидроксиды алкиламмония, которые аналогичны гидроксиду аммония. Анилин с водой не реагирует, так как является слабым основанием.
Как основания, амины вступают в реакции с различными кислотами и образуют соли алкиламмония.
Данная реакция помогает различить первичные, вторичные и третичные амины, которые по-разному с ней взаимодействуют.
При конденсации первичных аминов с альдегидами и кетонами получают основания Шиффа, соединения, которые содержат фрагмент «N=C».
Соли аминов легко разлагаются щелочами (растворимыми основаниями). В результате образуется исходный амин, соль кислоты и вода.
При горении аминов азот чаще всего выделяется в молекулярном виде, так как для реакции азота с кислородом необходима очень высокая температура. Выделение углекислого газа и воды обыкновенно при горении органических веществ.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Амины. Аминокислоты
Амины
Амины – это производные аммиака, в молекуле которого один, два или три атома водорода замещены углеводородными радикалами.
Классификация
По числу углеводородных радикалов, замещающих атомы водорода в молекуле NH3, все амины можно разделить на три типа:
Группа – NH2 называется аминогруппой.
Существуют также амины, которые содержат две, три и более аминогрупп, например:
Изомерия
Рассмотри все виды изомерии на примере аминов с эмпирической формулой C4H11N:
Физические свойства
Низшие предельные первичные амины — газообразные вещества, имеют запах аммиака, хорошо растворяются в воде. Амины с большей относительной молекулярной массой — жидкости или твердые вещества, растворимость их в воде с увеличением молекулярной массы уменьшается.
Химические свойства
По химическим свойствам амины похожи на аммиак.
1.Взаимодействие с водой — образование гидроксидов замещенного аммония.
Вспомним, как взаимодействует с водой аммиак:
Раствор аммиака в воде обладает слабыми щелочными (основными) свойствами. Причина основных свойств аммиака — наличие у атома азота неподеленной электронной пары, которая участвует в образовании донорно-акцепторной связи с ионом водорода. По этой же причине амины также являются слабыми основаниями. Амины — органические основания:
Растворимые амины — более сильные основания, чем аммиак.
2.Взаимодействие с кислотами — образование солей (реакции нейтрализации).
Как основание аммиак с кислотами образует соли аммония:
Аналогично при взаимодействии аминов с кислотами образуются соли замещенного аммония:
Щелочи, как более сильные основания, вытесняют аммиак и амины из их солей:
3.Горение аминов
Амины являются горючими веществами. Продуктами горения аминов, как и других азотсодержащих органических соединений, являются углекислый газ, вода и свободный азот; например:
Способы получения
1.Взаимодействие спиртов с аммиаком при нагревании в присутствии Аl2О3 в качестве катализатора. Примеры смотреть в теме «Спирты».
2.Взаимодействие алкилгалогенидов (галогеналканов) с аммиаком; например:
Образовавшийся первичный амин может вступать в реакцию с избытком алкилгалогенида и аммиака, в результате чего образуется вторичный амин:
Аналогично могут быть получены третичные амины.
Анилин
Анилин — простейший представитель первичных ароматических аминов:
Физические свойства
Анилин — бесцветная маслянистая жидкость с характерным запахом, малорастворим в воде, ядовит.
Химические свойства
Основные свойства у анилина выражены очень слабо, так как сказывается влияние бензольного ядра на аминогруппу.
1.Реакции с участием аминогруппы
2.Реакции с участием бензольного кольца
Аминогруппа как заместитель I рода облегчает реакции замещения в бензольном ядре, при этом заместители становятся в орто- и пара- положения к аминогруппе:
Получение анилина
Анилин и другие первичные ароматические амины получают с помощью реакции, открытой в 1842 г. русским химиком Н. Н. Зининым. Реакция Зинина — это метод получения ароматических аминов (в том числе анилина) восстановлением нитросоединений:
Это общий, но не единственный способ получения ароматических аминов.
Применение анилина
Аминокислоты
Аминокислоты — это производные углеводородов, содержащие аминогруппы (—NH2) и карбоксильные группы.
Общая формула: (NH2)mR(COOH)n, где m и n чаще всего равны 1 или 2. Таким образом, аминокислоты являются соединениями со смешанными функциями.
Аминокислоты организма:
Заменимые — синтезируются в организме человека, к ним относятся глицин, аланин, глутаминовая кислота, серин, аспарагиновая кислота, тирозин, цистеин.
Незаменимые – не синтезируются в организме человека, поступают с пищей. К ним относятся валин, лизин, фенилаланин.
Физические свойства
Аминокислоты — бесцветные кристаллические вещества, хорошо растворяются в воде, температура плавления 230—300 о С. Многие α-аминокислоты имеют сладкий вкус.
Способы получения
Для получения α-аминокислот в лабораторных условиях обычно используют два следующих способа.
1.Взаимодействие α-галогенкарбоновых кислот с избытком аммиака. В ходе этих реакций происходит замещение атома галогена в галогенкарбоновых кислотах на аминогруппу. Выделяющийся при этом хлороводород связывается избытком аммиака в хлорид аммония. Например, аланин можно получить при взаимодействии α-хлорпропионовой кислоты с аммиаком:
2.Гидролиз белков. При гидролизе белков обычно образуются сложные смеси аминокислот, однако с помощью специальных методов из этих смесей можно выделять отдельные чистые аминокислоты.
Химические свойства
а) как кислота (участвует карбоксильная группа):
б) как основание (участвует аминогруппа):
2.Взаимодействие внутри молекулы — образование внутренних солей:
а) моноаминомонокарбоновые кислоты (нейтральные кислоты).
Водные растворы моноаминомонокарбоновых кислот нейтральны (рН = 7);
б) моноаминодикарбоновые кислоты (кислые аминокислоты).
Водные растворы моноаминодикарбоновьж кислот имеют РН 7 (щелочная среда), так как в результате образования внутренних солей этих кислот в растворе появляется избыток гидроксид-ионов ОН.
3. Взаимодействие аминокислот друг с другом — образование пептидов:
Две аминокислоты образуют дипептид:
При составлении названия дипептида сначала называют аминокислоту, у которой в образовании дипептид участвует группа —СООН. В тривиальном названии этой кислоты последняя буква «н» заменяется буквой «л». Затем прибавляют без изменений тривиальное название аминокислоты, у которой в образовании дипептида участвует группа —NH2.
Любой дипептид имеет свободные амино- и карбоксильную группы и поэтому может взаимодействовать еще с одной молекулой аминокислоты, образуя трипептид; таким же путем получают тетрапептиды и т. д.:
Аминогруппа (NH2): строение, свойства, примеры
Содержание:
Амиды, RC (O) NH2с карбонильной группой C = O, также являются другим примером соединений, содержащих аминогруппу. Во многих других соединениях аминогруппы встречаются просто как заместители, поскольку в остальной структуре могут быть оксигенированные группы с большей химической значимостью.
Аминогруппа считается побочным продуктом аммиака, NH3. Когда три его связи N-H заменяются связями N-C, возникают соответственно первичные, вторичные и третичные амины. То же самое относится и к амидам.
Соединения с аминогруппами характеризуются как основные или щелочные вещества. Они также являются частью множества биомолекул, таких как белки и ферменты, а также фармацевтических продуктов. Из всех функциональных групп она, вероятно, самая разнообразная из-за замен или преобразований, которым она способна подвергаться.
Состав
И не говоря уже о пространстве, которое неподеленная пара электронов занимает на азоте, который может образовывать связи с протонами в середине. Отсюда основность аминогруппы.
Свойства
Основность
Быть RNH3 + полученная конъюгированная кислота. Боковая цепь R помогает уменьшить плотность положительного заряда, который теперь появляется на атоме азота. Таким образом, чем больше групп R, тем меньше будет «ощущаться» положительный заряд, поэтому стабильность конъюгированной кислоты будет увеличиваться; что, в свою очередь, означает, что амин является более основным.
Аналогичное рассуждение может быть применено, учитывая, что цепи R вносят вклад в электронную плотность атома азота, «усиливая» отрицательную плотность неподеленной пары электронов, тем самым увеличивая основной характер амина.
Затем говорят, что основность аминогруппы увеличивается по мере того, как она становится более замещенной. Из всех аминов наиболее основными являются третичные амины. То же самое происходит с амидами и другими соединениями.
Полярность и межмолекулярные взаимодействия
Аминогруппы придают полярность молекуле, к которой они присоединены, благодаря их электроотрицательному атому азота.
Следовательно, соединения, содержащие NH2 Они не только базовые, но и полярные. Это означает, что они склонны растворяться в полярных растворителях, таких как вода или спирты.
Его температуры плавления или кипения также значительно высоки в результате диполь-дипольных взаимодействий; в частности, водородных мостиков, которые устанавливаются между двумя NH2 соседних молекул (RH2N-HNHR).
Хотя группа NH2 вносит вклад в полярность и сильные молекулярные взаимодействия в соединение, его влияние меньше по сравнению, например, с действием групп ОН или СООН.
Кислотность
Хотя аминогруппа отличается своей основностью, она также имеет определенный кислотный характер: она вступает в реакцию с сильными основаниями или может нейтрализоваться ими. Рассмотрим следующую реакцию нейтрализации:
Примеры
Некоторые примеры соединений, содержащих группу NH, будут перечислены ниже.2, без замен; то есть вторичные или третичные амины не рассматриваются. Тогда у нас есть:
Последние четыре примера соответствуют аминокислотам, фундаментальным частям, из которых построены белки, и в молекулярных структурах которых присутствуют обе группы NH.2 как группа COOH.
Эти четыре аминокислоты содержат в своих боковых цепях R группу NH.2 дополнительный, так что при образовании пептидной связи (объединение двух аминокислот через их NH-концы2 и COOH) NH не исчезает2 в образующихся белках.
Помимо аминокислот, в организме человека есть другие соединения, несущие группу NH.2: Так обстоит дело с гистамином (см. Выше), одним из многих нейромедиаторов. Обратите внимание, насколько азотистая его молекулярная структура.
Ссылки
Болезнь Паркинсона: причины, симптомы, лечение и профилактика
Учебная программа: цель, виды учебной программы, структура
Амины: способы получения, строение и свойства
Амины – это органические производные аммиака NH3, в молекуле которого один, два или три атома водорода замещены на углеводородные радикалы.
Строение аминов
Также атом азота в аминах имеет неподелённую электронную пару, поэтому амины проявляют свойства органических оснований.
Классификация аминов
По количеству углеводородных радикалов, связанных с атомом азота, различают первичные, вторичные и третичные амины.
По типу радикалов амины делят на алифатические, ароматические и смешанные.
| Амины | Первичные | Вторичные | Третичные | |||||||||||
| Алифатические | Метиламин CH3-NH2 | Диметиламин CH3-NH-CH3 | Триметиламин (CH3)3N | |||||||||||
| Ароматические | Фениламин C6H5-NH2 | Дифениламин (C6H5)2NH | Трифениламин (C6H5)3N | |||||||||||
| Смешанные | Метилфениламин CH3-NH-C6H5 | Диметилфениламин Номенклатура аминовПри наличии одинаковых радикалов используют приставки ди и три. В этом случае аминогруппа указывается в названии приставкой амино-: Например, N-метиланилин: Символ N- ставится перед названием алкильного радикала, чтобы показать, что этот радикал связан с атомом азота, а не является заместителем в бензольном кольце. Изомерия аминовДля аминов характерна изомерия углеродного скелета, изомерия положения аминогруппы и изомерия различных типов аминов. Изомерия углеродного скелетаДля аминов характерна изомерия углеродного скелета (начиная с С4H9NH2).
Изомерия положения аминогруппыДля аминов характерна изомерия положения аминогруппы (начиная с С3H9N).
Изомерия между типами аминов
(первичный амин) | Метилэтиламин (вторичный амин) | Триметиламин (третичный амин) | ||||||||||
 |  |  |
Физические свойства аминов
При обычной температуре низшие алифатические амины CH3NH2, (CH3)2NH и (CH3)3N – газы (с запахом аммиака), средние гомологи – жидкости (с резким рыбным запахом), высшие – твердые вещества без запаха.
Ароматические амины – бесцветные жидкости с высокой температурой кипения или твердые вещества.
Первичные и вторичные амины образуют слабые межмолекулярные водородные связи:
Это объясняет относительно более высокую температуру кипения аминов по сравнению с алканами с близкой молекулярной массой.
Амины также способны к образованию водородных связей с водой:
Поэтому низшие амины хорошо растворимы в воде.
С увеличением числа и размеров углеводородных радикалов растворимость аминов в воде уменьшается. Ароматические амины в воде не растворяются.
Химические свойства аминов
| Амины имеют сходное с аммиаком строение и проявляют подобные ему свойства. |
Как в аммиаке, так и в аминах атом азота имеет неподеленную пару электронов:


| Поэтому амины и аммиак обладают свойствами оснований. |
1. Основные свойства аминов
| Алифатические амины являются более сильными основаниями, чем аммиак, а ароматические — более слабыми. |
Это объясняется тем, что радикалы СН3–, С2Н5– увеличивают электронную плотность на атоме азота:
Это приводит к усилению основных свойств.
| Основные свойства аминов возрастают в ряду: |
1.1. Взаимодействие с водой
В водном растворе амины обратимо реагируют с водой. Среда водного раствора аминов — слабощелочная:
1.2. Взаимодействие с кислотами
Амины реагируют с кислотами, как минеральными, так и карбоновыми, и аминокислотами, образуя соли (или амиды в случае карбоновых кислот):
При взаимодействии аминов с многоосновными кислотами возможно образование кислых солей:
1.3. Взаимодействие с солями
Амины способны осаждать гидроксиды тяжелых металлов из водных растворов.
| Например, при взаимодействии с хлоридом железа (II) образуется осадок гидроксида железа (II): |
2. Окисление аминов
Амины сгорают в кислороде, образуя азот, углекислый газ и воду. Например, уравнение сгорания этиламина:
3. Взаимодействие с азотистой кислотой
Первичные алифатические амины при действии азотистой кислоты превращаются в спирты:
| Это качественная реакция на первичные амины – выделение азота. |
Вторичные амины (алифатические и ароматические) образуют нитрозосоединения — вещества желтого цвета:
4. Алкилирование аминов
Первичные амины способны взаимодействовать с галогеналканами с образованием соли вторичного амина:
Из полученной соли щелочью выделяют вторичный амин, который можно далее алкилировать до третичного амина.
Особенности анилина
Анилин С6H5-NH2 – это ароматический амин.
| Анилин – бесцветная маслянистая жидкость с характерным запахом. На воздухе окисляется и приобретает красно-бурую окраску. Ядовит. В воде практически не растворяется. |
При 18 о С в 100 мл воды растворяется 3,6г анилина. Раствор анилина не изменяет окраску индикаторов.
| Для анилина характерны реакции как по аминогруппе, так и по бензольному кольцу. |
Анилин не реагирует с водой, но реагирует с сильными кислотами, образуя соли:
Реакция с галогенами идёт без катализатора во все три орто- и пара- положения.
| Качественная реакция на анилин: реагирует с бромной водой с образованием 2,4,6-триброманилина (белый осадок ↓). |
Получение аминов
Восстановление нитросоединений
Первичные амины можно получить восстановлением нитросоединений.
Алюминий реагирует с щелочами с образованием гидроксокомплексов.
В щелочной и нейтральной среде получаются амины.
Восстановлением нитробензола получают анилин.
При этом образуются не сами амины, а соли аминов:
Амины из раствора соли выделяют с помощью щелочи:
Алкилирование аммиака и аминов
При взаимодействии аммиака с галогеналканами происходит образование соли первичного амина, из которой действием щелочи можно выделить сам первичный амин.
Если проводить реакцию с избытком аммиака, то сразу получится амин, а галогеноводород образует соль с аммиаком:
Гидрирование нитрилов
Таким образом получают первичные амины. Возможно восстановление нитрилов водородом на катализаторе:
.
Соли аминов
Соль амина с более слабыми основными свойствами может реагировать с другим амином, образуя новую соль (более сильные амины вытесняют менее сильные из солей):
12 комментариев
Добавить ваш
Да, спасибо, поправил. В узком смысле реакцией Зинина называют получение именно ароматических аминов, в широком смысле так называют восстановление любых нитросоединений сульфидом аммония.
Здравствуйте! Скажите, пожалуйста, реагируют ли третичные амины с галогеналканами? Если да, то как идет реакция и что получается? Например,при взаимодействии триметиламина с хлорметаном?
Здравствуйте! Реагируют, но дальнейшее замещение по связям N-H не идет.
Здравствуйте! Не показано взаимодействие аминов со спиртами.
Третичные амины с алкилгалогенидами реагируют. Получаются четвертичные аммониевые соли. Говорить, что они вообще не реагируют, неправильно. Они не вступают в реакцию алкилирования.
По такой схеме за счет пары электронов на азоте реагируют алифатические амины, ароматические амины, пиридин с получением N-алкилпиридинийхлорида (иодида) и пр.
Да, спасибо за комментарий. Я имел в виду, что не идет дальнейшее замещение.
спасибо, отличная идея!
для полноты информации я бы добавил оптическую изомерию и примеры этой изомерии ко всем классам органических веществ, потому что на егэ это есть
На ЕГЭ пока оптической изомерии нет.
Admin>Здравствуйте! Реагируют, но дальнейшее замещение по связям N-H не идет.
что значит «дальнейшее»? у триметиламина — и так уже нет N-H связей, может вы имели в виду протонированный триметил-амин (скажем) солянокислый, что в форме соли он останется третичным амином например до момента щелочного депротонирования(высвобождения основания амина)
—
а что кстати, есть способ галоидным алкилом моноалкилирование первичного ароматического амина до вторичного осуществить, избежав образования третичного амина — диалкилированного уже
на этилировании уже проще, а вот метиллирование нейромедиаторов не удавалось остановить на стадии N,N-ДиМет.(например в ацетоне с карбонатом калия, или с DIPEA), выход третичного целевого амина всегда оказывался либо самым низким из продуктов реакции, либо просто очень низким(10% в сложной смеси аминов с преобладанием четвертичной соли триметиламмония метилиодида, а сейчас подумал — если при N-метилировании первичного ароматического амина метилиодидом, образуется гидроиодид N-метил…исх.пер.амина, он же даже во второе метиллирование уже не должен входить, усиленным основанием став (скажем адреналином, основнее норадреналина исходного как я понимаю за счет появившегося электроннодонороного метила) и так будет выведен из реакционной среды(например выпав осадком соли, не солватированной в неполярной РС)
получается в отсутствие основного катализа алкилирование первичных аминов ограничивается моно-алкилированием — не далее чем до вторичного амина? или на практике соли не так надёжны как в оптимистичных прогнозах теоретизирующего учащегося?
Добавить комментарий Отменить ответ
Этот сайт использует Akismet для борьбы со спамом. Узнайте, как обрабатываются ваши данные комментариев.