Двухосновные предельные карбоновые кислоты
Двухосновные предельные карбоновые кислоты (двухосновные насыщенные карбоновые кислоты) – карбоновые кислоты, в которых насыщенный углеводородный радикал соединен с двумя карбоксильными группами –COOH. Все они имеют общую формулу HOOC(CH2)nCOOH, где n = 0, 1, 2, …
Номенклатура
Систематические названия двухосновных предельных карбоновых кислот даются по названию соответствующего алкана с добавлением суффикса -диовая и слова кислота.
Изомерия
Изомерия скелета в углеводородном радикале проявляется, начиная с бутандиовой кислоты, которая имеет два изомера:
Гомологический ряд
| Тривиальное название | Название по ИЮПАК | Формула | Название солей |
|---|---|---|---|
| Щавелевая кислота | Этандиовая кислота | HOOCCOOH | оксалаты |
| Малоновая кислота | Пропандиовая кислота | HOOCСH2COOH | малонаты |
| Янтарная кислота | Бутандиовая кислота | HOOC(СH2)2COOH | сукцинаты |
| Глутаровая кислота | Пентандиовая кислота | HOOC(СH2)3COOH | глутараты |
| Адипиновая кислота | Гександиовая кислота | HOOC(СH2)4COOH | адипинаты |
| Пимелиновая кислота | Гептандиовая кислота | HOOC(СH2)5COOH | пимелинаты |
| Пробковая кислота | Октандиовая кислота | HOOC(СH2)6COOH | субераты |
| Азелаиновая кислота | Нонандиовая кислота | HOOC(СH2)7COOH | азелаинаты |
| Себациновая кислота | Декандиовая кислота | HOOC(СH2)8COOH | себацинаты |
| — | Ундекандиовая кислота | HOOC(СH2)9COOH | |
| — | Додекандиовая кислота | HOOC(СH2)10COOH | |
| Брассиловая кислота | Тридекандиовая кислота | HOOC(СH2)11COOH | |
| — | Тетрадекандиовая кислота | HOOC(СH2)12COOH | |
| — | Пентадекандиовая кислота | HOOC(СH2)13COOH | |
| Тапсиевая кислота | Гексадекандиовая кислота | HOOC(СH2)14COOH | |
| — | Гептадекандиовая кислота | HOOC(СH2)15COOH | |
| — | Октадекандиовая кислота | HOOC(СH2)16COOH | |
| — | Нонадекандиовая кислота | HOOC(СH2)17COOH | |
| — | Эйкозандиовая кислота | HOOC(СH2)18COOH | |
| Японовая кислота | Генэйкозандиовая кислота | HOOC(СH2)19COOH |
Полезное
Смотреть что такое «Двухосновные предельные карбоновые кислоты» в других словарях:
Двухосновные насыщенные карбоновые кислоты — Двухосновные предельные карбоновые кислоты (двухосновные насыщенные карбоновые кислоты) – карбоновые кислоты, в которых насыщенный углеводородный радикал соединен с двумя карбоксильными группами –COOH. Все они имеют общую формулу HOOC(CH2)nCOOH,… … Википедия
Двухосновные карбоновые кислоты — (или дикарбоновые кислоты) это карбоновые кислоты, содержащие две карбоксильные группы COOH, с общей формулой HOOC R COOH, где R любой двухвалентный органический радикал. Содержание 1 Химические свойства 2 Примеры … Википедия
Предельные дикарбоновые кислоты — Двухосновные предельные карбоновые кислоты (двухосновные насыщенные карбоновые кислоты) – карбоновые кислоты, в которых насыщенный углеводородный радикал соединен с двумя карбоксильными группами –COOH. Все они имеют общую формулу HOOC(CH2)nCOOH,… … Википедия
Дикарбоновые кислоты — Двухосновные карбоновые кислоты (дикарбоновые кислоты) – это карбоновые кислоты, содержащие две карбоксильные группы –COOH. Общей формулой HOOC R–COOH, где R любой двухвалентный органический радикал. Содержание 1 Химические свойства 2 Примеры … Википедия
Насыщенные дикарбоновые кислоты — Двухосновные предельные карбоновые кислоты (двухосновные насыщенные карбоновые кислоты) – карбоновые кислоты, в которых насыщенный углеводородный радикал соединен с двумя карбоксильными группами –COOH. Все они имеют общую формулу HOOC(CH2)nCOOH,… … Википедия
Кислота — У этого термина существуют и другие значения, см. Кислота (значения) … Википедия
Азелаиновая кислота — Азелаиновая кислота … Википедия
Адипиновая кислота — Адипиновая кислота … Википедия
Малоновая кислота — Общие … Википедия
Себациновая кислота — Номенклатура Тривиальное название себациновая кислота Систематическое название декандиовая кислота … Википедия
Двухосновные карбоновые кислоты
Двухосновные карбоновые кислоты (или дикарбоновые кислоты) — это карбоновые кислоты, содержащие две карбоксильные группы —COOH, с общей формулой HOOC—R—COOH, где R — любой двухвалентный органический радикал.
Содержание
Химические свойства
Дикарбоновые кислоты проявляют те же химические свойства, что и монокарбоновые — эти свойства обусловлены наличием карбоксильной группы:
В то же время есть существенные различия, обусловленные наличием второй карбоксильной группы:
Примеры
| Тривиальное название | Систематическое название | Химическая структура | Ka1 | Ka2 |
|---|---|---|---|---|
| Щавелевая кислота | Этандиовая кислота | HOOC—COOH | 1,27 | 4,23 |
| Малоновая кислота | Пропандиовая кислота | НООС—СН2—СООН | 2,87 | 5,70 |
| Янтарная кислота | Бутандиовая кислота | НООС—(СН2)2—СООН | 4,16 | 5,61 |
| Глутаровая кислота | Пентандиовая кислота | НООС—(СН2)3—СООН | 4,34 | 5,27 |
| Адипиновая кислота | Гександиовая кислота | НООС—(СН2)4—СООН | 4,26 | 5,30 |
| Пимелиновая кислота | Гептандиовая кислота | НООС—(СН2)5—СООН | ||
| Субериновая кислота | Октандиовая кислота | НООС—(СН2)6—СООН | ||
| Азелаиновая кислота | Нонандиовая кислота | НООС—(СН2)7—СООН | 4,55 | 5,42 |
| Себациновая кислота | Декандиовая кислота | НООС—(СН2)8—СООН | 4,62 | 5,59 |
| Фталевая кислота | Бензол-1,2-дикарбоновая кислота | 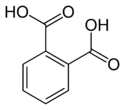 | 3,54 | 4,46 |
| Изофталевая кислота | Бензол-1,3-дикарбоновая кислота | 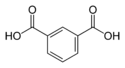 | ||
| Терефталевая кислота | Бензол-1,4-дикарбоновая кислота | 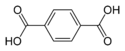 |
Другие важные представители
Применение
Используются для получения полиамидов и полиэфиров — например, таких широкоизвестных полимеров, как капрон и полиэтилентерефталат.
См. также
Полезное
Смотреть что такое «Двухосновные карбоновые кислоты» в других словарях:
Двухосновные предельные карбоновые кислоты — (двухосновные насыщенные карбоновые кислоты) – карбоновые кислоты, в которых насыщенный углеводородный радикал соединен с двумя карбоксильными группами –COOH. Все они имеют общую формулу HOOC(CH2)nCOOH, где n = 0, 1, 2, … Номенклатура… … Википедия
Двухосновные насыщенные карбоновые кислоты — Двухосновные предельные карбоновые кислоты (двухосновные насыщенные карбоновые кислоты) – карбоновые кислоты, в которых насыщенный углеводородный радикал соединен с двумя карбоксильными группами –COOH. Все они имеют общую формулу HOOC(CH2)nCOOH,… … Википедия
КАРБОНОВЫЕ КИСЛОТЫ — органические соединения, содержащие одну или несколько карбоксильных групп СООН. Известны одноосновные карбоновые кислоты RCOOH (уксусная, бензойная), двухосновные R(COOH)2 (щавелевая, фталевая) и многоосновные (лимонная) (R органический радикал) … Большой Энциклопедический словарь
КАРБОНОВЫЕ КИСЛОТЫ — КАРБОНОВЫЕ КИСЛОТЫ, органические соединения, содержащие одну или несколько карбоксильных групп COOH. По числу таких групп различают одноосновные карбоновые кислоты (например, уксусная), двухосновные (например, щавелевая) и многоосновные (например … Современная энциклопедия
Карбоновые кислоты — КАРБОНОВЫЕ КИСЛОТЫ, органические соединения, содержащие одну или несколько карбоксильных групп COOH. По числу таких групп различают одноосновные карбоновые кислоты (например, уксусная), двухосновные (например, щавелевая) и многоосновные (например … Иллюстрированный энциклопедический словарь
карбоновые кислоты — органические соединения, содержащие одну или несколько карбоксильных групп СООН. Различают карбоновые кислоты одноосновные RCOOH (уксусная, бензойная), двухосновные R(COOH)2 (щавелевая, фталевая) и многоосновные (лимонная) (R органический… … Энциклопедический словарь
КАРБОНОВЫЕ КИСЛОТЫ — органич соед., содержащие одну или неск. карбоксильных групп СООН. Различают К. к. одноосновные RCOOH (уксусная, бензойная), двухосновные R(COOH)2 (щавелевая, фталевая) и многоосновные (лимонная) (R органич. радикал). К. к. обычно значительно… … Естествознание. Энциклопедический словарь
Кислоты и основания — классы химических соединений. Обычно кислотами называют вещества, содержащие водород (HCl, HNO3, H2SO4, CH3COOH и т.д.) и диссоциирующие в воде с образованием ионов Н+ (точнее, ионов гидроксония H3O+). Присутствие этих ионов обусловливает … Большая советская энциклопедия
Дикарбоновые кислоты — Двухосновные карбоновые кислоты (дикарбоновые кислоты) – это карбоновые кислоты, содержащие две карбоксильные группы –COOH. Общей формулой HOOC R–COOH, где R любой двухвалентный органический радикал. Содержание 1 Химические свойства 2 Примеры … Википедия
Насыщенные дикарбоновые кислоты — Двухосновные предельные карбоновые кислоты (двухосновные насыщенные карбоновые кислоты) – карбоновые кислоты, в которых насыщенный углеводородный радикал соединен с двумя карбоксильными группами –COOH. Все они имеют общую формулу HOOC(CH2)nCOOH,… … Википедия
Двухосновные насыщенные и ненасыщенные карбоновые кислоты
Молекулы двухосновных (дикарбоновых) кислот содержат насыщенный или ненасыщенный углеводородный радикал и две карбоксильные группы. Двухосновные карбоновые кислоты имеют общую формулу НООС-R-СООН.
Если карбоксильные группы связаны с насыщенным углеводородным радикалом, то кислота является насыщенной (предельной) и ненасыщенной (непредельной), если карбоксильные группы связаны с ненасыщенным углеводородным радикалом, например, бутандиовая (янтарная) и бутендиовая кислоты:
Изомерия и номенклатура двухосновных насыщенных и ненасыщенных карбоновых кислот
Согласно правилам систематической номенклатуры ИЮПАК дикарбоновые кислоты называют аналогично соответствующим углеводородам, прибавляя окончание — диовая или слово дикарбоновая кислота. Например, пропандиовая или пропандикарбоновая кислота, пентандиовая или пентандикарбоновая кислота.
Первые девять членов ряда предельных дикарбоновых кислот имеют тривиальные названия. Тривиальные названия, названия по систематической номенклатуре и структурные формулы некоторых дикарбоновых кислот приведены в таблице:
Двухосновные карбоновые кислоты: Физические и химические свойства
Физические свойства дикарбоновых кислот
Двухосновные карбоновые кислоты – твердые кристаллические вещества. Они достаточно хорошо растворимы в воде, причем растворимость их выше, чем у соответствующих одноосновных (монокарбоновых) кислот. Температуры их кипения также выше, чем у монокарбоновых кислот. Это обусловлено тем, что большее число карбоксильных групп, способно образовывать большее число водородных связей, вследствие чего происходит ассоциация молекул.
Химические свойства дикарбоновых кислот
Двухосновные карбоновые кислоты сохраняют общие свойства одноосновных карбоновых кислот, такие как, способность образовывать полные или неполные функциональные производные – соли, эфиры и т.п. и специфические свойства.
Специфические химические свойства дикарбоновых кислот:
Двухступенчатая диссоциация в растворах:
Для первых двух членов ряда ионизация по первой ступени протекает легче, чем по второй. Для кислот с числом атомов углерода более 5 этого различия практически не наблюдается.
2. Действие температуры. Дикарбоновые кислоты, в отличие от монокарбоновых, менее устойчивы к повышенным температурам. При нагревании происходит их декарбоксилирование либо дегидратация. При этом, в зависимости от строения кислоты образуются различные продукты:
Среди дикарбоновых кислот важное место занимает малоновая кислота. Атомы водорода метиленовой группы являются очень подвижными и подвергаются электрофильному замещению:
На основе малонового эфира (диэтилового эфира малоновой кислоты) осуществляются важные синтезы.
Алкилмалоновый эфир также способен образовывать соединение с натрием и далее алкилироваться:
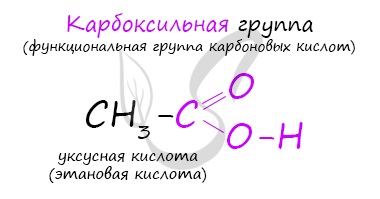
Карбоновые кислоты
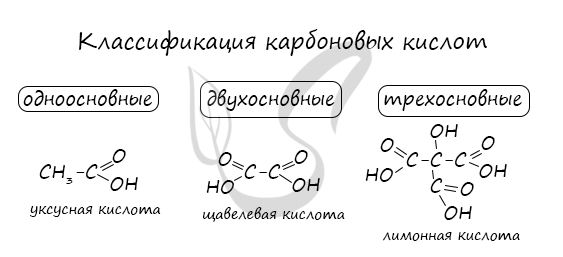
Классификация карбоновых кислот
Высшие карбоновые кислоты называют жирными кислотами. Более подробно мы изучим их теме, посвященной жирам, в состав которых они входят.
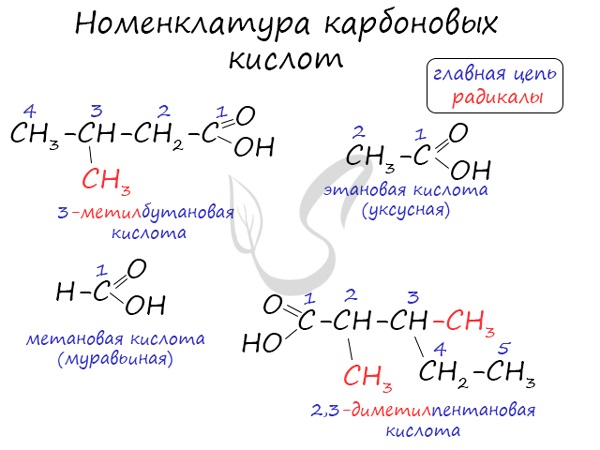
Номенклатура и изомерия карбоновых кислот
Названия карбоновых кислот формируются путем добавления суффикса «овая» к названию алкана с соответствующим числом атомов углерода и слова кислота: метановая кислота, этановая кислота, пропановая кислота, и т.д.
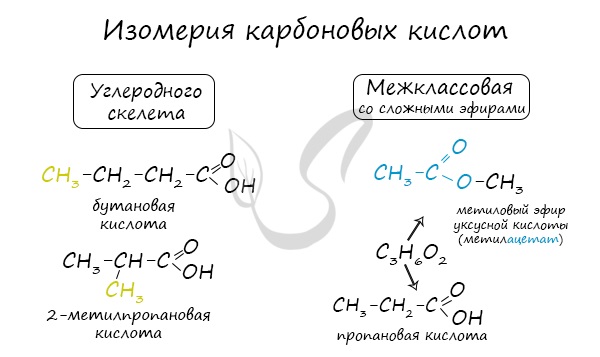
Для предельных карбоновых кислот характерна структурная изомерия: углеродного скелета, межклассовая изомерия со сложными эфирами.
Получение карбоновых кислот
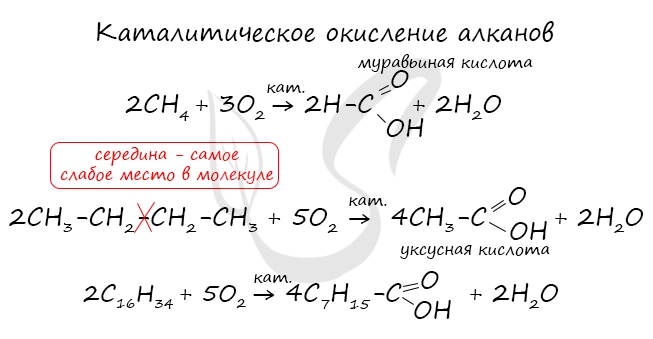
При повышенной температуре и в присутствии катализатора становится возможным неполное окисление алканов, в результате которого образуются кислоты.
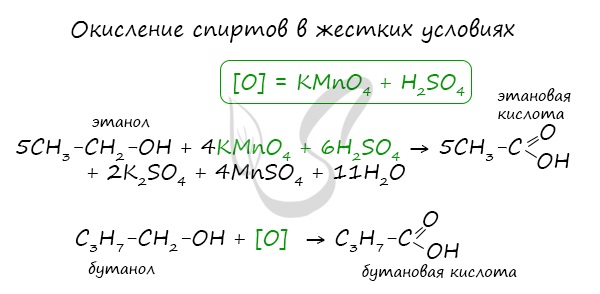
При реакции спиртов с сильными окислителями, такими как подкисленный раствор перманганата калия, спирты окисляются до соответствующих кислот.
Обратите особое внимание, что при написании реакции с аммиачным раствором серебра в полном виде, правильнее будет указать не кислоту, а ее аммиачную соль. Это связано с тем, что выделяющийся аммиак, который обладает основными свойствами, реагирует с кислотой с образованием соли.
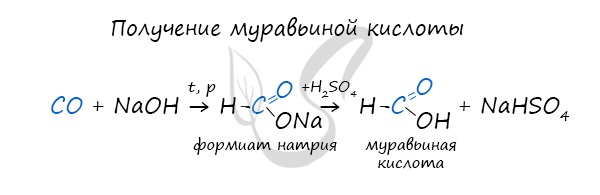
При дальнейшей обработке формиата серной кислотой образуется муравьиная кислота.
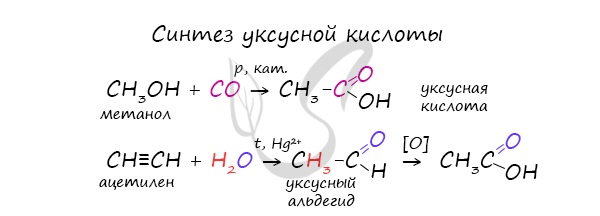
Специфичность синтеза уксусной кислоты заключается в реакции угарного газа с метанолом, в результате которой она образуется.
Также уксусную кислоту можно получить другим путем: сначала провести реакцию Кучерова, в ходе которой образуется уксусный альдегид. Окислить его до уксусной кислоты можно аммиачным раствором оксида серебра или гидроксидом меди II.
Химические свойства карбоновых кислот
Для карбоновых кислот не характерны реакции присоединения. Карбоновые кислоты обладают более выраженными кислотными свойствами, чем спирты.
Карбоновые кислоты вступают в реакции с металлами, которые способны вытеснить водород (стоят левее водорода в ряду напряжений металлов) из кислоты. Реагируют также с основаниями, с солями более слабых кислот, например, угольной кислоты.
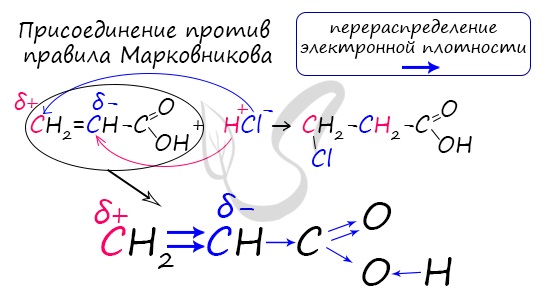
Перераспределение электронной плотности в молекулах этих кислот для лучшего запоминания лучше увидеть наглядно. Это перераспределение обусловлено большей электроотрицательностью хлора, который притягивает электронную плотность.
Муравьиная кислота отличается от своих гомологов. За счет наличия у нее альдегидной группы, она, единственная из карбоновых кислот, способна вступать в реакцию серебряного зеркала.
В такой реакции идет ее окисление до нестойкой угольной кислоты, которая распадается на углекислый газ и воду.
При нагревании и в присутствии серной кислоты (водоотнимающего компонента) муравьиная кислота распадается на воду и угарный газ.
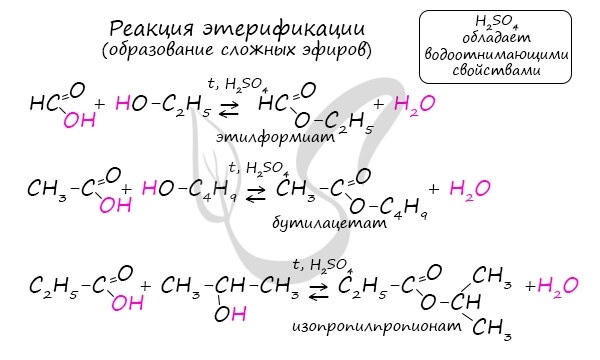
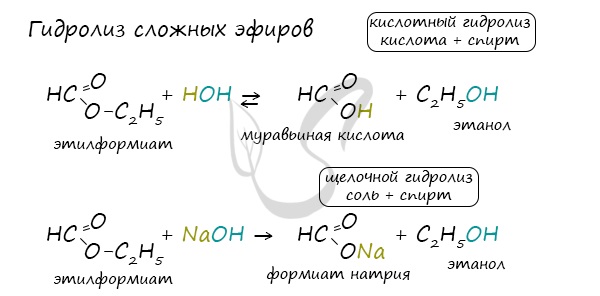
Сложные эфиры
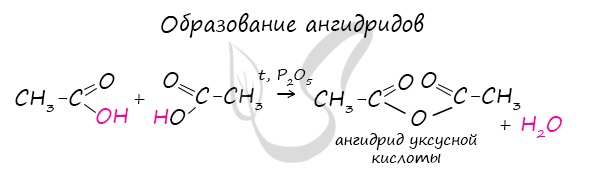
Ангидриды
Хлорангидриды карбоновых кислот образуются в реакции карбоновых кислот с хлоридом фосфора V.
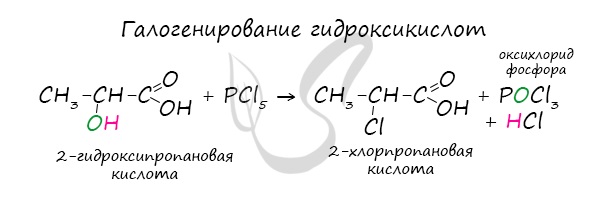
Следующая реакция не имеет отношения к ангидридам, однако (из-за их схожести) вы увидите ее здесь для наилучшего запоминания. Это реакция галогенирования гидроксикислот, в результате которой гидроксогруппа в радикале меняется на атом галогена.
Непредельные карбоновые кислоты
Распределение электронной плотности в молекулах творит чудеса: иногда реакции идут против правила Марковникова. Так происходит в непредельной акриловой кислоте.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.