Кислотные оксиды
Кислотные оксиды (ангидриды) – оксиды, проявляющие кислотные свойства и образующие соответствующие кислородсодержащие кислоты. Образованы типичными неметаллами и некоторыми переходными элементами. Элементы в кислотных оксидах обычно проявляют степень окисления от IV до VII. Они могут взаимодействовать с некоторыми основными и амфотерными оксидами, например: с оксидом кальция CaO, оксидом натрия Na2О, оксидом цинка ZnO, либо с оксидом алюминия Al2O3 (амфотерный оксид).
Характерные реакции
Кислотные оксиды могут реагировать с:
2) с водой (практически все кислотные оксиды при взаимодействии с водой (реакция гидратации) образуют соответствующие им кислотные гидроксиды (кислородосодержащие кислоты). Например, при растворении оксида серы (VI) в воде образуется серная кислота:
Кислотные оксиды могут быть получены из соответствующей кислоты:
Примеры
См. также
Полезное
Смотреть что такое «Кислотные оксиды» в других словарях:
Оксиды металлов — это соединения металлов с кислородом. Многие из них могут соединяться с одной или несколькими молекулами воды с образованием гидроксидов. Большинство оксидов являются основными, так как их гидроксиды ведут себя как основания. Однако некоторые… … Официальная терминология
Оксиды — Оксид (окисел, окись) бинарное соединение химического элемента с кислородом в степени окисления −2, в котором сам кислород связан только с менее электроотрицательным элементом. Химический элемент кислород по электроотрицательности второй… … Википедия
Кислотные дожди — Скульптура, пострадавшая от кислотного дождя Кислотный дождь все виды метеорологических осадков дождь, снег, град, туман, дождь со снегом, при котором наблюдается понижение pH дождевых осадков из за загрязнений воздуха кислотными оксидами (обычно … Википедия
кислотные осадки — дождь, снег или дождь со снегом, имеющие повышенную кислотность. Кислотные осадки возникают главным образом из за выбросов оксидов серы и азота в атмосферу при сжигании ископаемого топлива (угля, нефти и природного газа). Растворяясь в… … Географическая энциклопедия
оксиды — Соединение химического элемента с кислородом. По химическим свойствам все оксиды делятся на солеобразующие (наприме, Na2О, MgO, Al2O3, SiO2, P2O5, SO3, Cl2O7) и несолеобразующие (например, СО, N2O, NO, H2O). Солеобразующие оксиды подразделяют на… … Справочник технического переводчика
ОКСИДЫ — хим. соединения элементов с кислородом (устаревшее название окислы); один из важнейших классов хим. веществ. О. образуются чаще всего при непосредственном окислении простых и сложных веществ. Напр. при окислении углеводородов образуются О.… … Большая политехническая энциклопедия
КИСЛОТНЫЕ ДОЖДИ — (кислые дожди), характеризуются повышенным содержанием кислот (в основном серной); водородный показатель pH Современная энциклопедия
ОКСИДЫ — соединения элементов с кислородом. В О. степень окисления атома кислорода Ч2. К О. относятся все соед. элементов с кислородом, кроме содержащих атомы О, соединенные друг с другом (пероксиды, надпероксиды, озо ниды), и соед. фтора с кислородом… … Химическая энциклопедия
КИСЛОТНЫЕ ОСАДКИ — дождь, снег или дождь со снегом, имеющие повышенную кислотность. Кислотные осадки возникают главным образом из за выбросов оксидов серы и азота в атмосферу при сжигании ископаемого топлива (угля, нефти и природного газа). Растворяясь в… … Энциклопедия Кольера
Оксиды — [oxides] соединение химического элемента с кислородом. По химическим свойствам все оксиды делятся на солеобразующие (например, Na2O, MgO, Al2O3, SiO2, P2O5, SO3, Cl2O7) и несолеобразующие (например, СО, N2O, NO, H2O). Солеобразующие оксиды… … Энциклопедический словарь по металлургии
Кислотные оксиды

Всего получено оценок: 1207.
Всего получено оценок: 1207.
Оксиды – сложные вещества, состоящие из двух элементов, один из которых кислород. В названиях оксидов сначала указывают слово оксид, затем название второго элемента, которым он образован. Какие особенности имеют кислотные оксиды, и чем они отличаются от других видов оксидов?
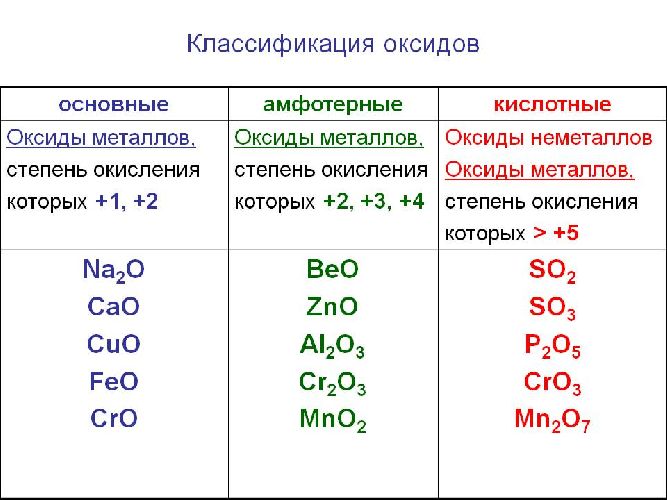
Классификация оксидов
Оксиды делятся на солеобразующие и несолеобразующие. Уже по названию ясно, что несолеобразующие не образуют солей. Таких оксидов немного : это вода H2 O, фторид кислорода OF2 (если условно его считать оксидом), угарный газ, или оксид углерода (II), монооксид углерода CO; оксиды азота (I) и (II): N2 O (оксид диазота, веселящий газ) и NO (монооксид азота).
Солеобразующие оксиды образуют соли при взаимодействии с кислотами или щелочами. В качестве гидроксидов им соответствуют основания, амфотерные основания и кислородосодержащие кислоты. Соответственно они называются основными оксидами (например, CaO), амфотерными оксидами (Al2 O3 ) и кислотными оксидами, или ангидридами кислот (CO2).
Основные свойства кислотных оксидов
Типичными реакциями являются взаимодействие кислотных оксидов с основаниями в результате чего образуется соль и вода:
Все кислотные оксиды, кроме диоксида кремния SiO2 (кремниевый ангидрид, кремнезем), реагируют с водой, образуя кислоты:
Кислотные оксиды образуются при взаимодействии с кислородом простых и сложных веществ (S+O2 =SO2 ), либо при разложении в результате нагревания сложных веществ, содержащих кислород, – кислот, нерастворимых оснований, солей (H2 SiO3 =SiO2 +H2 O).
Список кислотных оксидов:
| Название кислотного оксида | Формула кислотного оксида | Свойства кислотного оксида |
| Оксид серы (IV) | SO2 | бесцветный токсичный газ с резким запахом |
| Оксид серы (VI) | SO3 | легколетучая безцветная токсичная жидкость |
| Оксид углерода (IV) | CO2 | бесцветный газ без запаха |
| Оксид кремния (IV) | SiO2 | бесцветные кристаллы, обладающие прочностью |
| Оксид фосфора (V) | P2 O5 | белый легковозгораемый порошок с неприятным запахом |
| Оксид азота (V) | N2 O5 | вещество, состоящее из бесцветных летучих кристаллов |
| Оксид хлора (VII) | Cl2 O7 | бесцветная маслянистая токсичная жидкость |
| Оксид марганца (VII) | Mn2 O7 | жидкость с металлическим блеском, являющаяся сильным окислителем. |
Что мы узнали?
Кислотные оксиды относятся к солеобразующим оксидам и образуются с помощью кислот. Кислотные оксиды вступают в реакции с основаниями и водой, а их образование происходит при нагревании и разложении сложных веществ.
Кислотные оксиды – список с примерами и формулами
Оксиды – сложные вещества, состоящие из двух элементов, один из которых кислород. В названиях оксидов сначала указывают слово оксид, затем название второго элемента, которым он образован. Какие особенности имеют кислотные оксиды, и чем они отличаются от других видов оксидов?
Классификация оксидов
Оксиды делятся на солеобразующие и несолеобразующие. Уже по названию ясно, что несолеобразующие не образуют солей. Таких оксидов немного : это вода H2 O, фторид кислорода OF2 (если условно его считать оксидом), угарный газ, или оксид углерода (II), монооксид углерода CO; оксиды азота (I) и (II): N2 O (оксид диазота, веселящий газ) и NO (монооксид азота).
Солеобразующие оксиды образуют соли при взаимодействии с кислотами или щелочами. В качестве гидроксидов им соответствуют основания, амфотерные основания и кислородосодержащие кислоты. Соответственно они называются основными оксидами (например, CaO), амфотерными оксидами (Al2 O3 ) и кислотными оксидами, или ангидридами кислот (CO2).
Рис. 1. Виды оксидов.
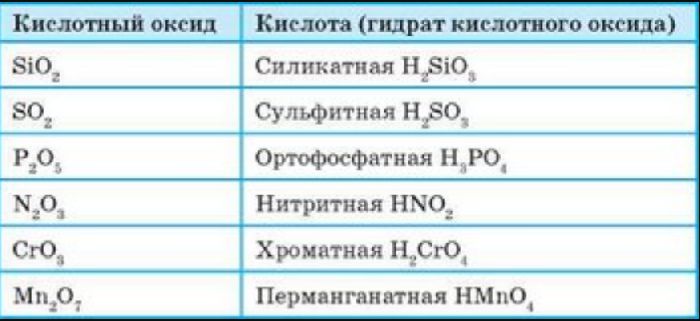
Основные свойства кислотных оксидов
Рис. 2. Кислотные оксиды с соответствующими кислотами.
SO3 (кислотный оксид)+CaO (основной оксид)=СaSO4 (соль);
Типичными реакциями являются взаимодействие кислотных оксидов с основаниями в результате чего образуется соль и вода:
Все кислотные оксиды, кроме диоксида кремния SiO2 (кремниевый ангидрид, кремнезем), реагируют с водой, образуя кислоты:
Кислотные оксиды образуются при взаимодействии с кислородом простых и сложных веществ (S+O2 =SO2 ), либо при разложении в результате нагревания сложных веществ, содержащих кислород, – кислот, нерастворимых оснований, солей (H2 SiO3 =SiO2 +H2 O).
Список кислотных оксидов:
| Название кислотного оксида | Формула кислотного оксида | Свойства кислотного оксида |
| Оксид серы (IV) | SO2 | бесцветный токсичный газ с резким запахом |
| Оксид серы (VI) | SO3 | легколетучая безцветная токсичная жидкость |
| Оксид углерода (IV) | CO2 | бесцветный газ без запаха |
| Оксид кремния (IV) | SiO2 | бесцветные кристаллы, обладающие прочностью |
| Оксид фосфора (V) | P2 O5 | белый легковозгораемый порошок с неприятным запахом |
| Оксид азота (V) | N2 O5 | вещество, состоящее из бесцветных летучих кристаллов |
| Оксид хлора (VII) | Cl2 O7 | бесцветная маслянистая токсичная жидкость |
| Оксид марганца (VII) | Mn2 O7 | жидкость с металлическим блеском, являющаяся сильным окислителем. |
Рис. 3. Примеры кислотные оксиды.
Что мы узнали?
Кислотные оксиды относятся к солеобразующим оксидам и образуются с помощью кислот. Кислотные оксиды вступают в реакции с основаниями и водой, а их образование происходит при нагревании и разложении сложных веществ.
Урок №43. Оксиды: классификация, номенклатура, свойства, получение, применение
Сегодня мы начинаем подробное знакомство с важнейшими классами неорганических соединений. Неорганические вещества по составу делятся, как вы уже знаете, на простые (металлы и неметаллы) и сложные:
А – кислотный остаток
ОН – гидроксильная группа
Сложные неорганические вещества подразделяют на четыре класса: оксиды, кислоты, основания, соли. Мы начинаем с класса оксидов.
ОКСИДЫ
оксид углерода ( II )
оксид марганца (VII )
Классификация оксидов
Все оксиды можно разделить на две группы: солеобразующие (основные, кислотные, амфотерные) и несолеобразующие или безразличные.
4). Несолеобразующие оксиды – это оксиды безразличные к кислотам и основаниям. К ним относятся оксиды неметаллов с валентностью I и II (Например, N 2 O, NO, CO).
Вывод: характер свойств оксидов в первую очередь зависит от валентности элемента.
Например, оксиды хрома:
Классификация по растворимости в воде
Кислотные оксиды
(не растворим в воде)
Основные оксиды
В воде растворяются только оксиды щелочных и щелочноземельных металлов
Амфотерные оксиды
С водой не взаимодействуют.
В воде не растворимы
Выполните задания:
1. Выпишите отдельно химические формулы солеобразующих кислотных и основных оксидов.
Выпишите оксиды и классифицируйте их.
Физические свойства оксидов
Химические свойства оксидов
ХИМИЧЕСКИЕ СВОЙСТВА ОСНОВНЫХ ОКСИДОВ
1. Основной оксид + Кислотный оксид = Соль (р. соединения)
3K 2 O + 2H 3 PO 4 = 2K 3 PO 4 + 3H 2 O
Na 2 O + H 2 O = 2NaOH
ХИМИЧЕСКИЕ СВОЙСТВА КИСЛОТНЫХ ОКСИДОВ
2. Кислотный оксид + Основание = Соль + Н 2 О (р. обмена)
P 2 O 5 + 6KOH = 2K 3 PO 4 + 3H 2 O
3. Основной оксид + Кислотный оксид = Соль (р. соединения)
4. Менее летучие вытесняют более летучие из их солей
CaCO 3 + SiO 2 = CaSiO 3 +CO 2
ХИМИЧЕСКИЕ СВОЙСТВА АМФОТЕРНЫХ ОКСИДОВ
Взаимодействуют как с кислотами, так и со щелочами.
ZnO + 2 HCl = ZnCl 2 + H 2 O
ZnO + 2 NaOH + H 2 O = Na 2 [Zn(OH) 4 ] ( в растворе)
ZnO + 2 NaOH = Na 2 ZnO 2 + H 2 O (при сплавлении)
Применение оксидов
Некоторые оксиды не растворяются в воде, но многие вступают с водой в реакции соединения:
В результате часто получаются очень нужные и полезные соединения. Например, H 2 SO 4 – серная кислота, Са(ОН) 2 – гашеная известь и т.д.
Если оксиды нерастворимы в воде, то люди умело используют и это их свойство. Например, оксид цинка ZnO – вещество белого цвета, поэтому используется для приготовления белой масляной краски (цинковые белила). Поскольку ZnO практически не растворим в воде, то цинковыми белилами можно красить любые поверхности, в том числе и те, которые подвергаются воздействию атмосферных осадков. Нерастворимость и неядовитость позволяют использовать этот оксид при изготовлении косметических кремов, пудры. Фармацевты делают из него вяжущий и подсушивающий порошок для наружного применения.
Такими же ценными свойствами обладает оксид титана (IV) – TiO 2 . Он тоже имеет красивый белый цвет и применяется для изготовления титановых белил. TiO 2 не растворяется не только в воде, но и в кислотах, поэтому покрытия из этого оксида особенно устойчивы. Этот оксид добавляют в пластмассу для придания ей белого цвета. Он входит в состав эмалей для металлической и керамической посуды.
Оксид хрома (III) – Cr 2 O 3 – очень прочные кристаллы темно-зеленого цвета, не растворимые в воде. Cr 2 O 3 используют как пигмент (краску) при изготовлении декоративного зеленого стекла и керамики. Известная многим паста ГОИ (сокращение от наименования “Государственный оптический институт”) применяется для шлифовки и полировки оптики, металлических изделий, в ювелирном деле.
Свойства кислотных оксидов
Получение оксидов в химии
Любой оксид можно получить несколькими способами.
Получение оксида окислением простых веществ. Реакции на примере металлов и неметаллов:
Получение оксида окислением сложных веществ. Реакции на примере бинарных и водородных соединений:
Бинарные соединения
Оксиды можно получить, когда разлагаются вещества, такие как соли, основания и кислоты:
Получение оксида окислением кислорода и озона:
Видео
Взаимодействие оксидов с кислотами
С кислотами реагируют основные и амфотерные оксиды. При этом образуются соли и вода:
Несолеобразующие оксиды не реагируют с кислотами вообще, а кислотные оксиды не реагируют с кислотами в большинстве случаев.
Когда все-таки кислотный оксид реагирует с кислотой?
Решая часть ЕГЭ с вариантами ответа, вы должны условно считать, что кислотные оксиды не реагируют ни с кислотными оксидами, ни с кислотами, за исключением следующих случаев:
1) диоксид кремния, будучи кислотным оксидом, реагирует с плавиковой кислотой, растворяясь в ней. В частности, благодаря этой реакции в плавиковой кислоте можно растворить стекло. В случае избытка HF уравнение реакции имеет вид:
а в случае недостатка HF:
2) SO2, будучи кислотным оксидом, легко реагирует с сероводородной кислотой H2S по типу сопропорционирования:
3) Оксид фосфора (III) P2O3 может реагировать с кислотами-окислителями, к которым относятся концентрированная серная кислота и азотная кислота любой концентрации. При этом степень окисления фосфора повышается от значения +3 до +5:
| P2O3 | + | 2H2SO4 | + | H2O | =t o => | 2SO2 | + | 2H3PO4 |
| (конц.) |
| 3P2O3 | + | 4HNO3 | + | 7H2O | =t o => | 4NO↑ | + | 6H3PO4 |
| (разб.) |
| P2O3 | + | 4HNO3 | + | H2O | =t o => | 2H3PO4 | + | 4NO2↑ |
| (конц.) |
4) Оксид серы (IV) SO2 может быть окислен азотной кислотой, взятой в любой концентрации. При этом степень окисления серы повышается с +4 до +6.
| 2HNO3 | + | SO2 | =t o => | H2SO4 | + | 2NO2↑ |
| (конц.) |
| 2HNO3 | + | 3SO2 | + | 2H2O | =t o => | 3H2SO4 | + | 2NO↑ |
| (разб.) |
Взаимодействие с водой
Все кислотные остатки при взаимодействии с водой создают соответствующую кислоту. При этом для ангидридов сильных кислот реакция будет необратимой. А неустойчивые оксиды реагируют с водой обратимо, и равновесие реакции смещено в сторону реагентов.
Исключением является оксид кремния, так как кремниевая кислота нерастворима в воде.
Химические свойства
Окислительно-восстановительные свойства
Чаще всего кислотные ангидриды проявляют окислительные свойства, принимая электроны. Это присуще тем соединениям, где атом неметалла находится в высшей степени окисления. Однако вещества с промежуточными зарядами также способны выступить в роли окислителей.
Но чаще всего атомы с промежуточной степенью окисления проявляют восстановительные свойства. Они отдают электроны и увеличивают свой заряд до максимального значения. Или до ближайшего устойчивого состояния.
В таблице Менделеева для элементов, стоящих в одном периоде, кислотные свойства увеличиваются с ростом номера группы. А для атомов одной группы с ростом номера периода будет происходить уменьшение способности отдавать электроны.
Оксиды азота
Азот — газ, который образует 5 различных соединений с кислородом — 5 оксидов азота. А именно:
— N2O — гемиоксид азота. Другое его название известно в медицине под названием веселящий газ или закись азота — это бесцветный сладковатый и приятный на вкус на газ. — NO — моноксид азота — бесцветный, не имеющий ни запаха ни вкуса газ. — N2O3 — азотистый ангидрид — бесцветное кристаллическое вещество — NO2 — диоксид азота. Другое его название — бурый газ — газ действительно имеет буро-коричневый цвет — N2O5 — азотный ангидрид — синяя жидкость, кипящая при температуре 3,5 C
Из всех этих перечисленных соединений азота наибольший интерес в промышленности представляют NO — моноксид азота и NO2 — диоксид азота. Моноксид азота (NO) и закись азота N2O не реагируют ни с водой, ни с щелочами. Азотистый ангидрид (N2O3) при реакции с водой образует слабую и неустойчивую азотистую кислоту HNO2, которая на воздухе постепенно переходит в более стойкое химическое вещество азотную кислоту Рассмотрим некоторые химические свойства оксидов азота:
2NO2 + H2O→ HNO3 + HNO2 — образуется сразу 2 кислоты: азотная кислота HNO3 и азотистая кислота.
2NO2 + 2NaOH→ NaNO3 + NaNO2 + H2O — образуются две соли: нитрат натрия NaNO3 (или натриевая селитра) и нитрит натрия (соль азотистой кислоты).
2NO2 + Na2CO3→ NaNO3 + NaNO2 + CO2 — образуются образуются две соли: нитрат натрия и нитрит натрия, и выделяется углекислый газ.
Получают диоксид азота (NO2) из моноксида азота (NO) с помощью химической реакции соединения c кислородом:
Кислоты
Кислоты — это сложные вещества, в состав молекул которых входит активный атом водорода и кислотный остаток. Этот активный атом водорода в химических реакциях способен замещаться на атом металла, в результате чего всегда получается соль.
В формулах неорганических кислот этот атом водорода записывается на первом месте*:
* В химических формулах органических кислот атом водорода стоит в конце, например, CH3–COOH уксусная кислота
В состав любой кислоты кроме атомов водорода входит кислотный остаток. Кислотный остаток — это часть молекулы кислоты без атомов водорода (которые могут быть замещены на атом металла). Валентность кислотного остатка равна числу таких атомов водорода:
При определении валентности кислотного остатка учитываются те атомы водорода, которые участвовали в реакции или могут участвовать в ней. Так, фосфорной кислоте Н3РО4, в зависимости от условий, могут соответствовать кислотные остатки иного состава:
У органических кислот не все атомы водорода в молекуле способны замещаться на атом металла:
Задание 2.13. Определите состав и валентность кислотных остатков для кислот, учитывая, что все атомы водорода кислот участвуют в реакции:
По числу атомов водорода кислоты делят на одноосновные и многоосновные:
По составу кислоты делят на:
Бескислородные кислоты представляют собой растворы некоторых газов в воде, при этом и растворённому газу, и полученному раствору приписывают одинаковые свойства, хотя это не так. Например, из простых веществ водорода и хлора получается газ хлороводород:
Этот газ не проявляет кислотных свойств, если он сухой: его можно перевозить в металлических ёмкостях, и никакой реакции не происходит. Но при растворении хлороводорода в воде получается раствор, который проявляет свойства сильной кислоты, её перевозить в металлических ёмкостях нельзя! Этот раствор называется «соляная кислота».
Названия бескислородных кислот составляют по принципу:
«ЭЛЕМЕНТ» + «ВОДОРОД»ная кислота
Кислородсодержащие кислоты могут быть получены при действии воды на кислотные оксиды (см. задание 2.6). Исходные кислотные оксиды называются «АНГИДРИДЫ кислот»:
Метафосфорная кислота неустойчива и, присоединяя воду, превращается в более устойчивую кислоту:
или в суммарном виде:
Таким образом, Р2O5 — ангидрид фосфорной кислоты, а также некоторых других, менее устойчивых кислот.
Обратите внимание! Название кислородосодержащей кислоты содержит в виде корня название элемента, входящего в состав ангидрида:
Если элементу соответствуют несколько кислот, то для кислоты с большей валентностью элемента, входящего в состав ангидрида, в названии употребляют суффикс «Н» или «В». Для кислот с меньшей валентностью элемента в названиях добавляют еще один суффикс «ИСТ».
Валентность элемента проще всего определять по формуле ангидрида:
Сведём всё известное о названиях кислот в таблицу 4.
Задание 2.14. Заполнить табл. 4, заменив знаки вопросов формулами и названиями соответствующих кислот.
Задание 2.15. Напишите НА ПАМЯТЬ формулы кислот: кремниевой, сернистой, серной, сероводородной, азотистой, азотной, соляной, фосфорной, угольной. Укажите ангидриды этих кислот (там, где они существуют).
Свойства кислот
Главным свойством всех кислот является их способность образовывать соли. Соли образуются в любой реакции, в которой участвует кислота, при этом замещаются активные атомы водорода (один, все или несколько).
1. Кислоты реагируют с металлами, при этом атом водорода кислоты замещается на атом металла — в результате образуется растворимая соль* и водород:
* Если образуется нерастворимая соль, то эта соль закрывает поверхность металла и реакция останавливается.
Не все металлы способны вытеснять водород из растворов кислот: этот процесс возможен только для тех металлов, которые стоят в ряду напряжений ДО водорода (рис. 3 или таблица 3).
Задание 2.16. Составьте уравнения возможных реакций:
При составлении уравнений пользуйтесь рядом напряжений и схемой реакции:
кислота + металл (до водорода) → соль + водород
Не забывайте, составляя формулы солей, учитывать валентность металла и кислотного остатка.
Некоторые кислоты могут растворять металлы, которые стоят в ряду напряжения после водорода, но водород при этом не выделяется:
2. Кислоты реагируют с основаниями, образуя соль и воду*. Это реакция обмена, и поэтому валентность составных частей в результате реакции не меняется:
* Реакция между кислотой и основанием называется реакцией нейтрализации.
Задание 2.17. Составьте аналогичные уравнения реакций по схеме:
кислота + основание → соль + вода
3. Кислоты могут реагировать с солями. При этом сильная кислота вытесняет более слабую из её соли.
Происходит реакция обмена: образуется новая соль и новая кислота.
Более подробно о подобных реакциях см. в уроке 6.
Задание 2.18. Составьте НА ПАМЯТЬ формулы: а) сильных, б) слабых кислот.
Задание 2.19. Составьте уравнения реакций по схеме:
(более сильная) кислота + соль → соль + кислота (более слабая):
4. И, наконец, выяснив свойства кислот, зададим себе вопрос: а можно ли обнаружить кислоту в растворе? Например, в одном стакане налита вода, а в другом — раствор кислоты. Как определить, где кислота? Хотя многие кислоты кислые на вкус, пробовать их НЕЛЬЗЯ — это опасно! Выручают особые вещества — ИНДИКАТОРЫ. Это соединения, которые изменяют цвет в присутствии кислот:
Выводы
Кислоты обнаруживаются индикаторами в кислой («красной») области.
























