Чем опасна вакцинация от коронавируса
Что известно о COVID-19?
Это РНК-содержащий вирус животного происхождения, относящийся к группе коронавирусов. Согласно данным ВОЗ, он передается от заболевшего человека через мелкие капли, которые выделяются при чихании и кашле из носа и рта. С момента заражения до появления первых симптомов проходит от 1 до 14 дней (в среднем – 7). Носитель вируса еще не знает о своей болезни, но в плане заражения уже представляет опасность для окружающих. По информации коронавирусной эпидемиологии, COVID-19 в 2-3 раза заразнее гриппа, но в 2-3 раза менее заразен, чем корь.
При легком течении болезни ее симптомы сходны с ОРВИ и заканчиваются выздоровлением через 14 дней без каких-либо дальнейших последствий. В тяжелых случаях COVID продолжается до 8 недель. Даже при отсутствии выраженных признаков заболевания у переболевших формируется иммунитет. Но учитывая, пусть и нечастые случаи повторного заражения, сохраняется он не слишком долго. Гораздо большим эффектом обладает вакцина.
Как действует вакцина?
Сегодня в мире используется несколько иммунопрепаратов, разработанных специалистами разных стран и прошедших необходимые клинические испытания. Все они предназначены для формирования иммунитета к возбудителю. После их введения иммунная система:
У человека, прошедшего вакцинацию, формируется стойкий иммунитет к COVID.
Опасна ли вакцинация?
Каждый человек реагирует на иммунопрепарат индивидуально. Поэтому даже самая качественная вакцина может вызвать побочные эффекты. Их появление на непродолжительное время – единственная опасность.
Чем опасна вакцинация от коронавируса:
Эти неприятные симптомы исчезают в течение нескольких дней.
Тяжелые состояния после введения иммунопрепарата могут развиваться у людей, имеющих противопоказания. Нельзя проводить вакцинацию, если наблюдаются:
При этих патологиях прививка может спровоцировать обострение.
Также противопоказанием является возраст (младше 18 и старше 65 лет), беременность, недавно перенесенная тяжелая форма коронавирусной инфекции. У переболевших людей в первое время после выздоровления отмечается высокий уровень антител, а вакцина повысит его еще больше. Последствия могут проявиться бурной иммунной реакцией в форме цитокинового шторма.
Как уменьшить негативные проявления?
Снизить развитие побочных явлений поможет соблюдение всех рекомендаций врача. Чтобы уменьшить риск развития негативных симптомов после вакцинации, нужно:
При отсутствии противопоказаний и соблюдении всех требований, риск побочных эффектов сводится к минимуму.
После прививки от коронавируса врачи советуют соблюдать щадящий режим и выпивать не менее 1,5 литров жидкости в день. При повышении температуры рекомендуется принять жаропонижающее средство. Если слабость не проходит в течение нескольких дней, появились аллергические реакции, нужно немедленно обратиться к доктору.
Когда будет массовая вакцинация?
Массовая вакцинация в США, Канаде и европейских странах началась еще в декабре прошлого года. В это же время стартовала она и в России. Но на начальном этапе мероприятие проводилось только для определенной категории лиц – молодых людей и тех, кто по роду своей профессиональной деятельности не может ограничить число контактов. Сегодня привиться от ковида можно в любом регионе страны.
Какими бывают вакцины от COVID-19 и как они защищают нас от инфекции, «Доктору Питеру» рассказала заместитель управляющего по качеству НИЦ «Эко-безопасность», инфекционист, клинический фармаколог Гульнара Ислямовна Сыраева.
Такой разный иммунитет
Смысл любой вакцинации – так или иначе воздействовать на иммунную систему. Изначально понятие «иммунитет» подразумевало только способность организма противостоять внешним инородным агентам: бактериям, вирусам, простейшим. Потом оно стало шире. В современном понимании – это сложная, многогранная система, которая направлена в том числе на поддержание внутренней целостности и слаженной работы организма. В свое время Илья Мечников и Пауль Эрлих получили Нобелевскую премию за открытие иммунитета. Мечников разработал теорию клеточного иммунитета, Эрлих — гуморального. На момент своих разработок ученые друг друга критиковали, но в итоге жизнь показала, что они оба были правы. На сегодня две их теории не исключают, а дополняют друг друга. За клеточный иммунитет отвечают так называемые Т-клетки, которые поглощают чужеродные микроорганизмы, а также презентируют их — они носят на себе их фрагменты и показывают другим клеткам, после чего запускается выработка антител — специальных белковых комплексов в крови (иммуноглобулины IgА, IgМ, IgG), которые нейтрализуют и поглощают чужеродные микроорганизмы. Антитела отвечают за гуморальный иммунитет.
Любое вещество, которое организм человека воспринимает как чужеродное и потенциально опасное для себя, называется антигеном. Новый коронавирус SARS-CoV-2 относится к РНК-содержащим вирусам, и антигеном может быть как внутренняя его часть (нуклеиновые кислоты), так и внешняя (поверхностная оболочка, которая представлена сложными полипептидами – белками).
Помимо того, что иммунитет бывает клеточным и гуморальным, он подразделяется еще на естественный или искусственный.
Естественный иммунитет, в свою очередь, бывает врожденным (как выяснилось, у человека нет врожденного, генетически обусловленного иммунитета к новой коронавирусной инфекции) или приобретенным (он формируется после перенесенной болезни, в некоторых случаях даже на всю жизнь, как после ветрянки).
Искусственный иммунитет бывает активным и пассивным. Если человек уже болеет, у него вырабатываются антитела, но их недостаточно для выздоровления, тогда речь идет о необходимости пассивного иммунитета. Это не что иное, как переливание плазмы крови уже переболевших. Так происходит, например, при заражении клещевым энцефалитом: человеку в течение 72 часов вводят специальные противоклещевые иммуноглобулины. Вакцинация помогает создать активный искусственный иммунитет. Мы вводим человеку вакцину, в которой есть антигены, — на них организм начинает формировать иммунный ответ, но при этом они не вызывают заболевания.
В зависимости от использованных антигенов и принципа создания вакцины делятся на несколько видов. Расскажу об основных из них.
Векторные рекомбинантные вакцины. «Спутник V», «Конвидеция»
К плюсам векторных вакцин можно отнести высокую иммуногенность — при их введении формируется достаточно высокий титр защитных антител. По сути, это самые современные технологии создания вакцин — генная инженерия в чистом виде. Но как раз в ее новизне кроется и минус — они применялись на небольшом проценте популяции и еще мало изучены. Мы пока не можем говорить о долгоиграющих перспективах — сформируется ли пожизненный иммунитет? Или что будет, если вирус мутирует и ген, который использовали в создании вакцины, «в природе» немного изменит свою кодировку — состыкуется ли с ним антительный ответ после вакцинации? Кроме того, при введении такой вакцины организм может также отреагировать на вирус-вектор, что помешает главной цели – формированию стойкого иммунитета против целевого вируса. Именно поэтому для вектора важно выбрать оптимальный вариант — тот, на который реакция организма будет минимальной.
К векторным относится первая российская вакцина против коронавируса «Спутник V», разработанная НИЦ эпидемиологии и микробиологии им. Гамалеи. Разработчики «Спутник V» встроили ген, кодирующий информацию о структуре S-белка шипа коронавируса — он формирует всем известную «корону» и отвечает за связывание вируса с клетками человека. В качестве вектора они использовали давно и хорошо изученный аденовирус, который вызывает сезонную ОРВИ. Над векторными вакцинами трудятся и другие разработчики. В частности, регистрируемая китайская вакцина «Конвидеция» тоже векторная и тоже на основе аденовируса. Заявку на ее регистрацию подала биофармацевтическая компания «Петровакс» (входит в холдинг «Интеррос» Владимира Потанина). Сейчас она проходит 3-ю фазу клинического исследования, в которой только наш центр задействует 300 добровольцев из Петербурга.
До «Спутника V» в России в широкой клинической практике векторные вакцины не применялись. В 2015 году была зарегистрирована подобная вакцина против лихорадки Эбола, разработанная тем же Центром им. Гамалеи. Векторная вакцина против другой разновидности коронавируса – ближневосточного респираторного синдрома (MERS) – еще одна разработка Центра им. Гамалеи с использованием вектора на основе аденовируса, но она пока не зарегистрирована.
Есть еще одна разновидность генно-инженерных вакцин последнего поколения — на основе нуклеиновых кислот (ДНК- и РНК-вакцины). В них также используются модификации генетического материала, но, в отличие от векторных вакцин, этот материал синтезируют искусственно. Иначе говоря, собирают необходимую нуклеиновую последовательность в лаборатории и с ней работают. Это технология завтрашнего дня — пока в России нет ни одной такой вакцины, испытанной на людях.
Цельновирионные вакцины
На цельновирионных вакцинах человечество выросло — это классика. Для создания таких вакцин вирус используется целиком, а не какая-то его часть. Они бывают живыми ослабленными или инактивированными (в них вирус «убит» термически либо воздействием химических агентов, например, с помощью формалина или ацетона).
Для приготовления инактивированных вакцин используется большой спектр возбудителей — бактерий и вирусов. Такие вакцины защищают нас от бешенства (антирабическая), коклюша, гепатита А, гриппа, клещевого энцефалита, брюшного тифа.
Цельновирионную инактивированную вакцину против коронавируса, к примеру, разработал Научный центр им. Чумакова (по словам президента Путина, она уже «на подходе»). Сейчас она проходит стадию клинического исследования. 19 октября на базе научно-исследовательского центра «Эко-безопасность» стартовал второй этап — в нем участвуют 30 добровольцев. Чтобы «подхлестнуть» иммунитет и повысить уровень антител, вакцину вводят двукратно – с разницей в 10 дней. Кстати, дважды вводят и «Спутник V».
Для цельновирионных вакцин с живым, но ослабленным вирусом обычно достаточно одного введения. В них вирус сохраняет возможность размножаться в организме человека. Такие препараты нуждаются в регулярном изучении генетической стабильности, чтобы не вызвать заболевания при иммунизации. Бывают, к примеру, живые вакцины против кори, полиомиелита, гриппа, но их сейчас практически не применяют.
Субъединичные вакцины. «ЭпиВакКорона»
Такие препараты создаются на основе различных антигенных компонентов – субъединиц. Можно взять, к примеру, часть оболочки вируса — белки, которые отвечают за проникновение вируса в клетку. У коронавируса это S-белок. И хотя антитела при введении такой вакцины будут вырабатываться непосредственно на белок, уровень иммунного ответа и качество защитных антител, скорее всего, будет ниже, чем на векторную или цельновирионную вакцины. На целый вирус или кусочек генома вырабатываются более сложные по структуре антитела, чем на изолированный белок. Но надо понимать, что, говоря «белок», мы немного утрируем — там может использоваться много структур, включая поверхностную и внутреннюю мембрану, белки-носители и так далее.
В чем минусы таких вакцин? Поверхностный белок может со временем мутировать, и будет ли вакцина эффективна, скажем, через год — вопрос. Для усиления иммунного ответа в них так же, как и в цельвирионных, используются адъюванты. Плюс же в том, что субъединичные вакцины проще в производстве, чем, например, векторные.
К субъединичным относятся вакцины против пневмококковой и менингококковой инфекций, брюшного и сыпного тифа, холеры.
Вакцины на основе вирусоподобных частиц
Для производства этих вакцин берут пустую белковую оболочку вируса – без «нутра». Вирусоподобные частицы имитируют структуру вируса, но не содержат его генетического материала. В их состав также могут входить адъюванты и иммуностимуляторы.
Из плюсов. Они безопасны и способны вырабатывать высокий иммунный ответ, при этом эффективны даже в виде капель для носа – так они сразу активируют иммунитет слизистых оболочек, которые обычно становятся «входными воротами» для вирусов. В то же время такие вакцины технологически сложны для массового производства и требуют больших финансовых вложений. Опять же, даже при незначительной мутации вируса поверхностный белок может поменять свою конфигурацию, и тогда вакцина попросту может не сработать.
На сегодня такие вакцины созданы для профилактики гриппа, гепатита С.
Виды вакцин от COVID-19: какую выбрать
Оглавление
Сегодня поставить прививку от можно с использованием нескольких препаратов. Какие виды вакцин от ковида применяются в нашей стране? Чем они отличаются друг от друга? Какие прививки ставят в других странах? Давайте разберемся в этих вопросах.
Российские типы вакцин от ковида
В нашей стране в настоящий момент используются исключительно отечественные препараты.
Они разделяются на несколько групп:
Рассмотрим все вакцины от коронавируса более внимательно, определим их виды и отличия.
«Спутник V» (от Исследовательского центра имени )
Препарат создан на основе аденовируса (вируса, вызывающего ОРВИ) человека. Для разработки вакцины вирус лишили гена размножения. Благодаря этому он стал так называемым вектором (транспортным средством для доставки груза в клетки организма). В качестве груза в данном конкретном случае выступает генетический материал заболевания, против которого и работает препарат. Поступая в клетку, груз стимулирует выработку антител.
Важно! После введения первой дозы препарата организм человека от заражения еще не защищен. Это обусловлено тем, что антитела вырабатываются постепенно. Максимальный их уровень обеспечивается примерно через 2–3 недели после постановки второй прививки.
Иммунитет после вакцинации сохраняется примерно 2 года. При этом важно понимать, что антитела в крови присутствуют определенное количество времени, которое во многом зависит от индивидуальных особенностей пациента. В настоящий момент говорят о том, что хватает их примерно на год. При этом клеточный иммунитет сохраняется. Он защищает организм и после исчезновения антител.
«Спутник Лайт» (однокомпонентный вариант вакцины «Спутник V»)
Этот препарат отличается от исходного тем, что достаточно введения одной его дозы.
«ЭпиВакКорона» (от Центра «Вектор»)
Данная вакцина разработана на основе искусственно созданных фрагментов белков вируса. Благодаря этому она дает минимальное количество побочных эффектов. К основным относят возможную болезненность в месте инъекции и незначительное повышение температуры тела на короткое время. При этом и эффективность препарата является более низкой, чем у вакцины «Спутник V». Для повышения данного показателя проводится двукратная вакцинация с интервалом в 2–3 недели. На формирование иммунитета уходит около 30 дней. Ревакцинация по предварительным оценкам требуется примерно через 6–9 месяцев.
Разработчики уверяют, что препарат может обеспечить защиту организма от различных штаммов коронавируса. Но существует и другое мнение. Некоторые специалисты утверждают, что вакцина уязвима при мутациях вируса.
Иностранные виды вакцин от коронавируса
К ним относят: Pfizer/BioNTech и Moderna. Вирусные белки для производства препаратов синтезируются непосредственно в организме человека. Матричная РНК представляет собой своеобразную инструкцию. Прочитав ее, клетка начинает самостоятельно вырабатывать закодированный белок (фрагмент коронавируса). Препараты Pfizer/BioNTech и Moderna сегодня применяются для вакцинации в Великобритании, Израиле, странах Евросоюза, на Украине, в США и в других государствах. Прививки демонстрируют хорошую защиту от тяжелого течения заболевания. Это обусловлено тем, что вакцины проникают вглубь клеток, что имитирует инфицирование и приводит к формированию полноценного иммунитета. Недостатком препаратов является их недостаточная изученность.
Таким средством является вакцина AstraZeneca. Изготовлена она по принципу препарата «Спутник V». В качестве вектора в AstraZeneca выступает модифицированный вирус шимпанзе. Эффективность этой вакцины составляет 79%. При этом препарат на 100% защищает от тяжелого течения вирусной инфекции. Он используется в странах Евросоюза.
К ним относят Sinopharm и Sinovac.
Основными крупными поставщиками вакцин стали биофармацевтические компании из Китая. Они разработали препараты по принципу российского препарата «КовиВак». Вакцинация Sinopharm и Sinovac проводится не только в КНР, но и в Турции, ОАЭ, Чили, Аргентине и ряде других стран. Во время третьей фазы исследований определена общая эффективность препаратов, которая варьируется от 50% до 84%. При этом от тяжелого течения заболевания средства защищают на 100%.
Сравнение российских препаратов
Для правильного выбора прививки от коронавируса нужно сравнить между собой представленные препараты. Мы провели такое сравнение и оформили его в виде таблицы для вашего удобства.
| «Спутник V» | «Спутник Лайт» | «Кови Вак» | «Эпи Вак Корона» | |
|---|---|---|---|---|
| Срок формирования иммунитета (в днях) | 42 | 28 | Исследуется | 35-40 |
| Формирование антител (в процентах от вакцинированных) | У 98% | Почти у 97% | Исследуется | Более чем у 82% |
| Эффективность | Более 91% (в том числе для пациентов старше 65 лет) | Почти 80% | На стадии исследований | В настоящий момент не установлена |
Побочные эффекты вакцин
Необходимо сразу уточнить, что все побочные эффекты легкого и умеренного типов являются вариантом нормы.
В некоторых случаях также возможно развитие диареи.
После введения препарата пациент на 20–30 минут остается в медицинском учреждении. Это необходимо по причине риска развития аллергической реакции.
Преимущества обращения в МЕДСИ
Опубликованы первые данные по инактивированной вакцине против COVID-19 «КовиВак»
Вступление
Продолжающаяся в настоящее время пандемия новой коронавирусной инфекции 2019 года (COVID-19), вызванная коронавирусом 2 тяжелого острого респираторного синдрома SARS-CoV-2, унесла более 4 миллионов жизней (по данным на март 2021 года [1, 2]), и необходимость быстрого внедрения безопасных и эффективных вакцин против данного вируса остается очень высокой. Беспрецедентное в новейшей истории повсеместное распространение пандемии требует применения всех существующих вакцинных платформ, чтобы в конечном счете обеспечить доступность вакцин против SARS-CoV-2 для жителей каждой страны мира.
SARS-CoV-2 относится к подроду Sarbecovirus рода Betacoronavirus и семейству Coronaviridae [3]; в качестве основного рецептора для проникновения в клетки человека вирус использует ангиотензинпревращающий фермент 2 (АПФ2) [4, 5]. Диаметр заключенного в оболочку вириона SARS-CoV-2 составляет 100–150 нм; сам вирион имеет сферическую форму. В нем содержится несколько структурных белков: шипиковый гликопротеин (S), мембранный белок (M), белок оболочки (E), расположенный на поверхности, и белок нуклеокапсида (N), который связан с РНК внутри вирусной частицы. S-белок представляет собой трансмембранный белок слияния I типа, который во время синтеза подвергается значительному гликозилированию; протеаза хозяина расщепляет его на два фрагмента — S1 и S2. Фрагмент S1 содержит рецептор-связывающий домен (РСД), который взаимодействует с рецептором клетки хозяина (т.е. АПФ2). Фрагмент S2 необходим для слияния мембран после еще одного расщепления протеазами клетки хозяина и дальнейших структурных перестроек [6]. Благодаря этим свойствам шипиковый белок и его РСД являются основными мишенями для нейтрализующих антител организма хозяина (НАт) в процессе развития иммунного ответа [7].
Иммунный ответ на инфекцию SARS-CoV-2 активно изучается с целью разработки и улучшения как диагностики заболевания, так и создания и совершенствования вакцин. Как было выявлено в ходе экспериментов, титры НАт являются одними из основных маркеров защиты от SARS-CoV-2, поскольку адоптивный перенос очищенных IgG, которые были получены от выздоравливающих макак-резусов, дозозависимо способствовал формированию иммунной защиты от заражения SARS-CoV-2 у наивных макак-реципиентов [8]. Легкая или средняя степень тяжести течения COVID-19 приводит к выработке НАт, концентрация которых коррелирует с титрами IgG к РСД, определенными методом ELISA; данные титры НАт сохраняются примерно от двух-трех [9, 10] до пяти месяцев [11]. Учитывая возможность снижения концентраций антител после заражения, пристально исследуется более трудный для изучения клеточный компонент иммунитета.
Для разработки вакцин против COVID-19 тестируются многочисленные методы. В настоящее время наиболее часто применяются инактивированные вирусные векторные вакцины, вакцины на основе нуклеиновых кислот (РНК, ДНК) и белковые (субъединичные, вирусоподобные (ВПВ)) вакцины [12]. В качестве основных антигенов, вызывающих синтез НАт, в большинстве вакцин используются S-белок и РСД. Различные передовые технологии разработки вакцин уже продемонстрировали свой потенциал в плане предотвращения развития COVID-19, и несколько таких препаратов, таких как вакцины на основе мРНК и аденовирусные векторные вакцины, после успешного завершения клинических испытаний были одобрены для использования по всему миру [13, 14]. Тем не менее, разработка инактивированных вакцин как более традиционный метод является надежным и экономичным способом, имеющим долгую и успешную историю применения [15, 16]. В Центре Чумакова на культуре клеток Vero были успешно разработаны две инактивированные вакцины против клещевого энцефалита и полиомиелита [22, 23]. Таким образом, вакцина против COVID-19 создавалась на основе ранее отработанной платформы для культивирования клеток с использованием уже отлаженных методов.
Во всем мире разрабатывается несколько инактивированных вакцин против инфекции SARS-CoV-2, и по крайней мере пять из них успешно прошли доклинические и клинические испытания, и их применение было одобрено [17–20]. Тем не менее, несмотря на множество высококачественных публикаций о клинических испытаниях различных вакцин, подробных сведений об общей токсичности, репродуктивной токсичности, профилактической эффективности, иммуногенности и устойчивости иммунного ответа на животных моделях крайне мало.
В данной работе авторы провели оценку безопасности, иммуногенности и устойчивости иммунного ответа на вакцину «КовиВак», созданную на основе цельного вириона, инактивированного β-пропиолактоном, у грызунов и нечеловеческих приматов. У исследованных видов животных не было обнаружено признаков острой/хронической, репродуктивной, эмбрио- и фетотоксичности, тератогенного действия, а также аллергенных свойств. Вакцина привела к формированию стабильного и сильного гуморального иммунного ответа как в виде специфических IgG к SARS-CoV-2, так и НАт у мышей линии BALB/c, сирийских хомячков и обыкновенных игрунок. В течение года титры НАт существенно не снизились. Профилактическая эффективность вакцины изучалась на сирийских хомячках. Надежность производственного процесса была продемонстрирована путем оценки четырех партий вакцины и сравнения их иммуногенных свойств на мышах.
Результаты
Производство и описание вакцины
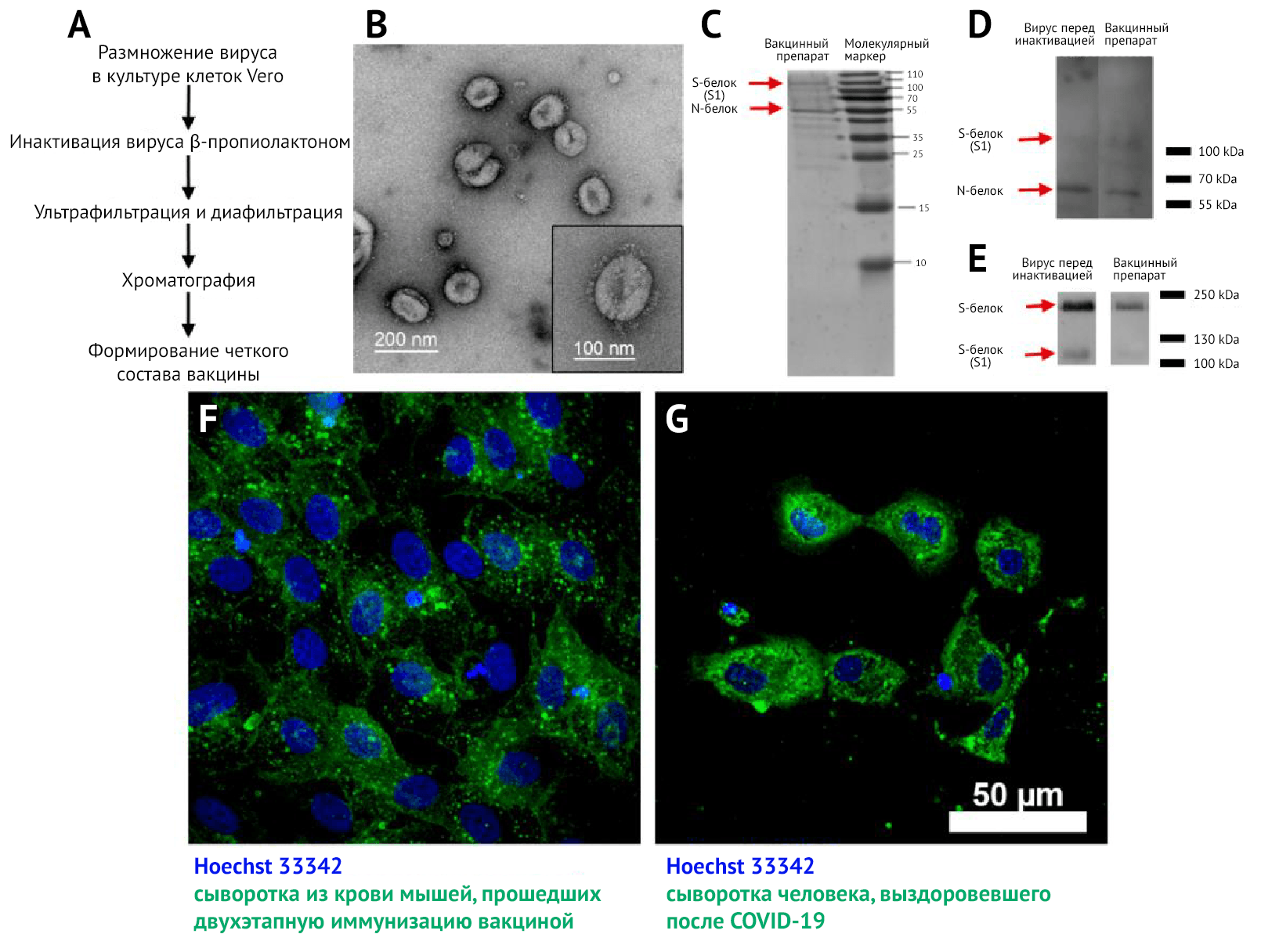
Ранее был представлен процесс выделения и генетического описания вакцинного штамма AYDAR-1 [21]. Вирус удалось профильтровать на третьем пассаже и дополнительно очистить путем разбавления. Были созданы первичные, основные и рабочие посевные серии штамма (а именно пассажи под номерами 7, 8 и 9), которые были охарактеризованы в соответствии с национальными руководствами по производству вакцин.
Благодаря трансмиссионной электронной микроскопии (ТЭМ) (рис. 1B) с негативным контрастированием концентратов были обнаружены плеоморфные сферические вирусные частицы диаметром около 120 нм, покрытые шиповидными структурами длиной 16–20 нм.
Методом ТЭМ (рис. 1B) были подтверждены гомогенность и чистота вакцинного препарата и выявлены вирионы с шипиковыми белками, соотносящиеся по форме и размеру с таковыми, выявляемыми в других исследованиях [26, 27].
В ходе электрофореза SDS-PAGE и вестерн-блоттинга (ВБ) концентратов вакцин перед инактивацией и после хроматографии, окрашенных сыворотками реконвалесцентов после COVID-19 (рис. 1 C и D), были выявлены два основных белка в концентратах: N и S, которые должны содержаться и в препарате вириона. С помощью окрашивания сывороткой анти-S-белка (рис. 1E) были обнаружены две формы S-белка в вирусных препаратах до и после инактивации: S1 и полноразмерный S-белок. Это свидетельствует о том, что в вакцинном препарате присутствует антиген-мишень для индукции синтеза НАт.
Специфичность реактивности антител подтверждается отсутствием свечения (флуоресценции) в неинфицированных клетках культуры Vero.
Изучение эмбрио-, фетотоксичности и тератогенных эффектов в антенатальном и постнатальном периодах развития
Беременные крысы линии Wistar (N = 60) были случайным образом распределены в три группы и иммунизированы внутримышечно на 2, 9 и 16 дни беременности. Крысам из первой исследуемой группы вводили одну дозу вакцины (6 мкг/доза; 0,5 мл), из второй — двойную дозу (12 мкг/доза; 1,0 мл), а из третьей контрольной группы — двойную дозу плацебо (1,0 мл). Ежедневно проводилось измерение массы тела и общего физического состояния животных; на поздних сроках беременности с помощью теста «открытое поле» оценивалась исследовательская активность и состояние самок. Прибавка в весе у самок проходила нормально; летальных исходов или признаков интоксикации не наблюдалось. Ни в одной из исследуемых групп не было признаков преждевременных или трудных родов. В тесте «открытое поле» на 18-е сутки беременности все самки крыс продемонстрировали преимущественно сбалансированный тип поведения с умеренной двигательной и поисковой активностью без признаков беспокойства.
Половину (N = 10 из каждой группы) животных в каждой группе умерщвляли на 20-й день беременности. Статистически значимых различий между исследуемыми группами по количеству желтых тел в яичниках, местах имплантации в матке, живым и мертвым плодам не было. Плоды сформировались нормально, топография всех исследованных органов была в пределах анатомической нормы, гистологическое строение соответствовало возрасту эмбрионов, развитие костей было нормальным. Патологических изменений органов и тканей обнаружено не было.
Другая половина (N = 10 из каждой группы) животных в каждой из трех групп вакцинированных была использована для выявления возможных нарушений эмбрионального развития, проявляющихся в постнатальном периоде. За потомством наблюдали в течение 60 дней после рождения. Проводилась оценка общего состояния потомства крыс, выживаемость, прибавка в весе, физическое развитие, сформированность сенсомоторных рефлексов, эмоционально-произвольного поведения и способности точно координировать движения. Соотношение самцов и самок в потомстве во всех группах было практически одинаковым (примерно 1: 1). Во всех исследуемых группах за весь период наблюдения (от рождения до двухмесячного возраста) смертность детенышей не превышала 4 % и достоверно не различалась между группами. В группах не было различий в физическом и неврологическом развитии детенышей крыс, а индивидуально обусловленные значения исследуемых показателей находились в пределах физиологической нормы.
Таким образом, вакцина «КовиВак» не оказала отрицательного влияния на общее состояние беременных крыс. Эмбриотоксических, фетотоксических или тератогенных эффектов обнаружено не было. Вакцинация не привела к увеличению смертности потомства и не повлияла на физическое и психологическое развитие детенышей крыс.
Обсуждение результатов
Безопасность
Существует множество тестов для оценки различных параметров безопасности разрабатываемых вакцин на животных моделях. Авторы выбрали классические модельные объекты для исследования безопасности (мыши, морские свинки, крысы и приматы). Для вакцины «КовиВак» проводилась оценка общей острой токсичности у трех видов (мышей, морских свинок и игрунок), хронической токсичности у двух видов (мышей и морских свинок) и гиперчувствительности у морских свинок. По сравнению с группой плацебо никаких изменений выявлено не было. Все показатели были в пределах физиологической нормы.
Существовали предположения о возможной репродуктивной токсичности вакцинных препаратов, содержащих S-белок SARS-CoV-2. Исходя из данных экспериментов авторов на крысах линии Wistar, был сделан вывод о том, что многократная иммунизация вакциной «КовиВак» до или во время беременности не оказывает отрицательного эффекта на внутриутробное или постнатальное развитие потомства.
Таким образом, вакцина «КовиВак» безопасна и может быть использована в клинических испытаниях на людях.
Иммунитет и его стойкость
Краткосрочная иммуногенность вакцины «КовиВак» была оценена на трех животных моделях (двух генетических линиях мышей, сирийских хомячках и обыкновенных игрунках), иммунизированных разными дозами. Вакцина индуцировала синтез НАт у всех изученных видов. Более того, у мышей были обнаружены антитела к двум основным структурным белкам вируса (S и N). В течение первых 2–4 недель не наблюдалось значительных различий между титрами НАт, синтез которых был вызван различными дозами антигена. Различия проявились начиная с пятой недели после первой иммунизации.
Как было отмечено выше, синтез НАт является одним из основных маркеров защиты от SARS-CoV-2 [8]. Следовательно, длительность антительного ответа (НАт) коррелирует с длительностью защиты. После естественного заражения, особенно в случае легкого течения инфекции, ответ в виде НАт довольно слабый и непродолжительный [11].
Сведений об устойчивости иммунитета, вызванного вакциной, очень мало. Хотя в опубликованных доклинических исследованиях показана индукция титров IgG и НАт к SARS-CoV-2 IgG вследствие введения различных вакцин, лишь в немногих работах содержатся данные о продолжительности иммунного ответа. Например, для препарата PiCoVacc (инактивированная вакцина), опубликованы результаты доклинических испытаний, согласно которым титр антител после вакцинации мышей и крыс сохраняется в течение шести недель, а у макак-резусов — до трех недель [25]. В работе, опубликованной Wang с соавт., анализ иммуногенности у животных был ограничен четырьмя неделями [27].
В случае вакцины-кандидата BBV152 измерение иммуногенности при трехдозовом режиме введения проводилось до 25-го дня [29]. Авторы провели оценку долгосрочной иммуногенности у мышей и игрунок в течение одного года. За этот период значительного снижения титров НАт обнаружено не было. Более низкие дозы вводимого антигена приводили к формированию более низкого титра НАт в течение длительного периода наблюдения. Хотя очевидно, что окончательные сведения о длительности иммунитета, обеспечиваемого вакцинами против COVID-19, будут получены в ходе длительных клинических исследований, в данной ситуации животные модели могут служить в качестве удобных суррогатных индикаторов на ранних этапах процесса разработки вакцины. В недавней работе, посвященной клиническому исследованию вакцины на основе мРНК компании Moderna, сообщается о существовании повышенного титра специфических антител в течение как минимум трех месяцев [30]. Согласно экспериментальным данным авторов статьи, вакцина «КовиВак» обеспечивала формирование стабильного длительного иммунитета у мышей и игрунок после двухкомпонентного режима введения препарата.
Профилактическая эффективность
В большинстве недавних исследований в качестве удобной и достоверно нелетальной животной модели профилактической эффективности вакцин против COVID-19 используется золотистый (сирийский) хомячок. У сирийских хомячков инфекция SARS-CoV-2 вызывает значительные патологические изменения в легких и, таким образом, поддерживает развитие стабильного постинфекционного гуморального иммунного ответа в экспериментах с пассивным переносом [35]. Более того, наблюдаемые иммуногистохимические изменения и характер потери массы тела у хомячков сходны с легкой формой инфекции SARS-CoV-2 у человека [36]. В ряде работ продемонстрирована пригодность сирийского хомячка в качестве модели для изучения профилактической эффективности НАт и вакцин против SARS-CoV-2 [37–46], хотя симптомы пневмонии у животного развиваются быстро и протекают тяжело.
Сирийский хомячок в качестве модельного объекта был использован для оценки профилактической эффективности нескольких инактивированных вакцин [47–48], в том числе одобренных для клинического применения [29]. К основным параметрам оценки относят вес животного и присутствие вируса и/или вирусной РНК в мазках из носа, легких и других органов в разные сроки после инфицирования.
В исследовании авторов животные из группы контроля теряли вес до пятого — седьмого дня с момента заражения, тогда как вакцинированные набирали вес с начиная с третьего дня после заражения, что соотносится с данными о BBV152 [29]. Однако потеря веса у контрольных животных в экспериментах авторов была более выраженной — 15 % против 2–10 % в исследовании BBV152. Скорость выведения вирусной РНК из верхних дыхательных путей также была сходной: начиная с седьмого дня после инфицирования в большинстве мазков из носа вирусная РНК не содержалась. Уровень вирусной РНК в легких контрольных животных был одинаковым в обоих исследованиях; по данным авторов, в органах всех контрольных животных содержалась вирусная РНК на четвертые, седьмые и 14-е сутки. Ткани легких вакцинированных животных в основном не содержали вируса: только у одного из пяти хомячков на четвертый и седьмой дни можно было выявить РНК вируса в легких; однако к 14-му дню ткань легких очищалась от вируса. Вирусная РНК была обнаружена в иных тканях (помимо легочной) у животных контрольной группы только на третий день после заражения. Аналогичные результаты были получены для вакцинного препарата BBV152 [29]. Таким образом, представленные результаты демонстрируют профилактическую эффективность вакцины «КовиВак» на модели сирийского хомячка.
Таким образом, для вакцины «КовиВак» не было обнаружено признаков острой/хронической, репродуктивной, эмбрио- и фетотоксичности или тератогенного влияния в антенатальном и постнатальном периодах развития, а также признаков гиперчувствительности у исследованных видов животных. Вакцина способствовала формированию стабильного и устойчивого гуморального иммунного ответа — как в виде специфических IgG к SARS-CoV-2, так и НАт у грызунов и обезьян. Значительного снижения титров НАт в течение одного года не наблюдалось. «КовиВак» продемонстрировала профилактический эффект по отношению к инфекции SARS-CoV-2 у сирийских хомячков. Эти данные стимулируют дальнейшее изучение вакцины «КовиВак» в клинических испытаниях.