Лечение рака желудка
О заболевании
Рак желудка – это новообразование в слизистой желудка. По мере разрастания опухоли она прорастает глубже в слои желудка, а также в ближайшие органы и лимфатические узлы.
Симптомы отличаются в зависимости от стадии онкологии. Чтобы подтвердить наличие опухоли, ее вид и ее стадию, пациент направляется на дополнительные исследования терапевтом или гастроэнтерологом.
При лечении проводится операция с последующей химиотерапией. Прогноз на выздоровление зависит от стадии рака, его вида и тактики проводимого лечения.
Виды рака желудка
В зависимости от гистологического строения, рак желудка делится на:
При раке желудка проводится иммуногистохимия для выявления HER/2 нео рецепторов. Эта опухоль отличается более агрессивным течением, но, вместе с тем, наличие данных рецепторов позволяет использовать в лечении высокоэффективный таргетный препарат (например, герцептин).
Симптомы рака желудка и первые признаки
Диагностика рака желудка на ранних стадиях происходит очень редко. Если вы следите за своим самочувствием и не пренебрегаете появившимися «малыми признаками», то лучше обратиться к врачу. В нашей клинике принимают онконастороженные терапевты и гастроэнтерологи, то есть они учитывают возможность наличия онкологии и, при малейшем подозрении, направляют таких пациентов на диагностику, которая позволяет исключить или выявить ранний рак.
Клиническое проявление онкологии напрямую зависит от стадии. Для начальных стадий характерно полное отсутствие симптомов или незначительное проявление:
К симптомам второй стадии относятся:
К симптомам третьей стадии относятся:
К симптомам четвертой стадии относятся:
Диагностика рака желудка
Установить верный диагноз можно только с помощью инструментальной диагностики. Но перед ее назначением предположительный диагноз должен подтвердиться другими диагностическими методами.
Для этого терапевтом или гастроэнтерологом проводится тщательный сбор и анализ жалоб пациента при подозрении на наличие онкологии. В зависимости от полученных данных назначается подходящая диагностика.
После всего этого проводятся лабораторные исследования:
Инструментальная диагностика рака предусматривает:
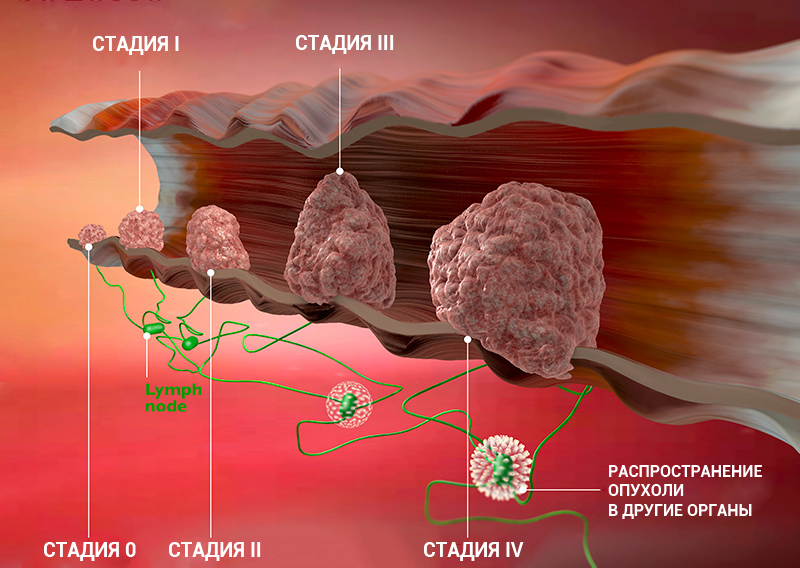
Стадии рака желудка и прогноз
1 стадия
Опухоль небольшого размера (до 2 см), занимает слизистый и подслизистый слой стенки желудка. Ближайшие лимфоузлы не поражены или поражены точечно, метастазов нет. Прогноз при данной стадии благоприятный и составляет 60-80% выживаемости.
2 стадия
Опухоль уже прорастает глубже в стенку желудка и поражает больше регионарных узлов (до 15), при этом метастазов нет. Прогноз при данной стадии составляет 50% выживаемости.
3 стадия
Происходит полное поражение всей стенки желудка и более отдаленных лимфоузлов, но нет метастазов в отдаленных органах. Возможно поражение опухолью соседних органов, но без поражения лимфоузлов. Прогноз при данной стадии составляет 20% выживаемости.
4 стадия
Характеризуется распространением рака на соседние органы или наличием хотя бы одного метастаза в отдаленные органы. Прогноз при данной стадии составляет 10% выживаемости.
Очень важно отметить, что при 4 стадии наша задача состоит в том, чтобы перевести заболевание в хроническую форму, что позволяет продлить жизнь пациента в 3 и более раз.
Не зависимо от стадии вы получите лечение европейского уровня, которое намного эффективнее, чем протоколы Минздрава, принятые в России и странах СНГ.
Метастазы при раке желудка
При раке желудка метастазы распространяются либо по лимфатическим путям, либо по системе кровоснабжения. Наиболее часто происходит метастазирование печени, поджелудочной, кишечника и брюшной стенки.
Лечение рака желудка
Рак желудка почти всегда лечится хирургически. Объем операции напрямую зависит от стадии заболевания. Если опухоль не успела прорасти вглубь стенки желудка, то проводят эндоскопическую резекцию при помощи гастроскопа.
При субтотальной гастрэктомии удаляется часть желудка, пораженную онкологией.
На более поздних стадиях желудок удаляется целиком с захватом окружающих тканей. Пищевод при этом сшивают с тонким кишечником. При наличии пораженных лимфоузлов, они также подлежат удалению.
В тяжелых случаях, когда полное излечение невозможно, проводится паллиативная операция. Хирург удаляет пораженную часть желудка, чтобы облегчить состояние пациента и перевести рак в хроническую форму.
Химиотерапия при раке желудка
Химиотерапия бывает адъювантной и неоадъювантной. То есть до операции и после нее. При некоторых видах онкологии ее совмещают с лучевой терапией. Сочетание химиотерапии и лучевой терапии может быть основной тактикой при метастазировании на поздних стадиях, когда полное излечение невозможно.
В отдельных случаях эффективны таргетные препараты: трастузумаб, рамуцирумаб, иматиниб, сунитиниб, регорафениб. Но их применение возможно только когда раковые клетки обладают нужными молекулярно-генетическими характеристиками.
Стадии рака: классификация онкологических заболеваний
Стадия онкологического заболевания дает информацию о том, насколько велика опухоль и распространилась ли она по организму. Это помогает врачам определять прогноз пациента и план лечения.
С помощью врача-онколога, резидента Высшей школы онкологии Сергея Югая разбираемся, как врачи устанавливают стадии рака и что каждая из них означает.
На что влияет стадия онкологического заболевания?
Стадирование нужно, чтобы спрогнозировать, какие у пациента шансы на выздоровление, а также чтобы определить, какой метод лечения будет наиболее эффективен в конкретном случае, — поясняет Сергей Югай.
Все начинается с медицинского осмотра и обследований — УЗИ, КТ, МРТ, ПЭТ-КТ и других методов в зависимости от вида рака. Затем врач берет кусочек опухоли — биопсию или удаляет опухоль целиком во время операции, а после отправляет материал на гистологический анализ, чтобы поставить диагноз.
Стадии рака по TNM-классификации
Стадии онкологического процесса описывают разными способами — это зависит от вида опухоли. Один из самых распространенных способов — стадирование с помощью TNM-классификации.
Т характеризует первичную опухоль, ее размеры и вовлечение окружающих структур в опухолевый рост, например, прорастание в стенку кишки или желудка. N говорит о наличии в лимфоузлах метастазов и количестве пораженных лимфоузлов, а М — о наличии отдаленных метастазов (во внутренних органах, костях, ЦНС или лимфоузлах, которые расположены далеко от первичной опухоли), — объясняет Сергей Югай.
Индекс Т принимает значения от 0 до 4. 0 означает, что первичная опухоль не обнаружена, 1 — опухоль маленькая, а 4 — опухоль проросла в прилегающие ткани. Таким образом, чем больше цифра рядом с Т, тем ситуация сложнее. При некоторых видах рака N принимает значение 0 или 1, при других — 0, 1 или 2, а иногда — 0, 1, 2 и 3. 0 означает, что опухоль не проникла в ближайшие лимфоузлы, а 3 — что поражено множество лимфоузлов. M0 показывает, что метастазов нет, а 1 — что метастазы есть.
Онкологи выставляют стадию по TNM клинически — до операции или когда операция не планируется и патоморфологически — при изучении удаленной во время операции опухоли, — объясняет Сергей.
Клиническая стадия обозначается буквой «c», например, cT2. Патоморфологическая — буквой «p», например, pN1.
От правильной стадии зависит тактика лечения. Например, пациент — мужчина с раком желудка и стадией cT1N0M0. Это значит, что опухоль прорастает в слизистую и подслизистый слой стенки желудка. В этом случае пациенту показана операция. Если же стадия выше (cT2N1M0, например), то есть опухоль пациента прорастает в мышечный слой, и есть метастазы в лимфоузлах, то может понадобиться химиотерапия перед операцией, которая позволит улучшить результаты лечения, — добавляет Сергей.
Стадию рака могут обозначать с помощью цифр — 0, I, II, III, IV. Что это значит?
Клинические стадии (0, I, II, III, IV) тесно связаны с системой TNM. Как правило, одна клиническая стадия включает в себя несколько вариантов стадирования по TNM. Эти варианты характеризуются схожими прогнозом и подходом к лечению. Например, стадии T1N3M0, T2N3M0, T3N2M0 рака легкого объединяются в IIIВ стадию, так как при любой из этих ситуаций пациент будет иметь примерно одинаковый прогноз и тактику лечения. В этом конкретном примере необходима химиолучевая терапия, а не операция, — комментирует Сергей Югай.
Меняется ли стадия после лечения, при прогрессировании заболевания?
Нет, стадия выставляется один раз. Но есть нюансы:
Например, мы хотим посмотреть, как опухоль ответила на лечение, чтобы понять, можно ли делать операцию. После лечения опухоль уменьшилась, и мы добавляем к стадии новые данные. При прогрессировании опухолевого процесса первоначальная стадия также остается прежней, но, к сожалению, прогноз будет менее благоприятный. Например, у человека II стадия рака желудка. Он прооперирован, и прогноз у него хороший. Через 2 года врачи обнаруживают у пациента метастазы в легких. Стадия остается II, но рак у пациента уже метастатический, что очень усложняет положение, — говорит Сергей.
Бывает, что люди сравнивают свою ситуацию с историями других пациентов. Если речь идет о разных онкологических заболеваниях, то такие сравнения некорректны — это заболевания с разными прогнозами и схемами лечения:
Например, с нейроэндокринным раком поджелудочной железы люди могут жить десятилетиями, а при метастатической стадии рака поджелудочной железы — полгода или год, — объясняет врач-онколог.
Что может повлиять на прогноз людей с одинаковой стадией и одним видом рака?
Сергей Югай выделяет три фактора:
Что значит новообразование неопределенного или неизвестного характера желудка
Нейроэндокринные опухоли (НЭО) развиваются в клетках периферической нейроэндокринной системы, рассеянной в различных органах, и наблюдаются довольно редко [1]. Отмечена тенденция к значительному увеличению частоты встречаемости НЭО, что может быть связано, с одной стороны, с совершенствованием и широким внедрением эндоскопической диагностики, с другой — с повышением информированности клиницистов и патоморфологов. Исходя из вышеизложенного, обзор литературы, посвященный патогенезу, диагностике и лечению НЭО желудка (НЭОЖ), весьма актуален.
Классификация
Классификация НЭО по стадиям имеет практическое значение в прогнозировании и выборе лечебной тактики. Европейским обществом нейроэндокринных новообразований (ENETS) предложена классификация (2006), основанная на величине митотического индекса и Ki-67 — маркера НЭО [2]. В дальнейшем (2010) эти протоколы были поддержаны классификацией ВОЗ [3], согласно которой НЭО группируют следующим образом: НЭО G1, НЭО G2, нейроэндокринная карцинома (НЭК), смешанная адено-НЭК, а также гиперпластические и предопухолевые образования (табл. 1). 
Опухоли класса G3 по критериям ENETS соответствуют НЭК в классификации нейроэндокринных образований ВОЗ (2010).
Эпидемиология
Среди всех первично выявленных НЭО 11—12% их локализуются в желудке. В последнее время прослеживается тенденция к увеличению доли НЭОЖ среди общего числа гастроинтестинальных НЭО [4—9]. Более чем 60-летние наблюдения позволяют предположить, что частота встречаемости НЭОЖ увеличилась с 0,3 до 1,8% среди всех злокачественных новообразований желудка, при этом у женщин европеоидной расы она возросла в 800 раз [8]. В некоторых наблюдениях отмечен 6—9-кратный рост встречаемости НЭОЖ за 1981—2000 гг. [10].
Эпидемиологические показатели НЭОЖ с 2000 по 2006 г. в Великобритании среди мужчин и женщин составили соответственно 0,16 и 0,15 на 100 000 человек, что по сравнению с показателями 1995 г. демонстрирует 23-кратное увеличение заболеваемости среди мужчин и 47-кратное — среди женщин [6]. Подобное увеличение частоты встречаемости НЭОЖ наблюдалось и в США: с 0,03 (1973—1977) до 0,33 (2003—2007) на 100 000 человек [11].
Данные японских исследователей также подтверждают увеличение встречаемости НЭО, локализованных в области передней кишки (желудка и двенадцатиперстной кишки) с 1,05 (2005) до 1,67 (2010) на 100 000 человек [7, 12]. Это связывают с ростом частоты развития хронического атрофического гастрита (ХАГ) на фоне систематического приема ингибиторов протонной помпы (ИПП) [13], с улучшением эндоскопической диагностики, стандартизацией морфологических исследований и возросшей публикационной активностью.
Гистологическая классификация и клиническая картина
НЭОЖ можно подразделить на хорошо и плохо дифференцированные. Хорошо дифференцированные НЭОЖ развиваются из энтерохромаффиноподобных (ЭХП) клеток тела и дна желудка, которые в норме продуцируют гистамин и участвуют в регуляции желудочной секреции.
В настоящее время НЭОЖ подразделяют на три типа [14]. В табл. 2 представлены 
Самым распространенным считают I тип — около 70—80% всех НЭОЖ, встречается преимущественно у женщин (60—70%) в возрасте старше 60—65 лет [27]. Распространенность поражения в популяции составляет 0,2 случая на 100 000 населения, при этом считают, что в последние годы она достигла 1,8 случая на 100 000 населения [10, 27].
Гистологически опухоли I типа состоят из ЭХП-клеток и обычно обнаруживаются у больных ХАГ типа А, включая аутоиммунный гастрит и атрофический гастрит, ассоциированный с Helicobacter pylori [23]. Известно, что ахлоргидрия, вызванная атрофией желез дна желудка при ХАГ, приводит к гипергастринемии и повышению внутрижелудочного рН с развитием гиперплазии G-клеток антрального отдела желудка. Гастрин взаимодействует с ССК2-рецепторами на мембране ЭХП-клеток и приводит к их гиперплазии. Перманентная стимуляция гастрином ССК2-рецепторов, а также протеинкиназы С и митоген-активируемой протеиновой киназы индуцирует постоянную экспрессию клеток mcl-1, синтезирующих белок, обладающий способностью подавлять апоптоз [28].
Предполагают, что прием ИПП, а также ваготомия вкупе с генетическими, диетическими, гормональными и бактериальными факторами играют роль ко-факторов в развитии гипергастринемии и НЭОЖ. Мутация Reg-гена, контролирующего в норме ответ ЭХП-клеток на гастрин, приводит к его бесконтрольному стимулирующему воздействию на ЭХП-клетки, их пролиферации и увеличению риска развития НЭОЖ I типа. В эксперименте показана вероятная роль инфекции Helicobacter pylori в развитии ХАГ, гипергастринемии и НЭОЖ [29—31].
При иммуногистохимическом окрашивании клетки НЭО определяются как положительные по наличию хромогранина A (CgA), синаптофизина, везикулярного моноаминного транспортера 2 и рецептора соматостатина 2А [32]. В частности, окрашивание CgA позволяет увидеть изменения в ЭХП-клетках по типу гиперплазии и дисплазии. Для гиперплазии характерно наличие более 6 рядов линейной гиперплазии на 1 мм. Дисплазия, присутствующая главным образом в микроинфильтративных образованиях, ассоциируется с повышенным риском НЭОЖ [33].
Как правило, опухоли I типа не злокачественные, часто множественные, размером менее 2 см. Локальное поражение наблюдается в 90—95%, а отдаленные метастазы — у 1—2% больных. Злокачественный потенциал напрямую зависит от размеров опухоли и глубины ее инвазии, но при этом мультицентричность напрямую не коррелирует с вероятностью появления метастазов. Выживаемость таких больных не отличается от сроков жизни в популяции людей соответствующего возраста [34—36]. При наличии метастазов 5-летняя выживаемость составляет обычно 50—60% и не превышает 75% [8]. В связи с этими особенностями развития опухоли возникает вопрос о допустимости локальных методов лечения при очевидном операционно-анестезиологическом риске.
НЭОЖ II типа встречается реже — в 5—6%, имеет промежуточный малигнизационный потенциал и может быть ассоциирована с синдромом МЭН I типа — 10—15% и синдромом Золлингера—Эллисона (СЗЭ) — около 1%. Приблизительно у 30% больных с этим типом опухоли обнаруживают метастазы. Если опухоль I типа локализуется, как правило, в теле и фундальном отделе желудка, то новообразования II типа могут встречаться и в антральном отделе [37]. Опухоли типа II, как и типа I, ассоциированы с гипергастринемией и развиваются из ЭХП-клеток.
НЭОЖ III типа — самый агрессивный тип, на долю которого приходится около 15—20%. Это спорадические опухоли, развитие которых не связано с желудочной секрецией и гиперплазией ЭХП-клеток. Отдаленные метастазы диагностируют у 50—100% больных. Эта опухоль обычно продуцирует 5-гидрокситриптофан и не связана с гипергастринемией [38, 39].
Технология микрочипов позволила выявить различия в экспрессии генов при различных вариантах опухоли. Так, из 270 исследованных генов статистически значимое различие установлено для мутаций CagA, MAGE — D2, MTAI, CCN2, что позволяет дифференцировать III и I типы. Доказано, что мутация гена супрессора опухоли р53 прямо коррелирует с НЭОЖ III типа и обусловливает стимуляцию пролиферации клеток [38, 39].
Большинство НЭОЖ I типа представляют собой небольшие, множественные опухоли, расположенные в теле или дне желудка и ограниченные слизистым или подслизистым слоем желудочной стенки. Поскольку большинство НЭОЖ I типа — это опухоли класса G1, метастатический риск является крайне низким, а прогноз — благоприятным. У пациентов с НЭОЖ I типа, ассоциированными с аутоиммунным гастритом, могут наблюдаться и другие аутоиммунные заболевания (сахарный диабет 1-го типа, аутоиммунный тиреоидит и первичный билиарный цирроз печени) или пернициозная анемия [24].
НЭОЖ I типа обычно протекают бессимптомно и случайно выявляются при скрининговом эндоскопическом исследовании верхних отделов желудочно-кишечного тракта. Опухоли I и II типа обнаруживают эндоскопически как полипы фундального отдела (часто множественные).
НЭОЖ II типа также небольшого размера, множественные и относительно доброкачественные. Однако в отличие от типа I они встречаются у мужчин и женщин одинаково часто. Приблизительно 30% НЭОЖ II типа на момент клинических проявлений имеют метастатическое распространение [19], а показатели выживаемости пациентов с такими НЭОЖ ниже, чем при типе I [40]. Течение большинства НЭОЖ II типа асимптомное, однако повышенная секреция желудочного сока, отмечаемая у больных с типом II, может привести к образованию пептической язвы, поэтому у таких пациентов могут наблюдаться клинические признаки язвенной болезни [41].
Контрольное обследование и прогноз
Программы контрольного обследования составляют в зависимости от типа и размеров опухоли, характера проведенного лечения, наличия рецидива. Контрольное обследование включает сбор анамнеза, осмотр, инструментальные исследования: ЭГДС, по показанию — КТ и МРТ в зависимости от клинических проявлений.
При опухоли I типа весь комплекс исследований повторяют 1 раз в 2 года, при опухоли II типа — ежегодно. В ходе ЭГДС необходима биопсия слизистой оболочки в зоне фонового ХАГ (для исключения развития аденокарциномы). Уровень гастрина исследуют у больных опухолью I и II типа.
Больным с высокодифференцированной опухолью III типа показана радикальная операция. В послеоперационном периоде проводят сцинтиграфию и исследование уровня CgA каждые 6 мес в течение 2 лет, а затем ежегодно в течение 3 лет. При метастазах опухоли контроль эффективности лечения осуществляют каждые 6 мес.
При опухоли I типа, как правило, указывают на 100% 5-летнюю выживаемость и крайне редкие летальные исходы, при опухоли II типа выживаемость составляет 60—75%, отражает уровень смертности при синдроме МЭН-I и более высокий потенциал малигнизации. При НЭОЖ III типа после радикального хирургического лечения 5-летняя выживаемость достигает 75%, а при злокачественной гастриноме IV стадии не превышает 20—38% [86].
Согласно рекомендациям NCCN [57], пациенты с небольшими ( 20 мм) должны обследоваться каждые 3—12 мес после резекции и каждые 6—12 мес в дальнейшем.
ENETS [47] рекомендует эндоскопический контроль пациентам с рецидивирующими НЭОЖ I типа каждые 12 мес, пациентам без рецидива каждые 24 мес. Ежегодная ЭГДС рекомендована больным с НЭОЖ II типа. Дальнейшее обследование пациентов с НЭОЖ III типа, перенесших гастрэктомию, проводят так же, как и после аналогичной операции при аденокарциноме желудка.
Таким образом, НЭОЖ представлены широким спектром новообразований, включающих и очень медленно прогрессирующие, и рано метастазирующие. Наблюдается значительное увеличение частоты встречаемости НЭОЖ. В соответствии с гистологическими критериями НЭОЖ делятся на 3 типа. Лечение каждого больного должно быть строго индивидуальным и проводиться командой специалистов разного профиля. При выборе способа лечения НЭОЖ следует исходить из типа опухоли, ее гистологических характеристик, локализации и степени выраженности местной инвазии, а также наличия метастазов. Личный опыт большинства хирургов ограничен небольшой группой больных, поэтому для выбора оптимального лечения необходимо опираться на результаты опубликованных исследований. Для определения оптимального способа диагностики и лечения НЭОЖ требуются дальнейшие исследования.
Авторы заявляют об отсутствии конфликта интересов.
The authors declare no conflict of interest.
Чем отличается доброкачественная опухоль от злокачественной
В медицине понятие доброкачественности означает лёгкое течение болезни, хорошие результаты лечения и неопасность для жизни. Под злокачественным процессом подразумевают разрушительное течение, сложность терапии, высокий риск смертности.
Для опухолей такое разделение условно. Тем не менее пациентам и врачам крайне важно определить вид опухоли. От этого зависят тактика лечения и прогноз.
Характеристика доброкачественных и злокачественных опухолей
Существуют чёткие критерии:
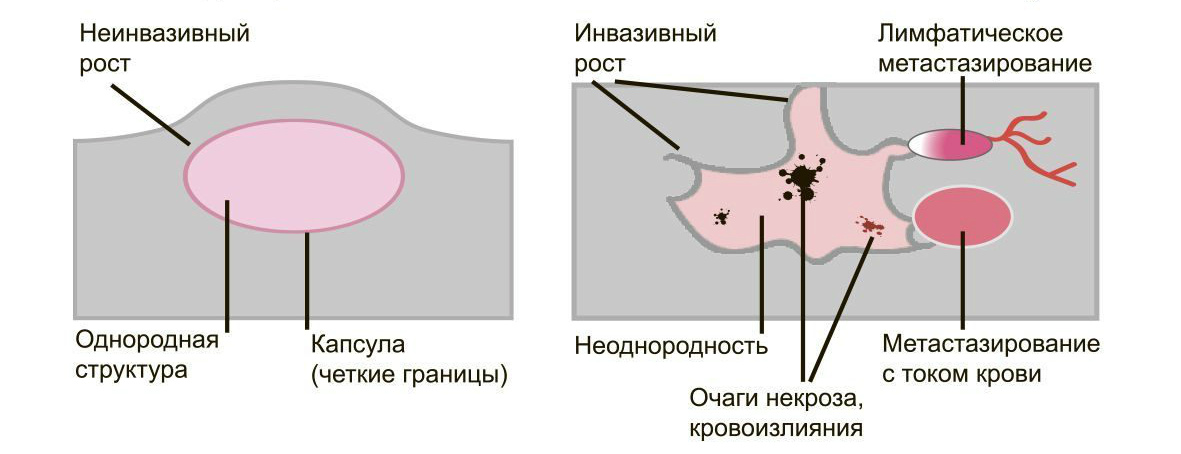
Доброкачественные опухоли чётко отграничены от здоровых тканей, часто имеют капсулу. Рак прорастает окружающие ткани, внедряется в сосуды, его контуры более аморфны.
Большинство доброкачественных опухолей могут расти годами, не проявляя симптомов. Карциномы растут быстро, нарушая функции органов и отравляя организм. Рост сопровождается утомляемостью, слабостью, потерей веса, болью.
Доброкачественные образования “сидят” на одном месте, постепенно растут и раздвигают здоровые ткани, подвижны при прощупывании. Раковые клетки слабо скреплены друг с другом, легко отделяются и разносятся лимфой и кровью по организму. Они оседают в лимфоузлах, костях, внутренних органах, образуя новые опухолевые очаги — метастазы. При пальпации узел спаян с тканями и не сдвигается.
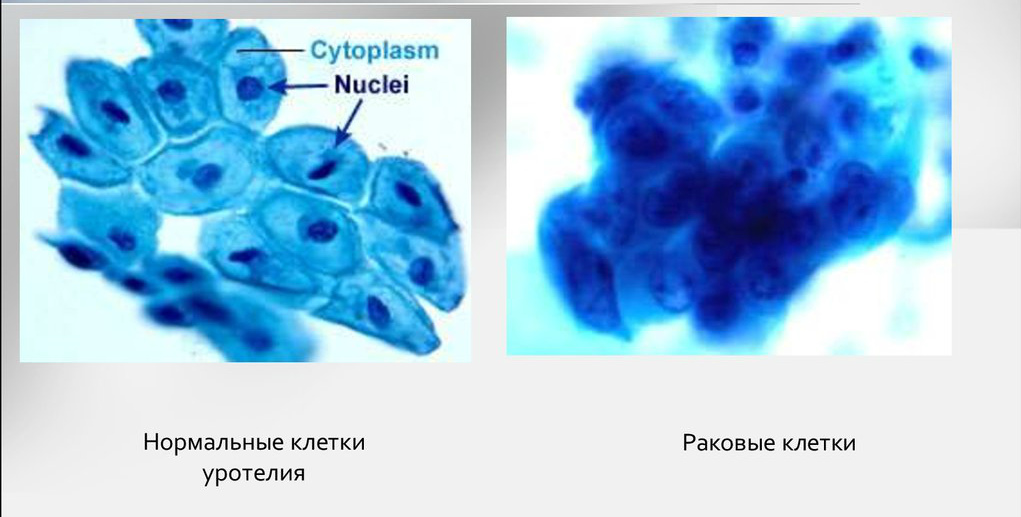
Много информации даёт биопсия. Исследование показывает, что доброкачественные клетки похожи на здоровые, их структура более чёткая. Структура злокачественных клеток сильно изменена из-за выраженных мутаций. Чем меньше клетки напоминают ткань, из которой выросли, тем хуже прогноз для лечения и жизни.
Доброкачественную опухоль, такую как аденома простаты, можно удалить и добиться полного излечения. Если возникнет рецидив, он будет на том же месте, где нашли первичный очаг. Злокачественные образования трудно удалить полностью. Даже одна оставшаяся клетка даст новую опухоль либо на старом месте, либо там, куда она попала по сосудам. Выживаемость больных существенно ниже.
Общие свойства доброкачественных и злокачественных опухолей
Есть моменты, объединяющие оба вида новообразований:
Тяжесть симптомов зависит не только от степени сдавления тканей опухолью, но и от неспособности новообразования выполнять функцию здоровых клеток.
Виды опухолей
Различия не всегда очевидны. Нужна тщательная диагностика для поиска атипичных клеток.
Может ли доброкачественная опухоль стать злокачественной
Любая опухоль способна к малигнизации. Миомы, липомы, фибромы редко переходят в рак. Кисты — крайне редко. Невусы, аденомы, полипы в желудке или кишечнике — очень часто. Многое зависит от условий, в которых находится опухоль, питания, экологии, уровня стресса, гормональных сбоев, наличия предраковых болезней.
В Клинике урологии имени Р. М. Фронштейна доступна современная диагностика опухолей, разработаны эффективные методики лечения. Обращайтесь на консультацию и наши специалисты вам помогут.