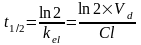Что значит полувыведение препарата
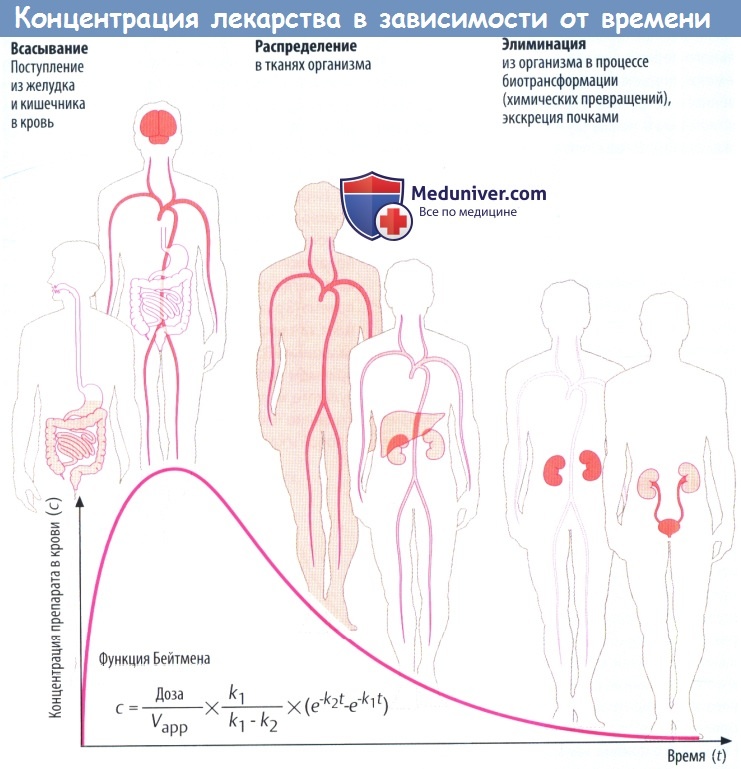
Такие процессы, как всасывание и выведение, обладают экспоненциальными характеристиками. В отношении всасывания это следует из простого факта: количество препарата, перемещающегося за единицу времени, зависит от разности концентраций (градиента) на границе двух тканей (закон Фика).
В процессе всасывания из пищеварительного тракта содержимое кишечника и кровь представляют собой ткани с изначально высокой и низкой концентрациями соответственно. При выведении лекарственного вещества через почки экскреция часто зависит от скорости клубочковой фильтрации, т. е. от количества препарата, попавшего в первичную мочу.
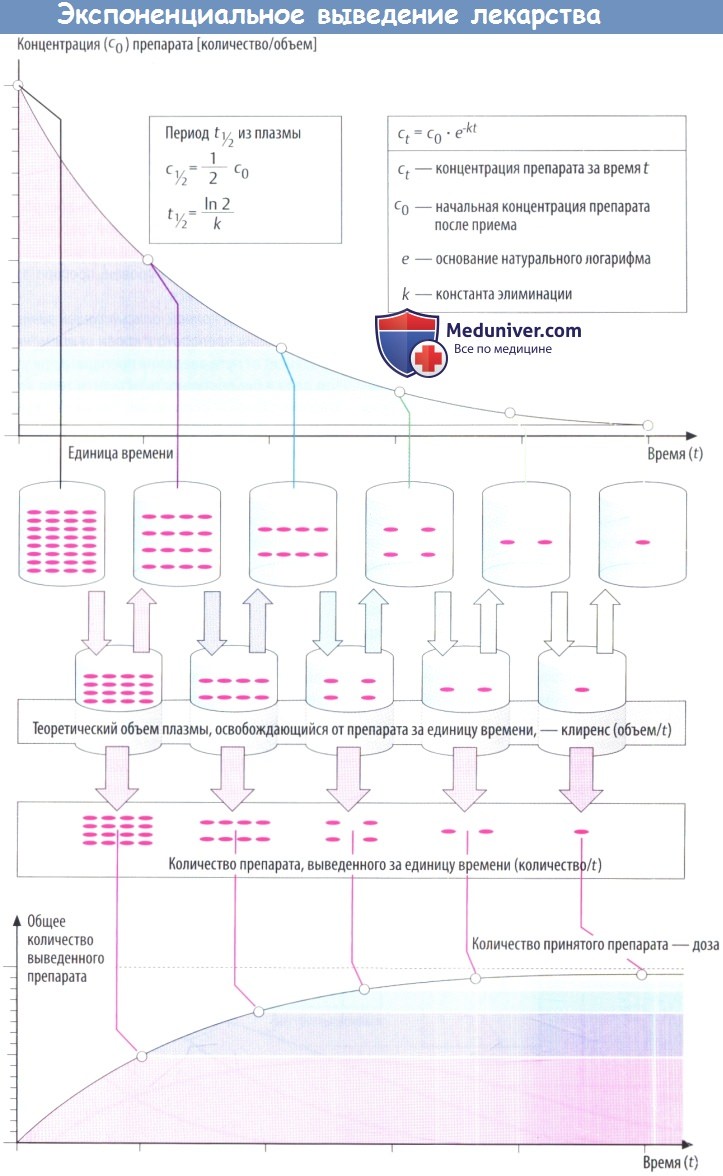
По мере снижения концентрации в крови количество лекарственного вещества, экскретируемого через почки за единицу времени, уменьшается. В результате происходит экспоненциальное снижение, показанное на рисунке ниже. Время экспоненциальногоснижения — постоянный интервал, в течение которого концентрация снижается в 2 раза.
Этот интервал представляет собой период полувыведения (t1/2) и связан с константой скорости элиминации (k) уравнением: t1/2 = (ln2)/k. Эти два параметра вместе с исходной концентрацией (с0) описывают скорость реакции первого порядка (экспоненциальную).
Поскольку эта скорость постоянная, она дает возможность вычислить объем плазмы, освобожденной от лекарственного вещества, учитывая, что оставшееся количество не распределено равномерно в общем объеме плазмы (условие, невозможное в реальности). Теоретический объем плазмы, освобождающейся от лекарственного вещества за единицу времени, называется клиренсом.
В зависимости от того, снижается концентрация в плазме в результате экскреции с мочой либо в результате разрушения в процессе метаболизма, клиренс называют почечным или печеночным. Почечный и печеночный клиренсы суммируются, образуя общий клиренс (Cltot) в случае, если препараты выводятся в неизмененном виде через почки и подвергаются биотрансформации в печени.
Cltot представляет собой сумму всех процессов, участвующих в выведении; он связан с периодом полувыведения (t1/2) и объемом распределения препарата (Vapp) формулой:
Чем меньше объем распределения и чем больше общий клиренс, тем короче период полувыведения.
Для препаратов, выводимых почками в неизмененном виде, t1/2 можно вычислить на основании кумулятивной экскреции с мочой; итоговое общее количество выведенного препарата соответствует количеству всосавшегося препарата.
Печеночная элиминация происходит по экспоненте, т. к. ферменты, катализирующие реакции метаболизма, действуют в квазилинейной области своей кривой активности концентрации; следовательно, количество вещества, подвергшегося метаболизму за единицу времени, уменьшается параллельно снижению концентрации в крови.
Самое известное исключение из экспоненциального закона — выведение алкоголя (этанола), которое происходит по линейному закону (кинетика нулевого порядка), во всяком случае, при концентрации в крови менее 0,02%. Это происходит потому, что лимитирующий скорость фермент алкогольдегидрогеназа достигает полунасыщения при очень низких концентрациях вещества — примерно 80 мг/л (0,008%).
Таким образом, при концентрации этанола в крови на уровне примерно 0,02% скорость реакции выходит на плато, при концентрациях выше этого уровня количество лекарственного вещества, выведенного за единицу времени, остается постоянным.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Период полувыведения (полужизни)
Период полувыведения [ править | править код ]
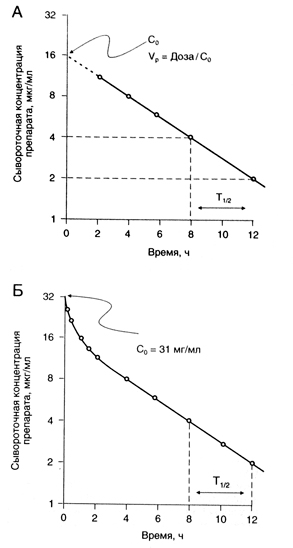
Период полувыведения (Т1/2) — это время, за которое сывороточная концентрация вещества (или его общее содержание в организме) снижается вдвое. В рамках однокамерной модели (рис. 1.4, А) определить Т1/2 очень просто. Полученное значение используют затем для расчета дозы. Однако для многих лекарственных средств приходится использовать многокамерную модель, так как динамика их сывороточной концентрации описывается несколькими экспоненциальными функциями (рис. 1.4, Б). В таких случаях рассчитывают несколько значений Т1/2.
Раньше Т1/2 рассчитывали по участку фармакокинетической кривой, отражающему стадию равновесия (стадию элиминации). С появлением более чувствительных методов измерения концентрации веществ в крови оказалось, что конечный Т1/2 гораздо больше начального. Например, для гентамицина конечный Т1/2 равен 53 ч, тогда как в Приложении II приведен T1/2 2—3 ч. Чрезвычайно длительный конечный Т1/2 индометацина (120 ч) обусловлен, вероятно, активным кишечно-печеночным кругооборотом препарата (в Приложении II приведен Т 1/2 2,4 ч). Клиническая значимость Т1/2 для того или иного периода зависит от того, какая доля вещества выводится из организма и каков объем распределения в этот период, а также от того, какой из показателей — сывороточная концентрация препарата или его общее содержание в организме — лучше коррелирует с фармакологическими эффектами. В Приложении II приведены величины Т1/2, имеющие наибольшее практическое значение.
В прошлом изменение фармакокинетики лекарственных средств при разных патологических состояниях оценивали только на основании Т1/2. В настоящее время общепризнано, что Т1/2 зависит от клиренса и объема рас- пределения вещества. В стационарном состоянии зависимость между Т1/2, клиренсом и объемом распределения приблизительно описывается следующим уравнением:
T1/2 = 0.693 x Vc / Cl(1.12)
Клиренс характеризует способность организма элиминировать вещество, поэтому при снижении этого показателя вследствие какого-либо заболевания Т1/2 должен увеличиваться. Но это справедливо лишь в том случае, если не меняется объем распределения вещества. Например, с возрастом Т1/2 диазепама увеличивается, но не за счет уменьшения клиренса, а вследствие увеличения объема распределения (Klotzetal., 1975). На клиренс и объем распределения влияет степень связывания вещества с белками плазмы и тканей, так что предсказать изменение Т1/2 при том или ином патологическом состоянии не всегда возможно. При остром вирусном гепатите Т1/2 толбутамида уменьшается, а не увеличивается, как это можно было бы ожидать, из-за снижения степени связывания препарата с белками плазмы и тканей. Объем распределения толбутамида не меняется, а клиренс увеличивается вследствие увеличения сывороточной концентрации свободного препарата (Williams et al., 1977).
По Т1/2 не всегда можно судить об изменении элиминации препарата, зато этот показатель позволяет рассчитать время достижения стационарного состояния (в начале лечения, а также при изменении дозы или частоты введения). Сывороточная концентрация, составляющая примерно 94% средней стационарной, достигается за время, равное 4Т1/2. Кроме того, с помощью Т1/2 можно оценить время, необходимое для полного удаления вещества из организма, и рассчитать интервал между введениями (см. ниже).
Стационарное состояние [ править | править код ]
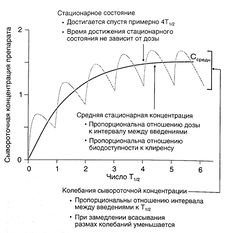
Согласно уравнению 1.1, если вещество вводится путем инфузии с постоянной скоростью, в стационарном состоянии скорость поступления вещества (скорость инфузии) равна скорости его элиминации (произведение клиренса на сывороточную концентрацию препарата — уравнение 1.3). Уравнение 1.1 можно применять и при дробном введении (например, 250 мг каждые 8 ч): в этом случае также устанавливается стационарная сывороточная концентрация препарата, но в промежутках между введениями она колеблется от минимальной до максимальной (рис. 1.5).
Описание к рис. 1.5. Динамика сывороточной концентрации лекарственного средства при дробном введении. Серая кривая описывает накопление препарата при введении с интервалами, равными Т1/2, при условии, что скорость всасывания в 10 раз больше скорости элиминации. При увеличении скорости всасывания максимальная концентрация в стационарном состоянии стремится к 2, а минимальная — к 1. Черная кривая отражает динамику сывороточной концентрации препарата, который вводят в эквивалентной дозе путем инфузии. Обе кривые соответствуют однокамерной фармакокинетической модели. Средняя концентрация в стационарном состоянии вычисляется по уравнению:
Cсредн=F x Доза / (Cl x T)
Это уравнение можно получить путем замены в уравнении 1.1 скорости поступления вещества на выражение F х Доза / Т. Ссредн соответствует концентрации препарата в стационарном состоянии при введении путем инфузии.
Сколько времени требуется, чтобы психотропные препараты вышли из организма?
С точки зрения фармакологии можно выделить несколько периодов ( 3-4) полураспада в качестве временного интервала времени для распада соединения, поскольку в это время происходит 8-16-кратное снижение концентрации препарата. Мы также должны учитывать активные метаболиты. Например, кофеин распадается на параксантин, теобромин и теофилин, все из которых имеют свои собственные эффекты и периоды полураспада, сохраняющиеся за пределами периодов распада исходного соединения.
Ответ на этот вопрос в значительной степени зависит от особенностей самого препарата. Это также зависит от генетических особенностей организма и других лекарств и продуктов, которые человек может употреблять с пищей, так как все они могут влиять на метаболические пути разрушения препарата. Например, грейпфрутовый сок может значительно повысить период выведения из организма многих лекарств, поскольку он ингибирует важный фермент, который разрушает эти препараты (CYP3A4).
Психотропные препараты обычно меняют физические структуры мозга и / или системы организма, а также изменяют их функционирование таким образом, что оно может быть неопределенным по длительности, независимо от того, принимаете ли вы препараты или нет. Они также склонны вызывать синдром отмены из-за физической зависимости, что обычно влечет за собой хроническое ( постоянное ) использование психотропных веществ. Изменения могут даже регистрироваться на эпигенетическом уровне, и многие часто используемые психотропные препараты как бы привязаны к долгосрочным рискам и дисфункциям, которые продолжают сохраняться даже после прекращения употребления психотропных средств (и даже после короткой продолжительности их использования). То есть, выведение лекарств из организма, в каких бы то ни было формах (активные метаболиты, неактивные метаболиты, потенциальные тканевые структутры и т. д.) не закончится восстановлением или более существенным процессом «очистки» от препарата.
12. Период полувыведения лекарств, его сущность, размерность, взаимосвязь с другими фармакокинетическими параметрами.
Период полуэлиминации (t½, мин) – это время, необходимое для снижения концентрации ЛС в крови ровно наполовину. При этом не играет роли каким путем достигается снижение концентрации – при помощи биотрансформации, экскреции или же за счет сочетания обоих процессов.
Период полуэлиминации определяют по формуле:
Период полувыведения – важнейший фармакокинетический параметр, позволяющий:
а) рассчитать время наступления равновесной концентрации (равно 5 периодам полуэлиминации)
б) определить время полной элиминации препарата
в) предсказать концентрацию ЛС в любой момент времени (для ЛС с кинетикой первого порядка)
13. Клиренс как главный параметр фармакокинетики для управления режимом дозирования. Его сущность, размерность и связь с другими фармакокинетическими показателями.
С 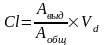
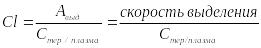
Таким образом, клиренс – отношение скорости выведения лекарственного средства к его концентрации в плазме крови.
В таком виде формулу клиренса используют для расчета поддерживающей дозы лекарства (Dп), т.е той дозы лекарственного средства, которая должна скомпенсировать потерю лекарства и поддержать его уровень на постоянном уровне:
Клиренс аддитивен, т.е. элиминация вещества из организма может происходить с участием процессов, идущих в почках, легких, печени и других органах: Clсистемный = Clпочечн. + Clпечени + Clдр.
Клиренс связан с периодом полуэлиминации ЛС и объемом распределения: t1/2=0,7*Vd/Cl.
14. Доза. Виды доз. Единицы дозирования лекарственных средств. Цели дозирования лекарств, способы и варианты введения, интервал введения.
Действие ЛС на организм в большей степени определяется их дозой.
а) разовая доза – количество вещества на один прием
е) загрузочная (вводная) доза – кол-во вводимого ЛС, которое заполняет весь объем распределения организма в действующей (терапевтической) концентрации: ВД = (Css * Vd)/F
ж) поддерживающая доза – систематически вводимое количество ЛС, которое компенсирует потери ЛС с клиренсом: ПД = (Css * Cl * T)/F
Единицы дозирования ЛС:
1) в граммах или долях грамма ЛС
2) количество ЛС в расчете на 1 кг массы тела (например, 1 мг/кг) или на единицу поверхности тела (например, 1 мг/м 2 )
Цели дозирования ЛС:
1) определить количество ЛС, необходимое для того, чтобы вызвать нужный терапевтический эффект с определенной длительностью
2) избежать явлений интоксикации и побочных эффектов при введении ЛС
Способы введения ЛС: 1) энтерально 2) парентерально (см. в. 5)
Варианты введения ЛС:
а) непрерывный (путем длительных внутрисосудистых инфузий ЛС капельно или через автоматические дозаторы). При непрерывном введении ЛС его концентрация в организме изменяется плавно и не подвергается значительным колебаниям
Интервал введения – интервал между вводимыми дозами, обеспечивающий поддержание терапевтической концентрации вещества в крови.
Средства для лечения кандидозов (ч. 2)
Синтетические противогрибковые препараты для наружного применения имеют имеют широкий спектр действия.
Преферанская Нина Германовна
Доцент кафедры фармакологии института фармации им. А.П. Нелюбина Первого МГМУ им. И.М. Сеченова (Сеченовский университет), к.фарм.н.
СИНТЕТИЧЕСКИЕ ПРОТИВОГРИБКОВЫЕ ПРЕПАРАТЫ
Клотримазол (Clotrimazolum), мазь 20 г и 30 г, 1% гель и крем — туба 20 г; табл. вагин. 100 мг — ТН «Кандид» — противогрибковое средство, широкого спектра действия, для наружного применения. Антимикотический эффект Клотримазола связан с нарушением синтеза эргостерола, входящего в состав клеточной мембраны грибов, что изменяет проницаемость цитоплазматической мембраны и вызывает последующий лизис клетки. В малых концентрациях действует фунгистатически, в больших — фунгицидно, причем не только на пролиферирующие клетки. В фунгицидных концентрациях взаимодействует с митохондриальными и пероксидазными ферментами, в результате чего происходит увеличение концентрации перекиси водорода до токсического уровня, что также способствует разрушению грибковых клеток.
Препарат проявляет фунгицидную и фунгистатическую активность в отношении дрожжеподобных и плесневых грибов (Candida spp., включая Candida albicans; Torulopsis glabrata, рода Rhodotorula, Pityrosporum orbiculare). Первично резистентные варианты чувствительных грибов встречаются очень редко. Развитие вторичной резистентности у чувствительных грибов также отмечается в исключительных случаях. При наружном применении после нанесения Клотримазола на интактную или воспаленную кожу он плохо всасывается через кожу и практически не оказывает системного действия. Дозу, способ и схему применения определяют индивидуально, в зависимости от показаний, возраста пациента и применяемой лекарственной формы.
Важно! При применении Клотримазола могут наблюдаться аллергические реакции: сыпь, зуд, волдыри, жжение, раздражение. Противопоказан при повышенной чувствительности к клотримазолу, при беременности и кормлении грудью. При появлении аллергических реакций или раздражения в месте нанесения средства лечение прекращают.
Сертаконазол (Sertaconazolum), 2% р-р 15 мл д/наружн. прим; суппоз. 300 мг; 2% крем, туба 20 г — ТН «Залаин», «Офломикол» — противогрибковое средство, хлорированное производное имидазола и бензотиофена. Механизм действия заключается в подавлении синтеза эргостерола, основного компонента мембран грибковых клеток и в конкурентном антагонизме с другим компонентом клеточной стенки — триптофаном. Это ведет к дезорганизации и увеличению проницаемости клеточной мембраны, деструкции и уничтожению патогенного гриба.
В терапевтических дозах оказывает фунгицидное и фунгистатическое действие. Обладает широким спектром действия в отношении патогенных грибов (Candida spp., в т.ч. Candida albicans, Candida tropicalis) и других патогенных грибов (Pityrosporum orbiculare, Malassezia spp.), а также дерматофитов (Trichophyton и Microsporum), грамположительных бактерий (Streptococcus spp., Staphylococcus spp.), а также Gardnerella vaginalis, Enterococcus faecalis, Bacteroides spp., Trichomonas vaginalis.
Сертаконазол не подавляет жизнеспособность Lactobacillus spp. in vitro.
Показаниями для его применения служат поверхностные микозы кожи, микозы голеней, стоп и кистей; микозы туловища; кандидоз; кандидозный вульвовагинит, разноцветный (отрубевидный) лишай; себорейный дерматит.
Вводят препарат интравагинально, однократно. В период лечения рекомендуется воздерживаться от половых контактов. Не рекомендуется использование кислотных моющих средств, т.к. кислая среда способствует размножению грибов рода Candida.
При применении препарата может возникать местная эритематозная реакция, ощущение жжения, зуд во влагалище, которые проходят самостоятельно во время лечения и не требуют отмены препарата.
Важно! Противопоказанием к применению Сертаконазола служит повышенная чувствительность к производным имидазола, бензотиофена и другим компонентам препарата, при беременности и кормлении грудью.
Миконазол (Miconazolum), 2% крем, туба 15 г — ТН «Микозон» — является хлорированным производным имидазола. Препарат ингибирует биосинтез эргостерола и изменяет липидный состав мембраны, вызывая гибель клетки гриба. Активен в отношении возбудителя разноцветного лишая Malassezia furfur, возбудителей некоторых дерматомикозов(Candida, Trichophyton, Epidermophyton floccosum, Microsporum). Проявляет активность в отношении Aspergillus spp., Dimorphons fungi, Cryptococcus neoformans, Pityrosporum, Torulopsis glabrata, Pseudallescheria boydii. Применяют Миконазол при заболеваниях кожи, вызванных грибами, чувствительными к нему, при кандидоз е слизистой полости рта, глотки и ЖКТ, вагинальных и вульвовагинальных кандидоз ах.
Применяют препарат местно, нанося на пораженные участки кожи 2 раза в день, утром и вечером, мягко втирая крем, возможная реакция — раздражение кожи, контактный дерматит. Дозу устанавливают в зависимости от показаний к применению данной лекарственной формы. Продолжительность курса лечения зависит от вида грибкового заболевания, эффективности лечения и результатов микологических тестов.
Важно! Препарат не рекомендуется применять при беременности и в период лактации.
Важно! При беременности следует применять только после консультации с врачом, в тех случаях, когда предполагаемая польза для матери превышает потенциальный риск для плода. В период лечения необходимо решить вопрос о прекращении грудного вскармливания.
Бутоконазол (Butoconazolum) 2% крем вагин., аппликатор 5 г — ТН «Гинофорт» — является производным имидазола, оказывает противогрибковое действие, блокирует в клеточной мембране гриба образование эргостерола из ланостерола, повышает проницаемость мембраны, что приводит к лизису клетки гриба. Препарат обладает фунгицидной активностью против грибов типа Candida, Trichophyton, Microsporum, Eridermaphyton и некоторых грамположительных бактерий; наиболее эффективен при кандидозах — при интравагинальном применении один аппликатор вводится во влагалище в любое время суток. Бутоконазол находится на слизистой влагалища, в течение 4–5 дней.
При применении препарата могут возникать жжение, зуд, болезненность и отек стенки влагалища, боли/спазмы в нижней части живота.
Фентиконазол (Fenticonazolum) — капс. вагин. 600 мг и 1000 мг, 2% крем вагин. — 30 г и 78 г — ТН «Ломексин» — является хлорированным производным имидазола с противогрибковым действием — ингибирует синтез эргостерола, нарушая проницаемость клеточной стенки гриба. Препарат активен в отношении Candida spp. (включая Candida albicans) и грамположительных бактерий (Staphylococcus aureus, Streptococcus spp.), а также в отношении Trichomonas vaginalis. В отличие от других известных азольных соединений препарат показан при вульвовагинальном кандидоз е, вагинальном трихомониазе; интравагинально 1–2 раза/сут. в течение 3–6 дней.
Важно! Не применять препарат во время менструации. Курс лечения целесообразно начинать после ее окончания. Применение в I триместре беременности противопоказано.
Итраконазол (Itraconazolum), капс. 100 мг, табл. вагин. 200 мг, р-р 10 мг/мл —150 мл — ТН «Орунгал», «Румикоз» — является синтетическим производным триазола, механизм действия которого заключается в ингибировании биосинтеза эргостерола — основного компонента клеточной мембраны гриба, участвующего в поддержании структурной целостности мембраны. Нарушение синтеза эргостерола приводит к изменению проницаемости мембраны и лизису клетки, что и обуславливает противогрибковый эффект препарата. Активен в отношении дерматофитов. Некоторые штаммы могут быть устойчивы: Candidaglabrata, Candidakrusei, Candidatropicalis, Absidiaspp., Fusariumspp., Mucorspp., Rhizomucorspp., Rhizopusspp., Scedosporiumproliferans, Scopulariopsisspp.
Эффективность лечения при микозах оценивается через 2–4 недели после прекращения терапии. Терапевтическая концентрация итраконазола в коже сохраняется в течение 2–4 недель после прекращения 4–недельного курса лечения.
Препарат применяют при вульвовагинальном кандидозе; дерматомикозе, разноцветном лишае, кандидозе слизистой оболочки полости рта, кератомикозе; онихомикозе, вызванный дерматофитами или дрожжеподобным грибами, а также при системных микозах — системный аспергиллез или кандидоз, криптококкоз (в т.ч. криптококковый менингит) у иммунокомпрометированных лиц и криптококкоз центральной нервной системы, бластомикозе, споротрихозе, паракокцидиоидозе, прочие редко встречающиеся системные и тропические микозы.
Важно! При применении препарата могут возникать побочные эффекты: диспептические расстройства, токсическое поражение печени, аллергические реакции, головная боль, головокружение и др. Какого–либо специфического антидота для Итраконазола не существует.
Флуконазол (Fluconazolum) капс. 50 г и 150 г; р-р д/в/в. инфуз. 2 мг/мл — 50 мл, 100 мл и 150 мл — ТН «Дифлюкан», «Флюкостат», «Микосист» — является производным триазола, мощным селективным ингибитором синтеза стеролов в клетке грибов.
Флуконазол активен в отношении большинства микроорганизмов: Candida albicans, Candida glabrata (многие штаммы умеренно чувствительны), Candida parapsilosis, Candida tropicalis, Cryptococcus neoformans.
Препарат имеет большой спектр применения (см. инструкцию).
Режим дозирования индивидуальный. Длительность лечения зависит от клинического и микологического эффекта. Длительный период полувыведения из плазмы крови позволяет принимать флуконазол при вагинальном кандидозе однократно 1 раз/сут. или 1 раз/нед. — при других показаниях. Флуконазол хорошо проникает во все жидкости организма. Уровни флуконазола в слюне и мокроте сходны с его концентрациями в плазме крови. Флуконазол обладает высокой специфичностью в отношении грибковых ферментов, зависимых от цитохрома Р450, что может сопровождаться повышением сывороточных концентраций тех средств, с которыми он принимается. При таких комбинациях следует тщательно контролировать состояние пациентов.
Важно! При применении могут возникать побочные эффекты: диспептические расстройства, токсическое поражение печени, аллергические реакции, головная боль, головокружение, бессонница, сонливость, тремор, алопеция, лекарственная сыпь, аллергические реакции, нарушения со стороны органов кроветворения, ССС, слабость, повышенная утомляемость.
С осторожностью применяют при нарушениях функции печени и функции почек.
Каприловая кислота (БАД, производитель NPS, США) — представляет собой особый тип полезной насыщенной жирной кислоты, которая обладает антибактериальными, противовирусными, противогрибковыми и противовоспалительными свойствами. Ее считают одной из трех основных жирных кислот (каприновой, лауриновой), найденных в кокосовом масле.
Каприловую кислоту также иногда называют октановой кислотой, ведь она содержит восемь атомов углерода, что делает ее жирной кислотой со средней длиной цепи. В последнее время каприловая кислота стала широко известна своими противогрибковыми эффектами, особенно в отношении поддержания функций пищеварения и здоровья половых органов, в т.ч. мочевого пузыря, кишечника и мочеиспускательного канала. Эту кислоту применяют для профилактики инфекций мочевых путей, мочевого пузыря, инфекции кандида, инфекций, передаваемых половым путем, таких инфекций полости рта, как гингивит и мн. др. Она препятствует разрастанию дрожжеподобных грибов, которые могут жить и размножаться в кишечнике. Кислота может проникать в клеточные мембраны дрожжей Candida, заставляет их отмирать, выводит токсины из желудочно-кишечного тракта и ускоряет процесс заживления.
Каприловая кислота при приеме внутрь быстро уменьшает симптомы, связанные с вирусными и грибковыми инфекциями, такие как Candida и хламидии. Помимо Candida дрожжи могут вызвать другие типы внутренних или внешних дрожжевых инфекций, которые проявляются на коже, половых органах, пальцах ног и других местах. Эта кислота избавляет от дрожжевых инфекций грибка на большом пальце ноги, инфекции полости рта, вагинита у женщин и стригущего лишая.
Специалисты рекомендуют принимать капс. от 500 до 1000 мг три раза в день в форме капсул для достижения оптимального результата.
Прием каприловой кислоты необходимо начинать медленно, чтобы предотвратить боли в желудке. Капсула 500 мг 1–2 раза в день рекомендуется в начале, а затем дозировка увеличивается по мере самочувствия по времени от трех до четырех месяцев, пока состояние не улучшится. Считается, что медленное увеличение дозировки помогает эффективно устранить дрожжевую инфекцию, не навредив организму с аутоиммунной реакцией.
Важно! БАД не рекомендуется к применению беременным женщинам, кормящим грудью, при заболеваниях печени, гипотонии или дефицитом ацил-КоА-дегидрогеназы жирных кислот.
Перед применением необходимо сделать проверку на аллергию и обязательно проконсультироваться с вашим лечащим врачом.