Щелочная вода
Измерение рН указывает на то, каким является раствор: кислым (рН рН)

Давайте разберем, что такое кислотно-щелочной баланс и почему важно его контролировать в организме?
Кислотно-Щелочной баланс
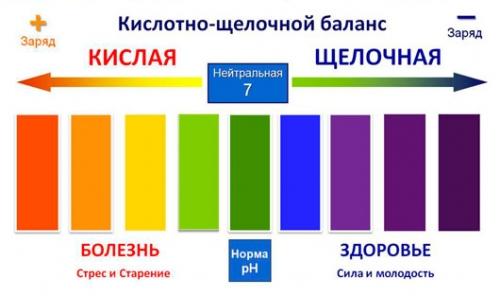
Кислотно-щелочной баланс (рН) это соотношение кислоты и щелочи в жидкости. А так как наш организм состоит на большую часть из воды, то этот показатель является очень важным.
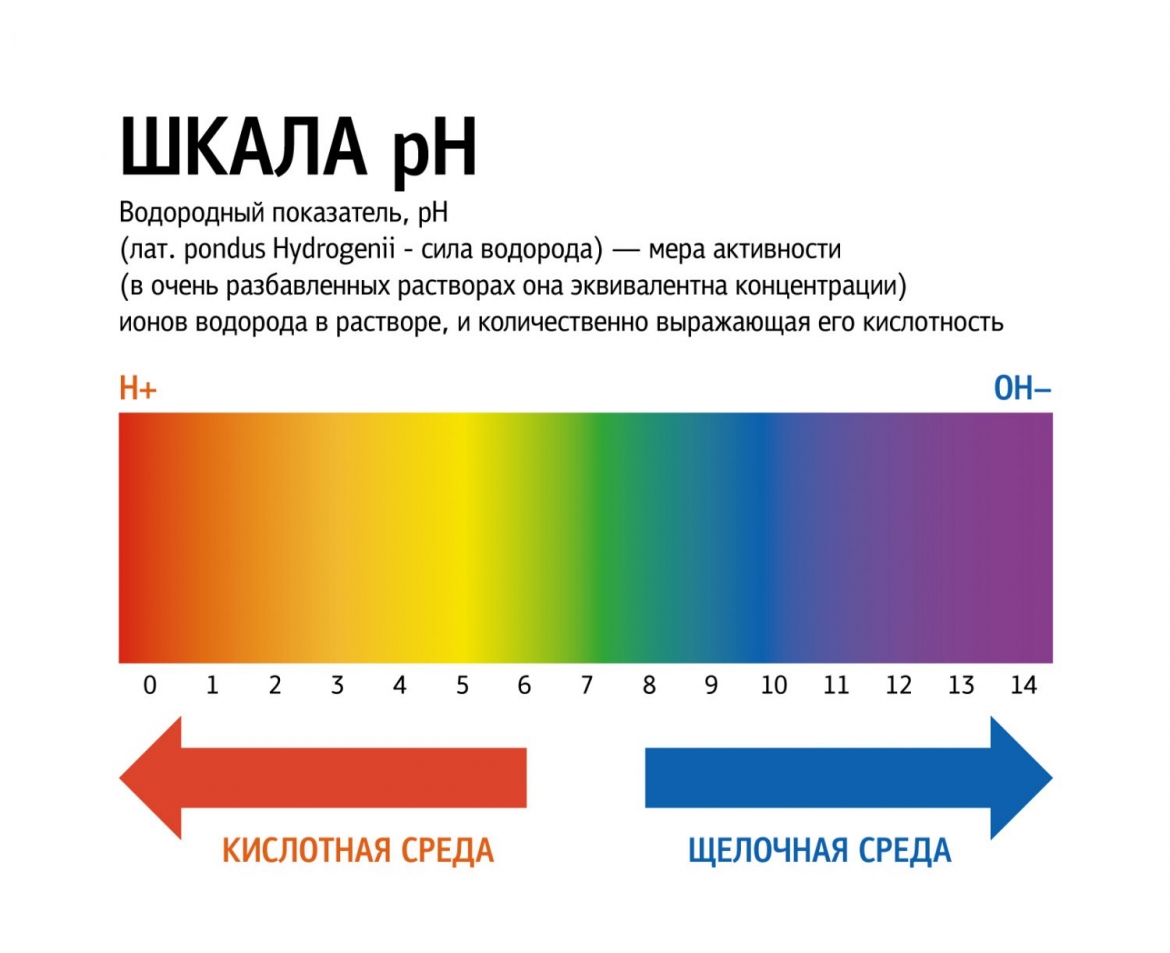
Показатель рН жидкости зависит от соотношения положительно заряженных ионов (Н+),образующими кислую среду и отрицательно заряженных ионов (-ОН), образующих щелочную среду.

Баланс рН так же называют водородным показателем, чем больше положительных ионов водорода (Н+) тем кислее среда, чем меньше количество ионов водорода, тем среда щелочнее.
Обычная питьевая вода в основном имеет сбалансированный уровень положительных и отрицательных ионов (рН = 7) из-за внешнего атмосферного воздействия. Но если в воду добавить различные вкусовые добавки, красители или газы, ее среда станет кислой.
Какой рН в организме человека
Организм человека состоит на большую часть из воды, поэтому важно контролировать баланс рН. В человеке находиться две среды: кислая и щелочная. Кислая среда необходима для химических процессов, например, пищеварения. Но в остальном уровень рН организма слабощелочной. Природой установлено, что щелочной среды должно быть в 4 раза больше кислой. Если происходит нарушение этого баланса, то возникают различные заболевания.

Все регулирующие процессы организма (дыхание, метаболизм, образование гормонов) направлены на выравнивание уровня рН. Такой процесс достигается путем выведения кислых остатков из клеток и тканей. Чтобы снизить кислотность, организм забирает кальций и другие необходимые минералы из костей и тканей, для ощелачивания кислотности. Поэтому при сильном окислении организма важно употреблять продукты содержащие важные минералы (кальций, магний, калий).
Значительное защелачивание организма так же возможно. Оно несет своеобразные нарушения в процессах организма, но организму намного легче справиться с такой задачей, чем с закислением внутренней среды. Снижение кислоты в организме требует больших энергозатрат и ресурсов, а учитывая то, что организм постоянно находиться в процессах окисления, то в регулирующих процессах и системах происходят перегрузки.
Нарушенный баланс кислот и щелочей – фактор развития болезней
В современном мире, закисление организма встречается у 7 из 10 человек, такое заболевание называется Ацидоз.
При закислении организма, в органах и мышцах накапливаются кислотные отходы, а необходимые минералы плохо усваиваются и быстро выводятся. Это приводит к блокировке биохимических и энергетических процессов в клетках, в итоге они погибают. Затвердевшие кислотные отходы заполняют капиллярные сосуды, из-за чего органы не дополучают достаточно крови, а с ней и питательных веществ. Последствием чего является гипертония, заболевание почек, сахарный диабет, онкологические и многие другие заболевания.

Причиной сильного закисления организма является постоянное потребление кислотообразующих продуктов питания, в то время как продукты, образующие щелочь (овощи и фрукты), все реже встречаются в нашем рационе. Все без исключения белковые, морские, мучные, молочные, алкогольные и сладкие продукты являются сильно кислыми.
Щелочными продуктами являются овощи, фрукты и зелень. Поэтому важно балансировать свое питание, о чем говорят нам все врачи и диетологи. По мимо питания, на закисление организма влияет: плохая экология, малоподвижный образ жизни и вредные привычки.
Процесс закисления происходит постепенно в несколько этапов:
Восстановить баланс рН поможет щелочная вода
Основная часть потребляемой пищи образует кислую среду, благодаря чему, наш организм постоянно находится в состоянии окисления. Чтобы помочь ему, необходимо дополнительное употребление щелочных продуктов. Основных решением снятия закисления организма является щелочная вода.
Потребление щелочной воды в значительной степени нейтрализует кислую среду, тем самым стабилизируется рН баланс, необходимый для нормальной работы жизненно важных процессов.

При стабилизации баланса рН, организм постепенно начинает приводить в ному вес. Это связано с тем, что при закислении, в организме начинают накапливаться жировые клетки для хранения кислых отходов. После достижения слабощелочного баланса рН, необходимость в жировых клетках теряется и организм начинает их сжигать, в результате происходит нормализация веса и похудение.
Врачи рекомендуют при ацидозе принимать щелочную воду, потому что это эффективный способ снять окислительный стресс. На рынке есть огромное количество разнообразных видов щелочной воды с разным показателем рН, начиная от 7,5 и выше.
Как сделать перевод статьи на русский?
Щелочная вода: история и медицинское заключение
Данные всемирной организации здравоохранения, определяют показания рН следующим образом:
Вредность щелочной воды. Есть ли обратная сторона медали?
Существует много противников щелочной воды, которые говорят о ее вреде и в определенном смысле они правы. Щелочность воды в основном определяется насыщенностью щелочных солей.
Есть щелочные воды, которые имеют показатель рН выше 9,5 (сильнощелочная вода). Такая вода необходима в ограниченных количествах если у Вас наблюдается сильное закисление организма (Ацидоз). Но если у Вас не наблюдается Ацидоза, а есть только небольшое закисление, то постоянное потребление сильнощелочной воды может нарушить баланс рН и нанести вред для Вашего организма.
При постоянном потреблении сильнощелочной воды можно привезти организм к заболеванию Алкалоз (защелачивание организма) прямо противоположному от ацидоза заболеванию.
В связи с этим, уровень рН является важным фактором щелочной воды. Полезно и без вреда, на постоянной основе, можно и нужно потреблять слабощелочную воду с показателями от 7.1 до 8.0 рН Такая вода будет максимально полезна и способна поддерживать баланс рН на нужном уровне для организма. Именно слабощелочная вода соответствует внутренней среде человека, и не оказывает нагрузку на организм.
Какая щелочная вода подойдет именно Вам? Возможно ли сделать воду щелочной в домашних условиях?
Щелочная вода в домашних условиях
Существует много способов как сделать щелочную воду для питья дома. Каждый способ имеет свои преимущества и недостатки. В основном, ощелачивание воды основано на обогащении воды щелочными минералами. Давайте разберем какой способ подойдет именно Вам.
1. Пищевая сода. Самый простой и дешевый способ сделать щелочную воду это разбавить пищевую соду с водой и хорошо размешать. Сода имеет высокое содержание щелочи. Но будьте осторожны с количеством соды, при переизбытке соды Ваше самочувствие может ухудшиться.
2. pH капли. Существуют специальные рН капли, предназначенные менять щелочность воды. Они состоят из высококонцентрированных щелочных минералов. Такие капли хоть и подщелачивают воду, но они не меняют структурных и биофизических свойств.
3. Электролиз воды. При помощи электролиза воды, вода делиться на две части, с положительно заряженными ионами и отрицательно заряженными ионами. Вода с отрицательно заряженными ионами имеет щелочную среду, где рН может достигать 10. Вода с положительными ионами является кислой, которая способна убивать разные типы бактерий. Такой водой можно протирать раны и кожу. Стоимость таких приборов очень высокая.
4. Щелочной фильтр для воды. Проходя через фильтры, вода очищается и в конце попадает в емкость с щелочными минералами, где обретает щелочную среду. Фильтры для воды дешевле чем приборы электролиза, но их требуется постоянно заменять.
5. Щелочные минералы. Существуют разные минералы, которые способны ощелачивать воду. В основном они содержат натрий, магнезию, гидрокарбонатные ионы. При постоянном потреблении воды с переизбытком щелочных минералов, может произойти обратный эффект.
6. Химическая реакция с металлами. Самый эффективный, недорогой и естественный способ получения щелочной воды с большим содержанием растворенного водорода. Щелочную воду можно получить при при помощи щелочноземельных металлов, таких как Магний, Кальций, Натрий и д.р.
Научные исследования щелочной воды
Однако публикаций о пользе щелочной воды полученной другим способом отличным от электролиза мы не обнаружили. В основном пишут, что щелочная вода при потреблении меняет только рН мочи и не влияет кислотно-щелочной баланс крови и органов, это говорит о том, что полезного эффекта не наблюдается.
Следовательно, польза щелочной воды будет только при условии, что она будет содержать молекулярный водород, который имеет доказанный терапевтический эффект.
Значение слова ЩЁЛОЧЬ. Что такое ЩЁЛОЧЬ?
Свойства щелочей
Щелочи — твердые вещества белого цвета; гигроскопичные, водорастворимые. Растворение в воде сопровождается активным выделением тепла. Вступают в реакции с кислотами, образуя соль и воду. Эта реакция нейтрализации является важнейшей из всех свойств щелочей. Кроме этого, гидроксиды реагируют с кислотными оксидами (образующими кислородосодержащие кислоты), с переходными металлами и их оксидами, с растворами солей.
Гидроксиды щелочных металлов растворяются в метиловом и этиловом спиртах, способны выдерживать температуры до +1000 °С (за исключением гидроксида лития).

Если сравнивать щелочи по химической активности, то она увеличивается при движении по столбцу таблицы Менделеева сверху вниз.
Концентрированные щелочи разрушают стекло, а расплавы щелочей — даже фарфор и платину, поэтому растворы щелочей не рекомендуется хранить в сосудах с пришлифованными стеклянными пробками и кранами, так как пробки и краны может заклинить. Хранят щелочи, обычно, в полиэтиленовых емкостях.
Именно щелочи, а не кислоты, вызывают более сильные ожоги, так как их сложнее смыть с кожи и они проникают глубоко в ткань. Смывать щелочь надо неконцентрированным раствором уксусной кислоты. Работать с ними необходимо в средствах защиты. Щелочной ожог требует немедленного обращения к врачу!
Видео
Что такое щелочь?
Щелочь — это те вещества, которые хорошо растворяются в воде. При этом реакция сопровождается с выделением тепла, с увеличением температуры. Если щёлочь сравнивать с кислотой, то на ощупь она намного «мыльнее», то есть скользкая. Вообще, щёлочи не сильно отстают от кислот по разъеданию и по силе. Они также могут с лёгкостью разъесть древесину, пластик, одежду и тому подобное.
Кстати, из щёлочей делают мыло, стекло, бумагу, ткань и это не весь список. Щёлочь можно найти у себя на кухне, ну или в магазине под названием пищевая сода. Кстати, пищевая сода это очень хороший помощник всем домохозяйкам.
Применение оснований
Нашатырный спирт используют не только для того, чтобы привести человека в сознание. С его помощью можно отлично вымыть окна, используя 1 столовую ложку препарата на 1 литр воды. Затем нужно вытереть поверхность бумажными полотенцами.
Если смешать 1 часть нашатырного спирта с 1 частью уксуса, а потом протирать полученным раствором поверхность утюга, то он станет чистым. Но не стоит думать, что получится мгновенный эффект. Поверхность нужно аккуратно потереть.
Широко применяют, прежде всего, гидроксиды кальция и натрия. Гашёная известь – это гидроксид кальция Сa(OH)2. Её используют, как вяжущий материал в строительстве. Смешивают с песком и водой. Полученную смесь наносят на кирпич, штукатурят стены. В результате взаимодействия основания с углекислым газом и оксидом силициума (IV), смесь твердеет. Известь способна поглощать кислые газы. Также может впитывать токсичные вещества, поэтому для здоровья жильцов белить комнату предпочтительнее, чем красить.
Также гидроксид кальция используют в сахарной промышленности, сельском хозяйстве, при изготовлении зубных паст, получении многих веществ.
Гидроксид натрия (каустическую соду) используют при производстве мыла в реакции щёлочи с жиром, при изготовлении лекарств, в кожной промышленности, для очищения нефти. Каустическая сода применяется для чистки масляных пятен. Всем известный «Крот» для труб представляет собой раствор гидроксида натрия, способный растворять жиры и даже волосы.
Щёлочи разъедают стекло и фарфор. Растворяют белковые вещества.
Применяются в медицине в качестве антисептиков, раздражающих и прижигающих препаратов. При заболеваниях пищеварительной системы щелочные минеральные воды действуют оздоравливающе. Эффективны в лечении подагры, стоматита, в лечении заболеваний дыхательной системы. Являются мочегонным средством. Нейтрализуют отравление кислотами.
Немаловажно участие щелочей в изготовлении каучука, искусственного волокна, красителей, очищения предметов из металла, обработки деревянных поверхностей. Являются хладагентом холодильных установок. Используются в сельском хозяйстве, лёгкой промышленности и металлургии.
Сильные кислоты и слабые кислоты
Есть некоторые кислоты, которые мы можем употреблять, в то время как работа с другими предполагает строгие меры безопасности.
Сильные кислоты — это те, которые полностью диссоциируют или ионизируются в водных растворах.
Один из способов визуализировать, как отличить слабые и сильные кислоты, по аналогии с игроками в регби:
Примеры сильных кислот
Среди известных сильных кислот выделяют:
Примеры слабых кислот
Обычно кислоты органических соединений известны как слабые:
Безопасность в работе со щелочами
Химические ожоги, причиняемые щелочами, в том числе едким натром и едким кали, намного опаснее, чем химические ожоги от кислот. Ожог усугубляется, если кусочек кристаллического вещества прилипает к коже.
Щёлочи способны разъедать много материалов, вызывать серьёзные ожоги на коже и слизистых оболочках, поражать глаза. Поэтому гидроксид натрия называют «едким натром», а гидроксид калия – «едким кали». При работе со щелочами и их растворами, нужно соблюдать осторожность. При попадании раствора щелочи на кожу, нужно сразу смыть его большим количеством воды. Затем обработать это место слабым раствором уксусной или борной кислоты. И опять промыть водой.
Химические свойства
Поглощают H2O и CO2 из воздуха. Щёлочи широко применяются в промышленности. Важное химическое свойство щелочей — способность образовывать соли в реакции с кислотами.
Чем отличаются кислоты от щелочей
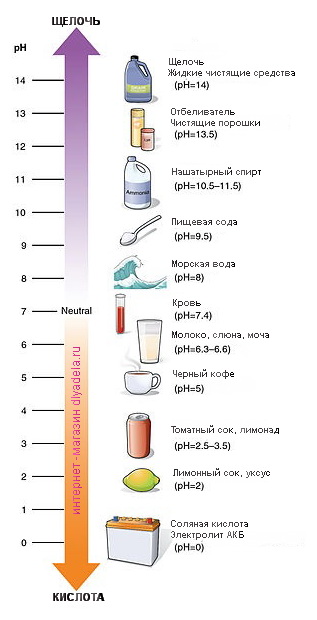
Кислоты и щёлочи отличают по показателям pH (шкала pH). Ниже Вы видите картинку – это специальная шкала, на которой имеются числа от 0 и до 14. Нулём обозначают самые сильные кислоты, а четырнадцатью – самую сильную щёлочь. Но какая же середина между этими числами? Может быть 5, может быть 7, а может быть 10? Серединой принято считать число 7 (нейтральное положение). То есть числа до 7 это все кислоты, а больше 7 это щёлочи.
Именно для этой шкалы разработаны специальные индикаторы — лакмусы. Это обычная полоска, которая реагирует на среду. В кислотной среде она окрашивается в красный цвет, а в щелочной среде – в синий цвет. Она необходима не только в химии, но и в быту.
Например, если у Вас есть аквариум, то немаловажную роль играет кислотность воды. От неё зависит вся жизнь аквариума. К примеру, показатель кислотности воды для аквариумных рыбок колеблется от 5 до 9 рН. Если будет больше или меньше, то рыбка будет чувствовать себя не комфортно, а может и вовсе умереть. Всё тоже самое и с растениями для аквариумов…
Кислоты
Кислоты — это соединения, содержащие водород и образующие ионы водорода (Н+) при растворении в воде. Ионы — это частицы с электрическим зарядом (см. статью «Химические связи»). Именно ионы придают кислотам их свойства, но существовать они могут только в растворе. Следовательно, свойства кислот проявляются исключительно в растворах. Молекула серной кислоты (H2SO4) состоит из атомов водорода, серы и кислорода. В состав соляной кислоты (НСl) входят водород и хлор. Кислота считается сильной, если большинство ее молекул распадаются в растворе, выделяя ионы водорода. Соляная, серная, азотная кислоты относятся к сильным. На контейнерах с сильными кислотами ставятся принятые во всем мире символы, означающие «опасно» и «высокая активность»Сила кислоты измеряется числом рН — водородным показателем. Сильные кислоты очень агрессивны; попав на поверхность предмета или на кожу, они прожигают её. На контейнерах с сильными кислотами ставятся принятые во всем мире символы, означающие «опасно» и «высокая активность».
Такие кислоты, как лимонная или уксусная, т.е. произведенные живыми организмами, называются органическими. Кислоты широко применяются в химической и медицинской промышленности, в производстве продуктов питания и синтетических волокон. Виноградный уксус содержит слабую кислоту, называемую уксусной. В помидорах есть органическая салициловая кислота. В цветных пятнах на коже морских улиток содержится кислота с неприятным вкусом, отпугивающая хищников. Для всех кислот характерно сходное поведение в химических реакциях. Например, при реакциях кислот с основаниями образуется нейтральное соединение — соль и вода. Реакции кислот с большинством металлов дают соль и водород. Реагируя с карбонатами, кислоты дают соль, углекислый газ и воду. Известный кулинарам пекарный порошок содержит гидрокарбонат натрия и винную кислоту. Когда в муку, содержащую пекарный порошок, добавляют воду, кислота и карбонат порошка вступают в реакцию, углекислый газ начинает выделятся в виде пузырьков, и это помогает тесту подниматься.
рН и индикаторы
Сила кислот и оснований определяется числом рН. Это мера концентрации ионов водорода в растворе. Число рН изменяется от 0 до 14. Чем меньше рН, тем выше концентрация водородных ионов. Раствор, рН которого меньше 7, — кислота. Апельсиновый сок имеет рН 4, значит, это кислота. Вещества с рН = 7 нейтральны, а вещества с рН больше 7 — основания или щелочи. рН кислоты или щелочи можно определить с помощью индикатора. Индикатор — это вещество, меняющее цвет при контакте с кислотой или щелочью. Так лакмус краснеет в кислоте и синеет в щелочи. Кислота окрашивает синюю лакмусовую бумажку в красные цвет, а красная лакмусовая бумажка в щелочи становится синей или фиолетовой. Лакмус получают из примитивных растений, называемых лишайниками. Другие растения, например, гортензия и краснокочанная капуста, также являются природными индикаторами.
Так называемый универсальный индикатор – это смесь нескольких красок. Он меняет цвет в зависимости от pH вещества. Он становится красным, оранжевым или желтым в кислотах, зеленым или желтым в нейтральных растворах и синим или фиолетовым в щелочах.
Серная кислота
Серная кислота играет важную роль в промышленности, прежде всего в производстве удобрений на основе суперфосфатов и сульфата аммония. Она также используется в производстве синтетических волокон, красителей, пластмасс, лекарств, взрывчатых веществ, моющих средств, автомобильных аккумуляторов. Когда-то серную кислоту называли минеральной кислотой, так как ее получали из серы — вещества, встречающегося в земной коре в виде минерала. Серная кислота очень активна и агрессивна. При растворении в воде она выделяет много тепла, поэтому ее нужно вливать в воду, но не наоборот — тогда кислота растворится, а вода поглотит тепло. Она — мощный окислитель, т.е. при реакциях окисления она отдает кислород другим веществам. Серная кислота также является осушителем, т.е. забирает воду, связанную с другим веществом. Когда сахар (C12H22O11) растворяется в концентрированной серной кислоте, кислота забирает у сахара воду, и от сахара остается пенящаяся масса черного угля.
Кислоты в почве
Цветы гортензии на кислотной почве синие, а на щелочной — розовыеКислотность почвы зависит от характера образовавших ее пород и от растущих на ней растений. На меловых и известняковых породах почва обычно щелочная, а на лугах, в песчаных и лесистых районах она более кислая. Кислотность также повышают кислотные дожди. Для земледелия лучше всего подходят нейтральные или слабокислые почвы, рН которых от 6,5 до 7. Разлагаясь, мертвые листья образуют органическую гуминовую кислоту и повышают кислотность почвы. Там, где почвы чересчур кислотные, в них добавляют измельченный известняк или гашеную известь (гидроксид кальция), т.е. основания, которые нейтрализуют кислоты почвы. Такие растения, как рододендроны и азалии хорошо растут на кислотных почвах. Цветы гортензии на кислотной почве синие, а на щелочной — розовые. Гортензия – природный индикатор. На кислотных почвах её цветы синие, а на щелочных розовые.
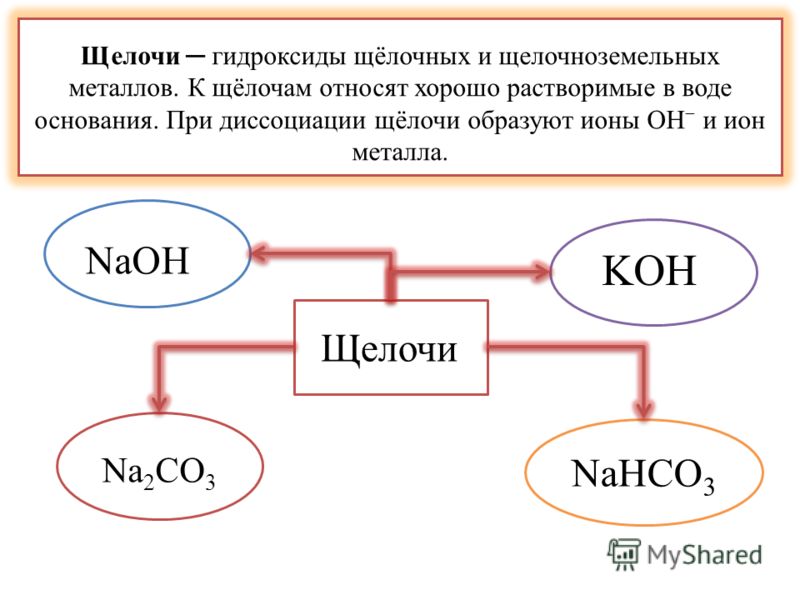
В настоящее время в химии принята теория Брёнстеда — Лоури и Льюиса, которая определяет кислоты и основания. В соответствии с этой теорией, кислоты — это вещества, способные отщеплять протон, а основания — отдавать электронную пару OH−. Можно сказать, что под основаниями понимают соединения, которые при диссоциации в воде образуют только анионы вида OH−. Если совсем просто, то щелочами называют соединения, состоящие из металла и гидроксид-иона OH−.
К щелочам принято относить гидроксиды щелочных и щелочно-земельных металлов. Все щелочи — это основания, но не наоборот, нельзя считать определения «основание» и «щелочь» синонимами.
Правильное химическое название щелочей — гидроксид (гидроокись), например, гидроокись натрия, гидроксид калия. Часто употребляются также названия, которые сложились исторически. Ввиду того, что щелочи разрушают материалы органического происхождения — кожу, ткани, бумагу, древесину, их называют едкими: например, едкий натр, едкий барий. Однако понятием «едкие щелочи» химики определяют гидроксиды щелочных металлов — лития, натрия, калия, рубидия, цезия.
Свойства щелочей
Щелочи — твердые вещества белого цвета; гигроскопичные, водорастворимые. Растворение в воде сопровождается активным выделением тепла. Вступают в реакции с кислотами, образуя соль и воду. Эта реакция нейтрализации является важнейшей из всех свойств щелочей. Кроме этого, гидроксиды реагируют с кислотными оксидами (образующими кислородосодержащие кислоты), с переходными металлами и их оксидами, с растворами солей.
Гидроксиды щелочных металлов растворяются в метиловом и этиловом спиртах, способны выдерживать температуры до +1000 °С (за исключением гидроксида лития).
Гидроксид натрия (едкий натр) используется в чистящих жидкостях, а также (как и гидроксид калия) для производства мыла. Мыло — это соль, образующаяся при реакции щелочей с кислотами растительных жиров. Жало осы выпускает щелочь, которую можно нейтрализовать кислотой, например уксусом.
Щелочи — активные химические реагенты, поглощающие из воздуха не только водяные пары, но и молекулы углекислого и сернистого газа, сероводорода, диоксида азота. Поэтому хранить гидроксиды следует в герметичной таре или, например, доступ воздуха в сосуд со щелочью организовать через хлоркальциевую трубку. В противном случае хим.реактив после хранения на воздухе будет загрязнен карбонатами, сульфатами, сульфидами, нитратами и нитритами.
Если сравнивать щелочи по химической активности, то она увеличивается при движении по столбцу таблицы Менделеева сверху вниз.
Концентрированные щелочи разрушают стекло, а расплавы щелочей — даже фарфор и платину, поэтому растворы щелочей не рекомендуется хранить в сосудах с пришлифованными стеклянными пробками и кранами, так как пробки и краны может заклинить. Хранят щелочи, обычно, в полиэтиленовых емкостях.
Именно щелочи, а не кислоты, вызывают более сильные ожоги, так как их сложнее смыть с кожи и они проникают глубоко в ткань. Смывать щелочь надо неконцентрированным раствором уксусной кислоты. Работать с ними необходимо в средствах защиты. Щелочной ожог требует немедленного обращения к врачу!
Применение щелочей
— В качестве электролитов.
— Для производства удобрений.
— В медицине, химических, косметических производствах.
— В рыбоводстве для стерилизации прудов.
Едкий натр. Самая популярная и востребованная в мире щелочь. Применяется для омыления жиров в производстве косметических и моющих средств, для изготовления масел в процессе нефтепереработки, в качестве катализатора и реактива в химических реакциях; в пищепроме.
Едкое кали. Применяется для производства мыла, калийных удобрений, электролитов для батареек и аккумуляторов, синтетического каучука. Также — в качестве пищевой добавки; для профессиональной очистки изделий из нержавеющей стали.
Гидроксид алюминия. Востребован в медицине как отличный адсорбент, антацид, обволакивающее средство; ингредиент вакцин в фармацевтике. Кроме этого, вещество применяется в очистных сооружениях и в процессах получения чистого алюминия.
Гидроокись кальция. Популярная щелочь с очень широким спектром применения, которую в быту знают под названием «гашеная известь». Используется для дезинфекции, смягчения воды, в производстве удобрений, едкого натра, «хлорки», строительных материалов. Применяется для защиты деревьев и деревянных сооружений от вредителей и огня; в пищепроме как пищевая добавка и реактив при производстве сахара.
Гидроокись лития. Востребованное соединение в химпроме как сырье; в стекольной, керамической, Фиксаналырадиотехнической индустрии; для производства смазочных материалов, электролитов; для поглощения вредных газов.
Гидроокись бария. Применяется в химпроме как катализатор, а также в пищепроме для очистки жиров, сахара.
• Кислоты и щелочи неспособны мирно сосуществовать даже одну секунду, находясь в соприкосновении. Перемешавшись, они мгновенно начинают бурное взаимодействие. Химическая реакция с ними сопровождается шипением и разогревом и длится до тех пор, пока эти ярые антагонисты не уничтожат друг друга.
• Кислотам свойственно образовывать кислую среду, а щелочам – щелочную.
• Химики отличают щелочь от кислоты по ее поведению с лакмусовой бумажкой или фенолфталеином.