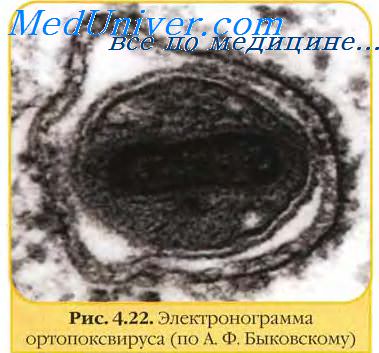
Какой генетический материал содержит вирус оспы
Геном вирусов оспы представлен одной линейной молекулой двуцепочечной ДНК с ковалентно замкнутыми концами размером 130 тпн (парапоксвирусы) — 280 тпн (авипоксвирусы). На обоих концах генома имеются идентичные, но противоположно ориентированные тандемы повторяющихся нуклеотидных последовательностей. Геномы вирусов оспы способны кодировать около 200 белков, из которых не менее 100 входят в структуру вириона. Однако функциональные особенности определены лишь у небольшого количества вирусных белков. Наиболее важными из них являются ферменты, участвующие в синтезе вирусных нуклеиновых кислот и структурных компонентов вирионов. Например, синтез ДНК-полимеразы, ДНК-лигазы, РНК-полимеразы, энзимов, связанных с кэппированием и полиаденилированием мРНК и тимидинкиназы.
Инфекционные вирусные частицы содержат системы транскрипции, которые могут выполнять in vitro синтез РНК, а также способны полиаденилировать, кэппировать и метилировать. В вирусных частицах содержится большое количество кодируемых вирусом энзимов и других биологически активных факторов.
Некоторые гены вирусов оспы кодируют белки, которые секретируются инфицированными клетками и вызывают ответ организма на инфекцию, в том числе и формирование иммунитета.
К таким вирокинам относятся гомологичный эпидермальный фактор роста, белок, снижающий активность комплемента, вирокины, обеспечивающие устойчивость к интерферону, и другие супрессоры иммунного ответа, подавляющие действие некоторых цитокинов организма хозяина.
Вирусы оспы обычно характеризуются узким спектром хозяев. Они передаются чаще респираторным путем и реже через поврежденную кожу. Вирусы оспы овец, свиней, птиц и миксоматоза передаются также через укус членистоногими. Вирусы оспы устойчивы в окружающей среде и могут сохраняться годами в высохших струпьях кожи или других вируссодержащих материалах.
Большинство вирусов оспы хорошо размножаются в культуре клеток. Исключение составляют парапоксвирусы, вирус оспы свиней и вирус контагиозного моллюска. Однако они, так же как и ортопоксвирусы, легко образуют оспины на хориоал-лантоисной оболочке куриных эмбрионов.
Вирусы оспы размножаются в цитоплазме, и, в отличие от других ДНК-вирусов, их размножение происходит независимо от ядра клетки, благодаря кодированию всех ферментов, необходимых для транскрипции и репликации вирусного генома. Некоторые из этих функций выполняются вирионами как таковыми. После слияния оболочки вириона с плазматической мембраной клетки или после эндоцитоза вирусная сердцевина освобождается в цитоплазму. Транскрипция вирусного генома характеризуется каскадностью, когда каждый временной класс генов («ранние», «промежуточные» и «поздние» гены) требует наличия специфических транскрипционных факторов, которые создаются предшествующим временным классом генов. Факторы, обеспечивающие транскрипцию промежуточных генов, кодируются ранними генами, тогда как факторы транскрипции поздних генов кодируются промежуточными генами. Транскрипция начинается вирионной транскриптазой и другими факторами, находящимися в сердцевине вириона, которые способны образовывать мРНК спустя минуты после инфицирования.
Белки, образующиеся в результате трансляции этих мРНК, включая ДНК-полимеразу, тимидинкиназу и несколько других ферментов, необходимы для репликации вирусной ДНК. Репликация ДНК ВО связана с синтезом конкатемерных промежуточных структур, которые затем разрезаются с образованием единиц геномной длины. Детали этого процесса недостаточно изучены. С началом репликации ДНК происходит резкий сдвиг в генной экспрессии. Транскрипция «промежуточных» и «поздних» генов контролируется специфическими вирусными белками. Некоторые продукты транскрипции ранних генов образуются на поздней стадии инфекции, упаковываются в вири-оны и используются в следующем круге инфекции. Так как в состав вирусов оспы входит большое количество белков, не является неожиданным, что сборка вирионов есть комплексный процесс, который длится несколько часов и все еще целиком не выяснен.
Образование вириона связано с вхождением ДНК внутрь незрелой сердцевинной структуры, которое затем завершается включением наружных покрывающих слоев. Репликация и сборка вирионов происходят в разных местах цитоплазмы в так называемых виропластах или вирусных фабриках. Вирионы выходят из клетки почкованием (оболочечные вирионы), или путем экзоцитоза, или при лизисе клеток (вирионы без оболочки). Большинство вирионов освобождаются при цитолизе и не имеют оболочки. Вирионы с оболочкой и без нее обладают инфекционностью, но первые, вероятно, играют более значительную роль в возникновении и распространении заболевания, а также в создании иммунитета.
В очищенном вирусе осповакцины (ВОВ) выявлены белки с молекулярной массой 10-250 кД. Многие из них сосредоточены в сердцевине вириона. Два структурных гликопротеина располагаются между оболочкой и сердцевиной. В оболочке ВОВ содержится около 10 белков, из которых иммунологически наиболее активны крупномолекулярные белки с молекулярной массой 58—32 кД (VP4c, VP6a, VP6b и VP7a). Белок 32 кД определяет круг хозяев и важен для репликации вируса.
В составе очищенного вируса оспы птиц обнаружено 29 полипептидов с молекулярной массой 14-138 кД. Наивысшей антигенной и иммуногенной активностью обладают полипептиды с молекулярной массой 35 и 37 кД. За индукцию вируснейтрализующих антител ВО ответственны антигены, расположенные на поверхности наружной оболочки вириона, и прежде всего белок 58 кД (VP4c), являющийся основным структурным компонентом трубочек (ворсинок). Антисыворотка к этому белку нейтрализовала инфекционность вируса и предотвращала образование синцития в культуре клеток. Этот белок ответственен за выработку иммунитета.
Внеклеточные вирионы покрыты дополнительной наружной оболочкой, отсутствующей у внутриклеточных вирионов. Она играет важную роль в индукции синтеза ВН-антител. Инфекционность ВОВ и ВО крупного рогатого скота, имеющих наружную оболочку, нейтрализовалась антисывороткой к имеющему эту оболочку ВОВ, но не нейтрализовалась антисывороткой к ВОВ, лишенному наружной оболочки.
За гемагглютинирующую активность ортопоксвирусов ответственны полипептид 85 кД и гликопротеид 41 кД. Во внеклеточном оболочечном ВОВ гемагглютинирующие свойства связаны с полипептидом 85 кД. Внутриклеточные вирионы (без дополнительной оболочки) практически не содержали этого полипептида. Неструктурный гемагглютинин формируется на цитоплазматических мембранах. С его образованием инфицированные клетки приобретают способность адсорбировать эритроциты. Вирусспецифические белки с молекулярной массой 32 и 37 кД, экспрессируемые на поверхности клеток, инфицированных ВОВ, делают их мишенями для специфических цитотоксических Т-лимфоцитов. МАТ-реактивные против каждого из пяти (54; 34; 32; 29 и 17—25 кД) белков наружного слоя поверхности вируса осповакцины нейтрализовали его инфекционность. В структуре полипептида 54 кД обнаружено два нейтрализующих эпитопа(Аи В). Анализ антигенных детерминант поверхностных полипептидов, проведенный с помощью МАТ, выявил в составе ортопоксвирусов, наряду с видоспецифическими, группоспецифические эпитопы.
Связывание ВОВ с нейтрализующими МАТ не препятствовало его прикреплению к клеткам-мишеням, но блокировало депротеинизацию вирионов.
Управление Роспотребнадзора по Республике Марий Эл
Управление Роспотребнадзора по Республике Марий Эл
Эпидемиологический надзор
Оспа
Оспа натуральная (variola vera) − антропонозная вирусная инфекционная болезнь с аспирационным механизмом передачи инфекции, характеризующаяся интоксикацией, лихорадкой, пустулезно-папулезной сыпью и высокой летальностью.
Болезнь ликвидирована в октябре 1977 г., что было сертифицировано Генеральной Ассамблеей ВОЗ в мае 1980 г.
Вместе с тем мероприятия по эпидемиологическому надзору за натуральной оспой продолжаются, в частности проводятся исследования поксвирусов животных (например, возбудителей оспы обезьян, белой оспы), которые могут в результате мутации стать вирулентными для человека, хотя вероятность этого представляется возможной в весьма отдаленном будущем.
Возбудитель − ДНК-содержащий вирус
При тяжелой геморрагической оспе («черная оспа») летальность равна 70-100 %, при сливной − 50-70 %, среднетяжелой − 5-10 %, при легкой (вариолоид, оспа у привитых) − 2-3 %. При доброкачественной форме натуральной оспы летальность составляет менее 2 %.
Оспа обезьян− зоонозная природно-очаговая вирусная инфекционная болезнь, характеризующаяся лихорадкой, общей интоксикацией и появлением экзантемы, сходной с высыпаниями при натуральной оспе.
Возбудитель − вирус, относящийся к семейству поксвирусов.
Вирус впервые был выделен в 1958 г. от больных обезьян. По своим свойствам сходен с другими представителями группы оспы. В антигенном отношении вирус оспы обезьян стоит ближе к вирусу натуральной оспы, чем к вирусам коровьей оспы и осповакцины.
Заболевания наблюдались в ряде стран Западной и Центральной Африки (Заир, Либерия, Сьерра-Леоне, Нигерия и др.). В основном регистрировались спорадические случаи, иногда − небольшие групповые заболевания. Около 10% всех случаев составляют заболевания, вызванные заражением человека от человека. Были случаи оспы обезьян, в семьях заболевших (протекали легко), третичной передачи не наблюдалось. Заболели лица, не получавшие прививок против натуральной оспы.
Инкубационный период длится около 2 недель. Клиническая симптоматика оспы обезьян весьма сходна с проявлениями натуральной оспы. Заболевание протекает легче, чем при натуральной оспе. Летальность составляет 10-15 %.
Инкубационный период − 22 дня (от 5 до 22 суток). У привитых противооспенной вакциной − от 15 до 17 суток.
Источник инфекции − больной человек или труп умершего от оспы.
Пути передачи возбудителя инфекции:
−воздушно-капельный и воздушно-пылевой (при рассеивании вируса с капельками слизи и слюны, особенно при кашле и чихании, при разговоре с больным);
−контактно-бытовой (при контакте с вещами больного или предметами обстановки, загрязненными слизью, гноем и корочками с пораженной кожи, содержащими вирус).
−при общении с больным, при соприкосновении с его вещами или предметами обстановки, загрязненными слизью, гноем и корочками с пораженной кожи, фекалиями, мочой больного, содержащими вирус;
Натуральная оспа
Натуральной оспой болеют только люди, экспериментальное заражение лабораторных животных удается с трудом. Возбудителем натуральной оспы является фильтрующийся вирус, антигенно родственный вакцинии, вирусу коровьей оспы, тонкое строение и закономерности размножения которого хорошо изучены. Инкубационный период при натуральной оспе продолжается от 8 до 14 дней, чаще ок. 11–12. Больные заразны для окружающих в течение всего периода высыпания и, по-видимому, даже за несколько дней до появления сыпи, в общей сложности около трех недель. Вирус выделяется из разрывающихся и подсыхающих пузырьков на коже, из ротовой полости и обнаруживается в моче и кале больного. Возбудитель инфекции передается путем непосредственных контактов, воздушно-капельным способом, от здоровых носителей и животных, и может сохранять жизнеспособность на одежде и постельном белье. Все невакцинированные люди восприимчивы к заражению; естественного иммунитета к натуральной оспе не бывает. Хотя заболевание возможно в любом возрасте, дети до четырех лет особенно уязвимы.
Что провоцирует / Причины Натуральной оспы:
Патогенез (что происходит?) во время Натуральной оспы:
В типичных случаях оспа характеризуется общей интоксикацией, лихорадкой, своеобразными высыпаниями на коже и слизистых оболочках, последовательно проходящими стадии пятна, пузырька, пустулы, корочки и рубца.
При вдыхании зараженного воздуха вирусы попадают в респираторный тракт. Возможно заражение через кожу при вариоляции и трансплацентарно. Вирус поступает в ближайшие лимфатические узлы и далее в кровь, что приводит к виремии. Гематогенно инфицируется эпителий, здесь происходит размножение вируса, с чем связано появление энантемы и экзантемы. Ослабление иммунитета ведет к активации вторичной флоры и превращению везикул в пустулы. Вследствие гибели росткового слоя эпидермиса, глубоких нагноительных и деструктивных процессов формируются рубцы. Может развиться инфекционно-токсический шок. Для тяжелых форм характерно развитие геморрагического синдрома.
Симптомы Натуральной оспы:
При типичном течении оспы инкубационный период длится 8-12 дней.
Начальный период характеризуется ознобом, повышением температуры тела, сильными рвущими болями в пояснице, крестце и конечностях, сильной жаждой, головокружением, головной болью, рвотой. Иногда начало болезни мягкое.
На 4-й день наблюдается снижение температуры тела, ослабляются клинические симптомы начального периода, но появляются типичные оспины на коже головы, лица, туловища и конечностей, которые проходят стадии пятна, папулы, пузырька, пустулы, образования корочек, отторжения последних и образования рубца. Одновременно появляются оспины на слизистой оболочке носа, ротоглотки, гортани, трахеи, бронхах, конъюнктивах, прямой кишке, женских половых органов, мочеиспускательного канала. Они вскоре превращаются в эрозии.
Изменение крови характеризуется лейкоцитозом, при тяжелых формах имеется резкий сдвиг влево с выходом в кровь миелоцитов и юных клеток.
К тяжёлым формам относятся сливная форма (Variola confluens), пустулезно-геморрагическая (Variola haemorrhagica pustulesa) и оспенная пурпура (Purpura variolosae).
У привитых противооспенной вакциной оспа протекает легко (Varioloid). Основными её особенностями являются продолжительный инкубационный период (15-17 дней), умеренные явления недомогания и других признаков интоксикации; истинная оспенная сыпь необильная, пустулы не образуются, рубцов на коже не остается, выздоровление наступает через 2 недели. Встречаются лёгкие формы с кратковременной лихорадкой без сыпи и выраженных расстройств самочувствия (Variola sine exanthemate) или только в виде необильной сыпи (Variola afebris).
К возможным осложнениям относятся энцефалиты, менингоэнцефалиты, пневмонии, панофтальмиты, кератиты, ириты, сепсис.
Диагностика Натуральной оспы:
Лечение Натуральной оспы:
Для лечения данного заболевания применяются противовирусные препараты (метисазон по 0,6 г 2 раза в день курсом 5-6 сут), противооспенный иммуноглобулин 3-6 мл внутримышечно. Для профилактики присоединения бактериальной инфекции на пораженные участки кожи наносятся антисептические препараты. При наличии бактериальных осложнений больным назначаются антибиотики широкого спектра действия (полусинтетические пенициллины, макролиды, цефалоспорины). Проводятся мероприятия направленные на детоксикацию организма, к ним относятся введение коллоидных и кристаллоидных растворов, в некоторых случаях проводится ультрафильтрация и плазмофорез.
Прогноз зависит от клинической формы болезни, возраста и преморбидного состояния. Летальность колеблется от 2% до 100%. При легком течении и у привитых прогноз благоприятный. Реконвалесценты выписываются из госпиталя после полного клинического выздоровления, но не раньше чем через 40 дней от начала заболевания. После легких форм больные выписываются без изменения категории годности. После тяжелых форм годность к военной службе решается ВВК в зависимости от резидуальных явлений (нарушение зрения и другие) или им предоставляется отпуск по болезни сроком до 1 мес.
Профилактика Натуральной оспы:
Вариоляция (вакцинация ранней, небезопасной вакциной) была известна на Востоке по крайней мере с раннего Средневековья: в Индии о ней сохранились записи VIII века, а в Китае X века. В Европу данная техника вакцинации была впервые привезена из Турции супругой британского посла в Стамбуле Мэри Уортли Монтегю в 1718 году, после чего была привита британская королевская семья.
В России вариоляция была введена после смерти от оспы 14-летнего императора Петра II.
В конце XVIII века английский врач Эдвард Дженнер изобрёл прививку от оспы на основе вируса коровьей оспы, которая была привита в Европе массово.
Первыми привитыми от оспы в России были Екатерина II Великая, Великий князь Павел Петрович, Великая княгиня Мария Фёдоровна, а через несколько дней и внуки Екатерины Александр и Константин Павловичи. Крестьянскому мальчику Маркову, от которого была привита оспа императрице, было присвоено дворянство, фамилия Оспенный и герб.
В Америке, Азии и Африке оспа держалась ещё почти двести лет. В XVIII веке от натуральной оспы в России умирал каждый 7-ой ребенок. В XX веке вирус унес жизни 300-500 миллионов человек. В конце 1960-х оспа поражала 10-15 млн непривитых людей.
В 1967 г. ВОЗ принимает решение об эрадикации натуральной оспы с помощью массовой вакцинации человечества.
Последний случай заражения натуральной оспой естественным путем был описан в Сомали в 1977 г. В 1978 г. зафиксирован и последний случай лабораторного заражения. Официально об искоренении оспы было объявлено в 1980 г. на Ассамблее ВОЗ, чему предшествовало соответствующее заключение комиссии специалистов, вынесенное в декабре 1979г.
Натуральная оспа относится к особо опасным инфекциям. Больные и подозрительные на эту инфекцию подлежат строгой изоляции, клиническому обследованию и лечению в специальных стационарах. Медицинский персонал работает в противочумной одежде III типа с маской. Проводят тщательную текущую и заключительную дезинфекцию помещения, где находится (находился) больной, предметов обихода и мест общего пользования 5% раствором лизола. Посуду замачивают 3% раствором хлорамина, затем кипятят. Весь мусор и отходы сжигаются.
Карантин для лиц, находившихся в контакте с больным (подозрительным) натуральной оспой, устанавливают на 17 дней. Все они вакцинируются против оспы независимо от срока предыдущей прививки. Им вводят однократно донорский гамма-глобулин в количестве 3 мл и назначают внутрь метисазон: взрослым 0,6 г 2 раза в сутки, детям — разовая доза из расчета 10 мг на 1кг массы тела ребенка 4—6 дней подряд.
К каким докторам следует обращаться если у Вас Натуральная оспа:
Интересные факты о болезни Натуральная оспа:
Прекращение вакцинации против натуральной оспы могло спровоцировать рост заражений ВИЧ-инфекцией. По мнению иммунологов, вакцина против оспы понижала вероятность проникновения в клетки вируса иммунодефицита.
Авторы исследования, американские ученые из Университета Калифорнии и еще нескольких научных центров, описали на страницах журнала результаты экспериментов на культуре клеток, взятых у людей, прошедших вакцинацию. Исследователи обнаружили, что в клетках людей, ранее привитых от оспы, ВИЧ размножался медленнее, чем в таких же клетках у людей, не проходивших вакцинацию.
Осторожность не повредит
Не следует, впрочем, считать, что вакцина от оспы защищает от ВИЧ, и немедленно бежать делать прививку: ученые подчеркивают, что эксперимент проведен на культуре клеток, а не на целом организме и пятикратное снижение скорости распространения вируса получено не для любой разновидности ВИЧ, а только для определенных штаммов. Эти штаммы довольно распространенные и играют важную роль в развитии эпидемии, но далеко не единственные. Да и замедление распространения вируса впятеро все-таки неравносильно его полному уничтожению.
Другое дело, что вплоть до 1970-х годов, когда прививки от оспы ставились массово, риск заражения мог быть меньше, и долгое время вирус просто не мог выйти за пределы ограниченной территории в Центральной Африке. Даже сейчас вероятность передачи ВИЧ при сексуальных контактах не превышает десятых долей процента и снижение этой величины в несколько раз вкупе со слабым развитием транспорта вполне могло не дать разгуляться пандемии. Сейчас, когда число носителей вируса составляет около 40 млн человек во всем мире, рассчитывать на искоренение ВИЧ не приходится, даже если результаты предварительных экспериментов полностью подтвердятся. Но любой мало-мальски перспективный подход к снижению риска передачи вируса, безусловно, заслуживает рассмотрения.
Как это работает?
Ключевую роль в потенциальном защитном механизме играют рецепторы типа CCR5 – белковые молекулы, расположенные внутри клеточной мембраны. Именно с этими молекулами взаимодействует ВИЧ при проникновению в клетку, и вирусологам известно, что люди с мутантной формой CCR5-рецепторов для ВИЧ уязвимы в гораздо меньшей степени.
Окна и двери
CCR5 – не единственная молекула, которой пользуется вирус для попадания в клетки. Столь же важны рецепторы класса CD4. Проводя аналогию, можно сравнить рецепторы с «окнами» и «дверьми» клетки. Злоумышленники проникают как через двери, так и через окна, поэтому установка ударопрочных стекол или надежных замков по отдельности лишь снижает, но не сводит на нет риск кражи.
Кстати, аналогия между рецепторами и окнами примечательна еще и тем, что рецепторы нужны самой клетке для избирательного взаимодействия с другими клетками.
Вирус же vaccinia, который и является основой вакцины (сходство в названиях не случайно, вирус назван именно за свою благородную функцию) от натуральной оспы, может менять экспрессию гена CCR5. Это означает, что ген, отвечающий за синтез белков рецептора, может «выключаться», и со временем у привитого пациента CCR5 рецепторы просто исчезают.
Как именно это происходит, насколько долго длится эффект (ученые вели опыты на клетках от людей, привитых за три и шесть месяцев до эксперимента) и можно ли его еще и усилить, пока неясно. Но очевидно то, что прививки от оспы достаточно безопасны для массового применения: их в свое время делали каждому ребенку на планете, и у многих на плече остался крохотный шрам.
Лишь в 1980-х, когда оспа исчезла с лица Земли и осталась только в нескольких микробиологических лабораториях, от прививок отказались, так как риск побочных последствий стал многократно превышать риск заражения оспой как таковой. Но если будет доказано, что прививки от оспы помогают и против ВИЧ (пусть даже не абсолютно), к осповакцинации вернуться будет несложно.
Вирус натуральной оспы: зло во благо
Человеку, как и другим животным, постоянно приходилось бороться с окружающими его патогенными микроорганизмами, что обусловило появление и развитие у нас систем врожденного и приобретенного иммунитета. Однако нарушения в регуляции работы этих механизмов, защищающих от внешних «агрессоров», приводят к развитию хронических воспалительных и аутоиммунных болезней, с трудом поддающихся лечению.
Для терапии таких заболеваний, как астма, атеросклероз, системная красная волчанка, псориаз, ревматоидный артрит, рассеянный склероз и другие, такие как вирус натуральной оспы, используются человеческие антитела, блокирующие белковые факторы воспаления. Оказалось, что для этих целей можно использовать и белки инфекционных микроорганизмов, которые эволюционно адаптированы к преодолению защитных систем организма.
Особый интерес для медицинской биотехнологии представляют высоко патогенные вирусы, для которых человек является единственным хозяином. И сегодня на основе белков вируса натуральной оспы, столетиями являвшегося настоящим бичом цивилизаций, создаются препараты для коррекции тяжелейших патологических состояний неинфекционной, в том числе аутоиммунной, природы.
Об авторе
Сергей Николаевич Щелкунов — доктор биологических наук, академик РАЕН, заведующий отделом геномных исследований и разработки методов ДНК-диагностики поксвирусов ГНЦ вирусологии и биотехнологии «Вектор» (Кольцово, Новосибирская обл.), профессор кафедры молекулярной биологии Новосибирского государственного университета. Лауреат премии правительства РФ (2005). Автор и соавтор более 200 научных публикаций.
Вплоть до открытий Антони ван Левенгука в XVII в. человечество и не подозревало, что живет в среде, наполненной множеством разнообразных мельчайших существ. Эти микроорганизмы настолько малы, что их можно увидеть, лишь вооружившись хорошим микроскопом: оптическим — для изучения бактерий и других одноклеточных, сложным и дорогим электронным — для получения «портретов» вирусов.
Большинство микроорганизмов сосуществует с человеком и животными вполне миролюбиво, а многие — и на взаимовыгодных началах, однако некоторые из них нарушают «мирный договор», переходя в разряд болезнетворных. Удивительно, но способность таких патогенных микроорганизмов преодолевать защитные системы организма хозяина можно использовать нам во благо. Особый интерес для современной медицинской биотехнологии представляют высокопатогенные вирусы, такие как вирус натуральной оспы, для которых человек является единственным хозяином. На основе белков этих вирусов сегодня создаются препараты для лечения тяжелых хронических воспалительных заболеваний неинфекционной, в том числе аутоиммунной, природы.
Микроорганизмы обитают везде: в воздухе и в воде, в почве и в наших собственных телах. По сравнению с человеком и животными размножаются они чрезвычайно быстро, и их сообщества неизмеримо многочисленнее. Так, если человечество перевести в масштаб микромира, то все 7 млрд человек легко уместились бы в стандартной микробиологической колбе.
Чтобы выжить, человеку, как и другим животным, постоянно приходилось бороться с окружающими его патогенными микроорганизмами. Такие события в эволюционной истории происходили многократно, чем и обусловлено появление и развитие у млекопитающих большого числа защитных механизмов, обеспечивающих их выживание в «микробном бульоне» тонкой биосферной прослойки нашей планеты.
Среди защитных реакций организма самая «быстрая» — неспецифическая, т. е. направленная против любых вирусов, микробов и биологических макромолекул. Речь идет о системе врожденного иммунитета, настроенной на распознавание и последующее реагирование на молекулярные компоненты микроорганизмов, представляющих угрозу. Важную роль в ранней неспецифической защите организма от инфекции играют хорошо всем знакомые воспалительные процессы, которые препятствуют распространению патогена в первые часы и дни после инфицирования.
Специфическая защита организма против конкретного инфекционного агента — адаптивный или приобретенный иммунитет, развивается медленнее и представляет собой сложное взаимодействие иммунных клеток разного типа, регулируемое специальными белками.
Иммунная оборона
Задача иммунной системы организма — защищать его от любых внешних и внутренних угроз.
Врожденный иммунитет неспецифичен — он обеспечивает защиту от любых инфицирующих агентов: вирусов, бактерий, а также макромолекул.
Одной из первых (возможно, и одной из самых древних) линий такой неспецифической защиты является апоптоз — программируемое самоубийство клетки. В случае вирусной инфекции апоптоз, индуцируемый в результате молекулярного распознавания специфичных молекул патогена, предотвращает размножение вируса и инфицирование других клеток организма хозяина.
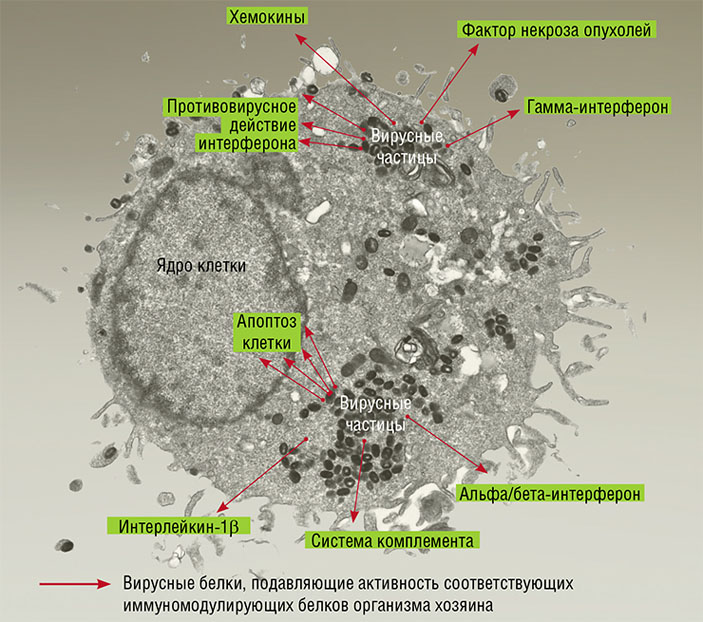
Важную роль в ранней неспецифической защите организма от вирусной инфекции играет воспаление, возникающее в первые часы и дни после инфицирования и направленное на ограничение распространения вируса. Клетки врожденной иммунной системы млекопитающих — макрофаги, дендритные клетки и натуральные киллеры, в ответ на инфекцию продуцируют так называемые провоспалительные цитокины, такие как интерлейкин-1β(IL-1β), интерлейкин-18 (IL-18), фактор некроза опухолей (TNF) и гамма-интерферон (γ-IFN). В развитии воспалительной реакции участвуют белки и другого класса — хемокины, которые регулируют перемещение и функции лейкоцитов.
К дополнительным механизмам врожденного иммунитета можно отнести комплемент — многокомпонентный набор сложных белков сыворотки крови, которые являются протеолитическими ферментами, участвующими в инактивации инфекционных агентов и зараженных ими клеток.
Специфическая защита организма против конкретного инфекционного агента — адаптивный или приобретенный иммунитет, развивается медленнее реакций врожденного иммунитета. Он осуществляется в результате сложного взаимодействия клеток разного типа, контролируемого цитокинами TNF, IL-1β и γ-IFN. Его результат — появление B-лимфоцитов, синтезирующих специфичные противовирусные антитела, и вирусоспецифических цитолитических T-лимфоцитов. Специфичные антитела могут взаимодействовать с вирусными частицами и их компонентами индивидуально либо в комплексе с комплементом, инактивируя их.
Таким образом, интерлейкин-1β, фактор некроза опухолей и гамма-интерферон являются важнейшими цитокинами, которые, наряду с регулированием воспалительных реакций, контролируют развитие адаптивного иммунного ответа организма на инфекцию.
Все эти системы защищают нас от внешних «агрессоров», однако нарушения в их работе могут приводить к развитию патологических состояний, сопровождающихся хроническими воспалительными и (или) аутоиммунными реакциями, такими как астма, атеросклероз, системная красная волчанка, псориаз, ревматоидный артрит, рассеянный склероз и другие тяжелые болезни, с трудом поддающиеся лечению.
В настоящее время разрабатываются методы так называемой «биологической» терапии подобных заболеваний, основанные на блокировании избыточной активации защитных систем с помощью различных биологических макромолекул. В том числе для этого используют человеческие антитела, способные специфично взаимодействовать и дезактивировать белки врожденной и адаптивной систем иммунитета, сверхсинтез которых и приводит к развитию патологий.
Но что если использовать для этих целей белки патогенных микроорганизмов, таких как вирусы, эволюционно-адаптированных к преодолению защитных систем организма, обернув, образно говоря, зло во благо?
Патогенный и антропонозный
Царство вирусов было открыто более ста лет назад выдающимся русским ученым Д. И. Ивановским, однако изучить эти мельчайшие организмы удалось лишь в последние десятилетия благодаря бурному развитию инструментальных методов исследований.
Хотя вирусы очень разнообразны по своей организации и функционированию, все они способны размножаться лишь в клетках других организмов, одноклеточных и многоклеточных. В процессе длительной совместной эволюции с организмом хозяина вирусы постоянно «пробуют» новые варианты подавления защитных реакций хозяина или их «обмана» за счет молекулярной мимикрии. В частности, вирусы могут включать в состав своего генома кодирующие последовательности клеточных генов, участвующих в регулировании иммунных реакций, и модифицировать их, приспосабливая для обеспечения собственной жизнедеятельности.
Разные вирусы млекопитающих отличаются не только по размеру генома и самих вирусных частиц, но и по стратегии своего развития в организме хозяина. Вирусы различных семейств демонстрируют удивительное разнообразие в механизмах преодоления систем врожденного и адаптивного иммунитета млекопитающих. Поэтому изучение этих особенностей вирусов позволяет выявить новые закономерности организации и функционирования защитных систем животных и человека, обеспечивающих выздоровление после инфицирования болезнетворным агентом.
Большинство вирусов способно заражать широкий спектр видов животных (круг хозяев). Однако для медицинской биотехнологии особый интерес представляют высокопатогенные и при этом антропонозные вирусы, для которых человек является единственным хозяином. В этом случае вирус может очень эффективно подавлять (или «уходить» от атаки) иммунные реакции именно человеческого организма. Генотипические исследования таких вирусов и выявление вирусных белков, эффективно подавляющих развитие воспалительных процессов в ответ на инфекцию, создает предпосылки для создания новых препаратов, предназначенных для лечения хронических воспалительных заболеваний неинфекционной природы.
Удивительный пример высокой патогенности для человека и строгой антропонозности представляет собой вирус натуральной оспы. Этот вирус, предположительно, исходно имел широкий круг хозяев, однако в процессе эволюции утратил способность размножаться в организме других млекопитающих, сохраняясь в эндемичном (т. е. свойственном только данной местности) состоянии в течение многих столетий в густонаселенных районах, прежде всего, Индийского субконтинента (Щелкунов, 2012).
Поксвирусы, к которым принадлежит вирус натуральной оспы, являются крупнейшими ДНК-содержащими вирусами млекопитающих. Вирусные белки, обладающие иммуномодулирующей активностью, синтезируются на ранних этапах вирусной инфекции. Они остаются в зараженной клетке либо выходят из нее, взаимодействуя с ключевыми белками-регуляторами как врожденного, так и адаптивного иммунитета организма хозяина. Подавляя активность этих белков, вирус обеспечивает зараженной клетке «круговую оборону» от атак иммунной системы хозяина. Клетка клеточной культуры фибробластов здоровой ткани легкого человека, инфицированная вирусом натуральной оспы (штамм Индия-1967). Электронная микроскопия. Фото Е. Рябчиковой
При этом вирус натуральной оспы не способен находиться в организме человека в латентном состоянии или вызывать хроническую инфекцию — болезнь всегда заканчивается либо выздоровлением, либо гибелью инфицированного. Это снижает вероятность выживания вируса в природе и свидетельствует о том, что он попал в своеобразный эволюционный «тупик»; с другой стороны, размножаясь из поколения в поколение только в организме человека, вирус натуральной оспы максимально приспособился на молекулярном уровне к преодолению многоярусных механизмов врожденного и адаптивного иммунитета человека (Щелкунов, 2011).
Такие свойства особо опасного вируса натуральной оспы позволили предположить, что его белки можно использовать для терапии различных иммунопатологий человека (Щелкунов, 1995). И сегодня в ГНЦ вирусологии и биотехнологии «Вектор» (Кольцово, Новосибирская обл.) идет работа над созданием лекарственных препаратов нового поколения на основе белков, секретируемых поксвирусами, к которым принадлежит и вирус натуральной оспы.
Сотрудники ГНЦ вирусологии и биотехнологии «Вектор» (Кольцово, Новосибирская обл.) первыми в мире расшифровали структуры геномов патогенных для человека вирусов натуральной оспы, оспы коров и оспы обезьян, выделенных от больных людей (Shchelkunov et al., 1993, 1998, 2001). Сравнение геномных стратегий этих вирусов и генов, кодирующих белки-иммуномодуляторы, показало, что все вирусы, относящиеся к семейству поксвирусов (Poxviridae), характеризуются наибольшим разнообразием механизмов преодоления защитных иммунных реакций организма человека по сравнению с вирусами других семейств (Shchelkunov, 2012). Вирус натуральной оспы, для которого человек является единственным хозяином, наиболее эффективно по сравнению с другими поксвирусами подавляет активность иммунной системы человека.
Оружие против воспаления
Как уже упоминалось, главной причиной аутоиммунных заболеваний является разбалансировка иммунитета, в том числе сверхсинтез веществ, провоцирующих воспалительные реакции.
Одним из ключевых цитокинов иммунного воспалительного ответа является фактор некроза опухолей (TNF) — именно его повышенная продукция приводит к таким болезням аутоиммунной природы, как псориаз, болезнь Крона, ревматоидный артрит и т. п. Высокий уровень продукции TNF обусловливает и тяжелую патологию, часто завершающуюся летальным исходом, — септический, или эндотоксический, шок.
Воспрепятствовать связыванию TNF с его белковыми рецепторами, зафиксированными на клеточных мембранах, можно с помощью соответствующих моноклональных антител либо так называемых растворимых форм его рецепторов, которые представляют собой внеклеточные домены (участки) рецепторных белков и обычно обнаруживаются в сыворотке и других биологических жидкостях. Присоединение подобных молекул к TNF должно инактивировать этот цитокин и уменьшить вызванный им воспалительный процесс.
Действительно, в модельных лабораторных экспериментах было доказано терапевтическое действие анти-TNF антител при лечении ряда патологий, обусловленных повышенной продукцией TNF. Однако попытки использовать для этих целей напрямую растворимые клеточные TNF-рецепторы не дали положительных результатов. Успеха удалось добиться лишь с помощью методов генетической инженерии, когда были созданы так называемые химерные белки, состоящие из TNF-связывающей части клеточных рецепторов и фрагмента иммуноглобулина человека.
Уже несколько таких биологических терапевтических средств, созданных на основе белков человеческого организма, в течение ряда лет успешно применяются в клинической практике для терапии воспалительных заболеваний неинфекционной природы. Это, в первую очередь, Etanercept (на основе химерного белка), а также Infliximab и Adalimumab (на основе моноклональных человеческих антител); недавно этот список пополнился еще двумя аналогичными препаратами.
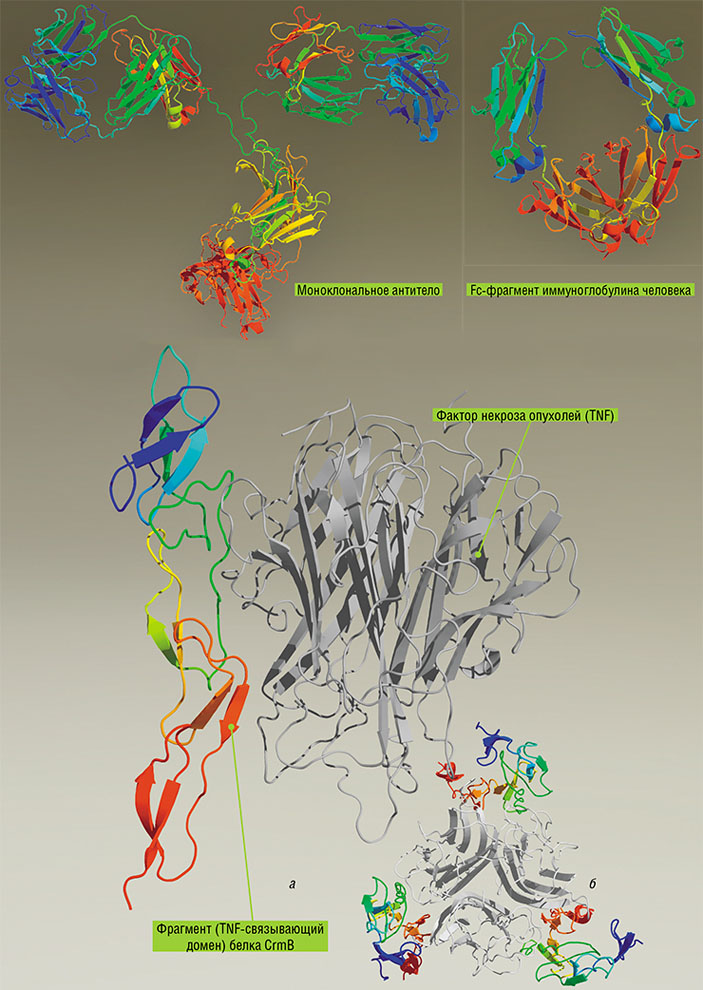
Для лечения аутоиммунных заболеваний создаются так называемые биологические терапевтические средства, направленные против провоспалительных цитокинов, таких как фактор некроза опухолей (TNF). Например, Infliximab и Adalimumab, созданные на основе человеческих моноклональных антител; Etanercept — химерный белок, состоящий из TNF-связывающей части клеточных рецепторов и фрагмента иммуноглобулина человека. Эти препараты одобрены для терапии ревматоидного артрита, псориаза и псориатического артрита, а также болезни Крона и язвенного колита. Препараты аналогичного действия могут быть созданы и на основе CrmB — белка вируса натуральной оспы, способного связываться с человеческим фактором некроза опухолей (а). С одной гомотримерной молекулой фактора некроза опухолей связывается три молекулы вирусного белка (б, вид сверху)
Однако клинические исследования показали, что пациенты, страдающие ревматоидным артритом или другим воспалительным или аутоиммунным заболеванием, оказываются избирательно чувствительны лишь к одному из этих анти-TNF препаратов. Кроме того, поскольку все эти препараты имеют белковую природу, они сами по себе являются мишенью для иммунной системы больных, поэтому при длительной терапии их эффективность может снижаться. Это означает, что при потере чувствительности к одному препарату его требуется заменить на другой.
И вот здесь на помощь терапевтам могут придти новые лекарственные средства на основе вирусных белков. Например, в ГНЦ ВБ «Вектор» уже разрабатываются анти-TNF препараты на основе TNF-связывающих белков поксвирусов.
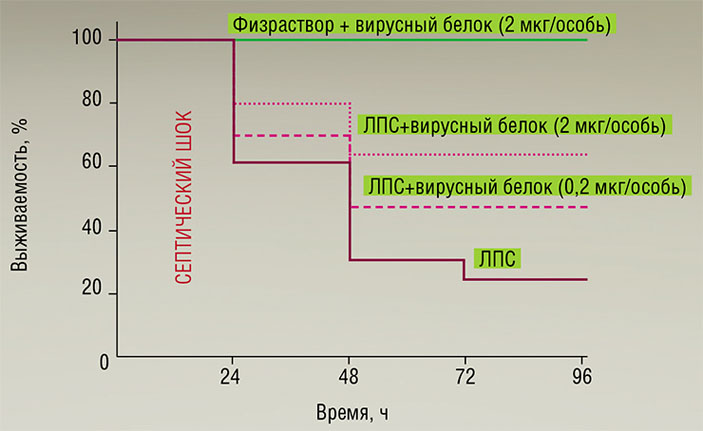
Эффективность действия TNF-связывающего белка вируса натуральной оспы при терапии септического шока проверена на лабораторных мышах, которым был введен бактериальный липополисахарид (ЛПС) — компонент бактериальных стенок, вызывает сильный иммунный ответ с выделением провоспалительных цитокинов, что приводит к развитию опасного септического шока. Введение вирусного белка значительно повысило выживаемость заболевших особей
Методами генетической инженерии здесь были созданы рекомбинантные бакуловирусы, способные продуцировать в клеточной культуре TNF-связывающий белок (CrmB), характерный для вирусов оспы коров, оспы обезьян и натуральной оспы. Однако на экспериментальной модели эндотоксического шока было показано, что существенным терапевтическим эффектом обладает лишь белок CrmB вируса натуральной оспы (Gileva et al., 2006). Именно этот белок или его реконструированные варианты могут стать действующим началом новых средств анти-TNF терапии (Гилева и др., 2009).
Ревматоидный артрит — системное аутоиммунное заболевание соединительной ткани, проявляющееся главным образом хроническим воспалением суставов: голеностопных, лодыжек, коленей и кистей рук.
Сегодня от этой болезни страдает каждый сотый житель Земли, т. е. более 70 млн человек. Женщины болеют в несколько раз чаще, чем мужчины. Болезнь обычно развивается после 30 лет. В 70% случаев ревматоидный артрит приводит к инвалидности, которая наступает довольно рано.
Причины возникновения этой болезни точно не установлены, но известно, что толчком к ее развитию служит сбой в иммунной системе в результате переохлаждения, стрессов, травм суставов и инфекции, в том числе ОРЗ, ангины и гриппа. При ревматоидном артрите наблюдается избыточный синтез таких провоспалительных цитокинов, как фактор некроза опухолей и гамма-интерферон.
Сепсис (от греч. «гниение») — тяжелое инфекционное заболевание человека, которое развивается как системная воспалительная реакция при попадании в кровь инфекционных агентов (бактерий или одноклеточных грибов) или их токсинов. Тяжесть заболевания нередко связана с развитием так называемого септического шока (инфекционно-токсический шок, эндотоксический шок), который чаще развивается при инфекции грамотрицательными бактериями и стафилококками и сопровождается нарушением функции легких, печени и почек, изменением свертывающей системы крови.
Несмотря на возросшие возможности современной антибактериальной и противогрибковой терапии, летальность при сепсисе до сих пор составляет 25–30%. На сегодняшний день эта болезнь остается одной из ведущих причин смертности: только в США от нее ежегодно умирает более 200 тыс. человек.
В настоящее время доказано, что инфекция сама по себе не является непосредственной причиной многочисленных патологических сдвигов, характерных для сепсиса. Скорее всего, они возникают как результат ответной реакции организма на инфекцию и некоторые другие факторы, обусловленной действием различных эндогенных регуляторных веществ. И если при нормальном состоянии подобные молекулярные реакции можно расценить как реакции приспособления или адаптации, то во время сепсиса их чрезмерная активация имеет повреждающий характер.
Ведущую роль в качестве медиаторов повреждения при септическом шоке играют суперпродуцируемые фактор некроза опухолей, гамма-интерферон и ряд интерлейкинов.
«Золотое дно» фармацевтики
Возможности медицинского «приложения» вирусных белков далеко не исчерпываются одной лишь анти-TNF терапией. Так, еще одним воспалительным цитокином является широко известный гамма-интерферон (γ- IFN). И в настоящее время вторую стадию клинических испытаний уже проходит препарат Fontolizumab, созданный на основе человеческих моноклональных анти-IFNγ антител и предназначенный для лечения некоторых аутоиммунных заболеваний.
Однако эффективным ингибитором IFNγ человека может оказаться и IFNγ-связывающий белок, секретируемый вирусом натуральной оспы. Такой белок, полученный в ГНЦ ВБ «Вектор», эффективно ингибировал защитное действие человеческого гамма-интерферона при заражении культуры клеток легкого эмбриона человека вирусом энцефаломиокардита мышей. По этой характеристике вирусный белок значительно превосходил препарат на основе человеческих клеточных IFNγ-рецепторов. (Непомнящих и др., 2005).
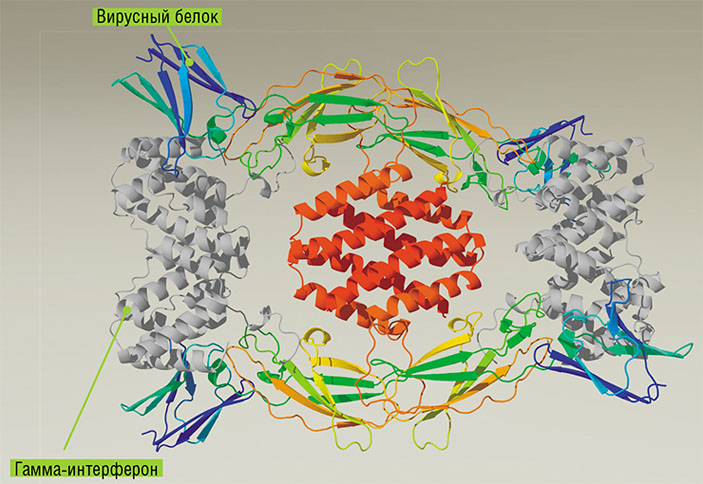
В ГНЦ ВБ «Вектор» получен рекомбинантный белок вируса натуральной оспы, способный связываться с человеческим гамма-интерфероном (γ-IFN), секреция которого увеличивается при ряде аутоиммунных заболеваний. На рисунке: структура гомотетрамерного комплекса вирусного γ-IFN-связывающего белка, связанного с двумя гомодимерами γ-IFN человека
На сегодня имеется много данных о том, что воспалительный процесс и гистопатологические изменения при ряде воспалительных и аутоиммунных заболеваний нервной системы, артрите, гломерулонефрите, системной красной волчанке и других болезнях во многих случаях обусловлены активацией системы комплемента крови, представляющей собой еще одну из систем неспецифического иммунитета. Комплемент играет важную роль и в реакции отторжения трансплантата.
Поксвирусы кодируют особый белок (КСБ), способный ингибировать активацию комплемента, причем наиболее эффективно с белками комплемента человека взаимодействует белок того же вируса натуральной оспы. Сегодня считается, что именно этот вирусный белок может стать перспективным препаратом для лечения болезни Альцгеймера, синдрома мультиорганной дисфункции и отторжения ксенотрансплантатов (Jha, Kotwal, 2003). Так, на лабораторных животных было показано, что рекомбинантный КСБ способствует восстановлению функций мозга после средней и тяжелой черепно-мозговой травмы. Этот белок оказался эффективен и при травмах спинного мозга: при его применении значительно уменьшались гистопатологические изменения, вызванные воспалительными реакциями.
В патогенезе воспалительных и аутоиммунных заболеваний важную роль играют и хемокины — обширное семейство небольших белков, имеющих очень сходную третичную структуру. Поксвирусы кодируют хемокинсвязывающие белки, по аминокислотной последовательности не имеющие гомологов среди известных белков позвоночных. Их высокий терапевтический потенциал был показан на ряде лабораторных моделей воспалительных и аутоиммунных заболеваний (Непомнящих, Щелкунов, 2008).
Таким образом, предположение ученых, что вирусные белки, являющиеся антагонистами иммунных белков-регуляторов, можно использовать в терапевтических целях, полностью подтвердилось. Сегодня на их основе с помощью методов генетической инженерии уже разрабатываются препараты нового поколения для коррекции патологических состояний человека, связанных с избыточной активацией белков-медиаторов защитных систем организма.
И с этой точки зрения мы можем по-новому взглянуть на смертельно опасный для человека вирус натуральной оспы: результаты лабораторных исследований и доклинических испытаний свидетельствуют о большой перспективности препаратов для лечения тяжелейших воспалительных и аутоиммунных заболеваний человека, созданных на основе белков этого вируса, на протяжении столетий бывшего настоящим бичом цивилизаций.
Автор и редакция благодарят к. б. н. Д. В. Антонец (ФБУН ГНЦ ВБ «Вектор») за помощь в подготовке иллюстративного материала.
Работа выполнена при финансовой поддержке РФФИ (грант 12-04-00110а).
Литература
1. Непомнящих Т. С., Щелкунов С. Н. Иммуномодулирующие белки поксвирусов как новые средства иммунокорректирующей терапии // Молекуляр. биология. 2008. Т. 42, №. 5. С. 904–912.
2. Щелкунов С. Н. Вирус натуральной оспы — источник новых медицинских препаратов // Соросовский образовательный журнал. 1995. № 1. С. 28–31.
3. Щелкунов С. Н. Генетическая инженерия: Учеб.-справ. пособие. 3-е изд., испр. и доп. Новосибирск: Сиб. универ. изд-во, 2008. 514 с.
4. Щелкунов С. Н. Преодоление ортопоксвирусами защитных систем организма млекопитающих // Молекуляр. биология. 2011. Т. 45, № 1. С. 30–43.
5. Щелкунов С. Н. Оспа — дамоклов меч цивилизаций // Наука из первых рук. 2012. № 6 (48). С. 96–109.
6. Shchelkunov S. N. Orthopoxvirus genes that mediate disease virulence and host tropism // Advances in Virology. 2012. Vol. 2012, Article ID 524743, 17 p. DOI: 10.1155/2012/524743.