Лечение кишечной непроходимости онкологических больных
Кишечная непроходимость — серьезное осложнение онкологических заболеваний. Она ухудшает состояние больного, приводит к нарушению питания, обмена веществ, чревата перфорацией, когда в стенке кишки появляется отверстие, кишечное содержимое попадает в брюшную полость и вызывает воспалительный процесс — перитонит. Таким образом, кишечная непроходимость — опасное для жизни состояние, в ряде случаев оно требует экстренного хирургического лечения.
Большое значение имеет причина, по которой пища перестала нормально проходить по кишечнику. В зависимости от этого выделяют типы кишечной непроходимости:
Странгуляционная, когда кишка скручивается, пережимается извне, при этом также может быть пережата ее брыжейка с сосудами, нарушено кровоснабжение. При онкологических заболеваниях причиной чаще всего становятся спайки после хирургического вмешательства.
Кишечная проходимость может возникать при раке тонкой, ободочной и прямой кишки, желудка, предстательной железы, матки, яичников, мочевого пузыря.
Хирургическое лечение кишечной непроходимости при онкологических заболеваниях
Основной метод лечения кишечной проходимости — хирургический. Быстрее всего приходится действовать при странгуляционной кишечной непроходимости, так как она быстро приводит к перитониту и серьезным осложнениям. Экстренная операция требуется при перитоните, перфорации стенки кишки.
Восстановить проходимость кишки помогают разные операции. Врач выбирает подходящий вариант, исходя из вида непроходимости, возможности удалить опухоль, общего состояния пациента:
Послеоперационный период и возможные осложнения
Обычно больные, которые перенесли операцию по поводу кишечной непроходимости, могут вернуться к нормальному приему пищи через несколько дней. В первые дни питание осуществляется внутривенно, разрешено лишь смачивать губы влажным кусочком ткани. Многих беспокоят сильные послеоперационные боли, поэтому важно назначить адекватное обезболивание.
Риск осложнений зависит от объема операции, общего состояния здоровья пациента и других факторов:
Стентирование кишки
Если хирургическое лечение невозможно, в кишечник можно установить стент — полый металлический или полимерный цилиндр с сетчатой стенкой. Он расширяет просвет пораженного участка кишки и помогает восстановить проходимость. Для того чтобы провести стентирование, не нужно делать разрез. Процедуру выполняют эндоскопически, например, во время колоноскопии (установка стента в толстую кишку) или ФГДС (в двенадцатиперстную кишку).
Консервативное лечение
Иногда можно обойтись без операции. Обычно консервативное лечение кишечной непроходимости предполагает следующие меры:
Если эти меры не помогают, и состояние больного ухудшается, прибегают к хирургическому лечению. Консервативная терапия возможна лишь в определенных случаях, при определенных видах кишечной непроходимости. Чаще всего при онкологических заболеваниях необходима операция.
Каков прогноз?
В большинстве случаев кишечная непроходимость возникает при запущенных стадиях рака, поэтому вопрос стоит о том, как улучшить состояние пациента и продлить его жизнь, а не о том, как вылечить. Такое лечение называется паллиативным. Прогноз зависит от стадии опухоли и ряда других факторов.
Например, пятилетняя выживаемость на 4 стадии онкологических заболеваний, которые могут приводить к кишечной непроходимости, составляет:
Кишечная непроходимость: практическое руководство для врачей
Определение
Состояние, при котором прохождение содержимого в желудочно-кишечном тракте замедлено, затруднено или полностью прекращено.
Частота
Возникает примерно у 3% паллиативных пациентов. Наиболее часто при раке яичников (25‒40%), колоректальном раке (10‒15%), раке желудка, желчных протоков, поджелудочной железы, эндометрия, мочевого пузыря, предстательной железы.
Классификация
По уровню возникновения ‒ клинически целесообразно ориентироваться на четыре уровня непроходимости отделов ЖКТ:
По этиологии ‒ на любом уровне обструкция может быть функциональной (динамической, нарушение перистальтики), или механической (органической), или сочетанной.
По степени нарушения пассажа кишечного содержимого ‒ полная или частичная.
По клиническому течению ‒ транзиторная (острая) или персистирующая (хроническая).
У пациентов могут отмечаться повторяющиеся эпизоды непроходимости, которые разрешаются через несколько дней покоя для ЖКТ. Частота и продолжительность эпизодов непроходимости имеют тенденцию к увеличению, и в конечном итоге она становится полной и необратимой. Прогноз обычно неблагоприятный, средняя продолжительность жизни составляет 1‒3 месяца.
Причины возникновения
Онкологические заболевания:
Последствия лечения онкологического заболевания или его симптомов:
Не связанные с онкологическим заболеванием:
Патофизиология
В результате обструкции происходит:
Клинические особенности
Основные симптомы зависят от уровня, этиологии, степени выраженности и продолжительности непроходимости.
Механическая эзофагальная непроходимость, как правило, манифестирует вначале дисфагией при глотании твердой пищи, затем дисфагией при глотании жидкостей.
Для непроходимости на уровне привратника желудка или проксимальных отделов тонкого кишечника характерны большие потери желудочного, панкреатического секрета, желчи вследствие обильной многократной мучительной для пациента рвоты и быстрое развитие водно-электролитных нарушений (гипогидратация, метаболичический алкалоз, гипокалиемия, гипохлоремия, гипонатриемия). При этом, как правило, отсутствует выраженное вздутие живота, в течение некоторого времени сохраняется отхождение газов и наличие стула. Даже при отсутствии питания через рот желудок требует опорожнения от поступающей слюны (
1500 мл/24 ч) и выделяемого желудочного сока (
1500 мл/ 24 ч). То есть, если пациент выделяет с рвотой менее 2‒3 л в сутки, значит, какая-то часть пищи проходит за уровень обструкции.
Особенностью непроходимости дистальных отделов тонкого кишечника, а также непроходимости толстого кишечника является стертость клинической симптоматики на ранних этапах развития заболевания и вместе с тем ‒ большая возможность для проведения консервативных мероприятий. На первый план при этом выступают признаки нарушения пассажа по кишечнику: болевой синдром, выраженное вздутие живота, рвота встречается реже, быстро прогрессируют явления эндотоксикоза. Вероятность развития инфекционных осложнений гораздо выше при низкой, чем при высокой непроходимости.
Боль в животе при наличии злокачественного новообразования ‒ постоянный и ранний признак непроходимости (90% случаев):
Колики часто встречаются при механической (в 75%) и практически отсутствуют при динамической непроходимости. Эпизоды колик сопровождаются слышимым урчанием. Плохо обезболиваются опиоидами, но уменьшаются или купируются спазмолитическими препаратами.
Рвота. Чем выше уровень непроходимости, тем более выражена рвота. В позднем периоде она становится неукротимой, рвотные массы приобретают вид и запах кишечного содержимого.
Растяжение является непостоянным симптомом (чаще встречается при низкой непроходимости), сопровождается тимпаническим звуком при перкуссии живота.
Кишечные шумы могут отсутствовать полностью при функциональной непроходимости, а при механической непроходимости ‒ быть активными и хорошо различимыми (урчание в животе). «Звук падающей капли» встречается редко.
Задержка стула и газов ‒ патогномоничный признак непроходимости кишечника, ранний симптом низкой непроходимости. При высоком ее характере вначале, особенно под влиянием лечебных мероприятий, может быть многократный стул, зачастую жидкий за счет эффекта «фильтра» ‒ прохождения жидкой и задержки плотной части кишечного содержимого выше участка непроходимости и опорожнения кишечника, расположенного ниже участка непроходимости. Необходимо быть максимально внимательным и не спешить расценивать данный симптом как диарею (жидкие водянистые выделения на фоне соответствующего диагноза, например, карциноматоза).
Обследование
Основывается на анамнезе и клиническом осмотре живота, хирургических протоколах. Дополнительные обследования проводятся в случае планирования/возможности проведения хирургического лечения (компьютерная томография, эндоскопия). Рентгенологическое обследование кишечника у пациентов с прогрессирующей формой непроходимости показано, если планируется паллиативная хирургическая операция для облегчения симптомов непроходимости и для дифференциального диагноза между механической непроходимостью и выраженным запором (табл. 1).
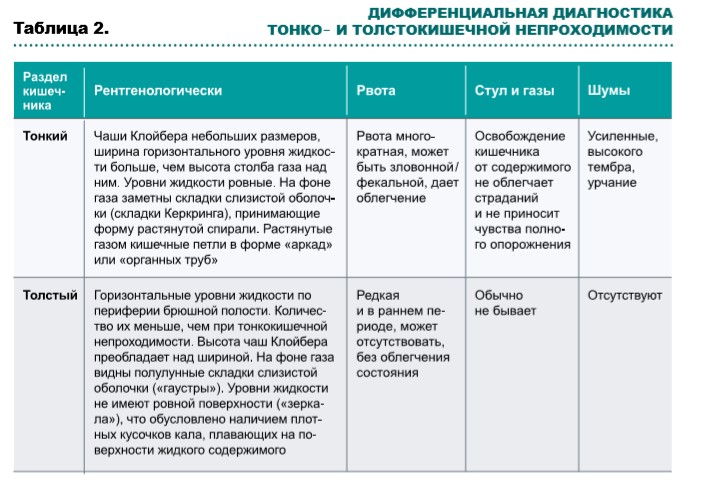
В таблице 2 представлены симптомы, позволяющие провести дифференциальную диагностику тонко- и толстокишечной непроходимости.
Лечение
Зависит от вида непроходимости, остроты ситуации (например, осложнение перитонитом), прогноза (необходимо учитывать траекторию и стадию заболевания) и предпочтений пациента. Тактику лечения следует определять в соответствии с решениями мультидисциплинарной команды специалистов, пациента и его семьи. Непроходимость кишечника в паллиативной сфере редко бывает острой.
Медикаментозное лечение непроходимости
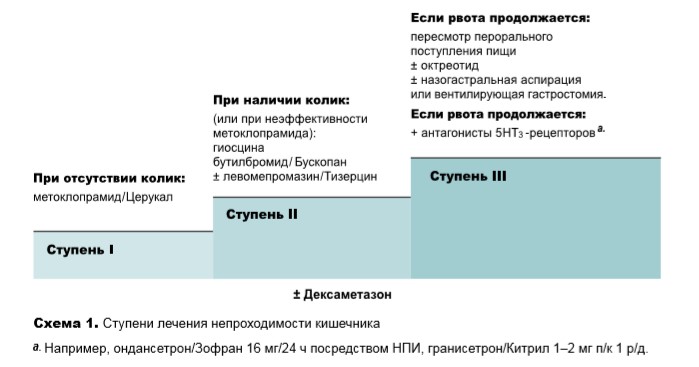
Медикаментозное лечение следует фокусировать, главным образом, на купировании боли, тошноты и рвоты и, по возможности, на разрешении частичной непроходимости. Введение препаратов осуществляется, как правило, посредством непрерывной подкожной инфузии (НПИ) или подкожно (п/к). Представленная ниже ступенчатая схема (схема 1) отражает общий подход к лечению. Может потребоваться титрование доз лекарственных препаратов в течение нескольких дней для достижения оптимального эффекта.
Ступень I. Возможная функциональная обструкция (отсутствие колик, нарушения перистальтики):
Ступень II. Возможная механическая обструкция
Ступень III (когда применения гиосцина бутилбромида недостаточно для контроля над рвотой, либо он недоступен, либо для наступления более быстрого облегчения):
Если рвота продолжается, необходимо ограничить поступление пищи через рот: возможно, необходима назогастральная аспирация или вентилирующая/разгрузочная гастростомия.
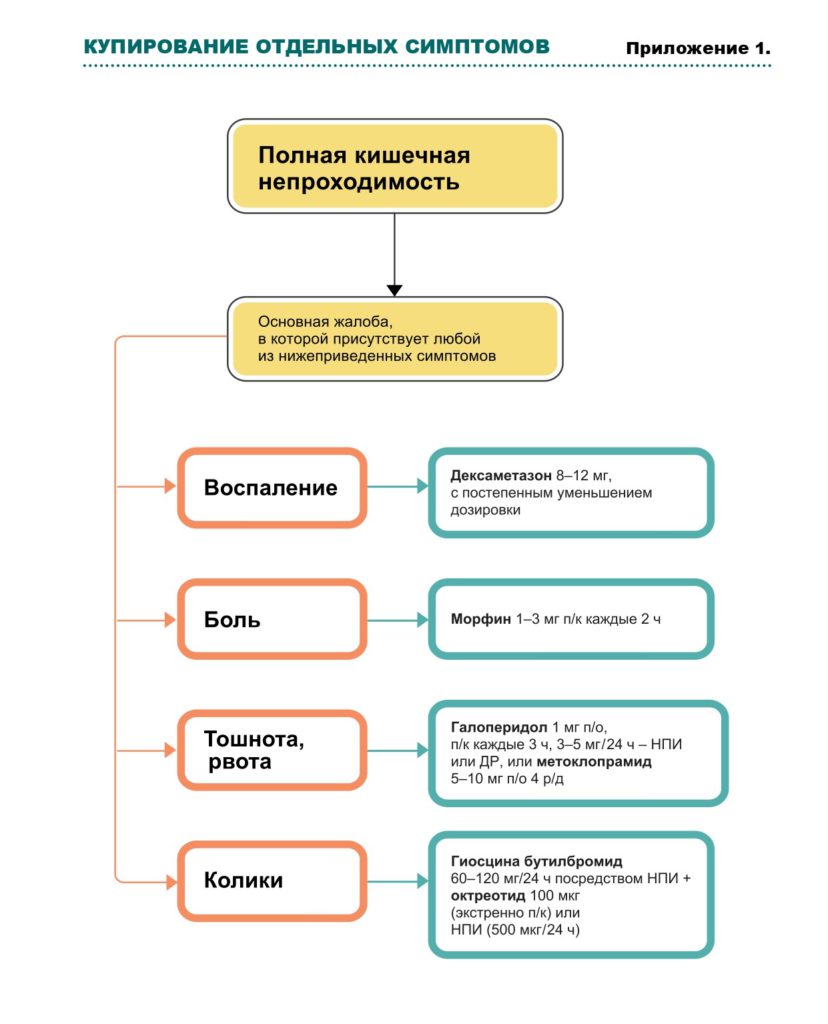
Купирование отдельных симптомов (см. также Приложение 1)
Уменьшение отека кишечной стенки и периопухолевого отека ‒ дексаметазон: дозы подбираются индивидуально из расчета 6‒8 мг 1‒3 р/д п/к или в/в (8‒16 мг п/к или в/в в первую половину дня). Действует также как ко-анальгетик и антиэметик. Если есть положительный эффект, лечение может быть продолжено перорально. В случае неэффективности в течение трех дней ‒ отменить. Но если пациент получал дексаметазон более длительное время, отмену следует производить постепенно, уменьшая дозу на 2 мг каждые три дня.
Стимуляция моторики ЖКТ ‒ метоклопрамид 30‒120 мг/24 ч НПИ или дробно (ДР) п/к каждые 4‒6 ч. Следите за клиникой: при усилении колик ‒ отменить.
Колики ‒ опиоиды НПИ, ДР, защечно, сублингвально или трансдермально для надлежащей адсорбции обезболивающих, что не может обеспечить пероральный прием; дозу титровать. При персистирующих, несмотря на прием опиоидов, коликах назначают антихолинэргические препараты: гиосцина бутилбромид (Неоскапан, Бускопан, Спанил) 40‒ 100мг/24 ч НПИ или ДР). Препараты уменьшают моторику кишечника, в результате снижается секреция жидкостей и перистальтика гладкой мускулатуры. Дозу антихолинэргических препаратов следует уменьшить после 1‒2 дней применения; если нет стула, в этом случае следует подумать о хирургическом вмешательстве. Если это невозможно/нецелесообразно, назначается гиосцина бутилбромид п/о 10 мг 4 р/д.
Хроническая боль ‒ опиоиды НПИ, ДР, защечно, сублингвально или трансдермально, чтобы обеспечить надлежащую адсорбцию обезболивающих; дозу титровать.
Запор ‒ слабительные: вазелиновое масло (наиболее безопасный препарат, от 1 до 5 чайных ложек от 1 до 4 р/д); докузат/ Норгалакс (несовместим с вазелиновым маслом) ‒ только при возможности ректального применения; лактулоза/Дюфалак ‒ с осторожностью титровать дозу, начиная с 3‒5 мл (способствует повышению осмотического давления и, как следствие, увеличению объема кишечного содержимого); очистительные клизмы с осторожностью (предпочтительно масляные, небольшого объема 100‒200 мл); мануальное освобождение прямой кишки (с обезболиванием).
Стентирование/стомирование
К ним прибегают в тех случаях, когда консервативное лечение непроходимости ЖКТ у пациентов с прогнозом жизни более двух месяцев в течение 48‒72 ч не приносит результатов.
Эзофагальная непроходимость
Для облегчения дисфагии у пациентов с раком пищевода или проксимальных отделов желудка используется стентирование и бужирование. Эндоскопически введенные стенты довольно эффективно смягчают симптомы непроходимости, избавляя больного от наложения стомы. У большинства пациентов быстро наступает облегчение. Смертность от данной процедуры низкая, но частота осложнений является относительно высокой. Возможные осложнения: боли в грудной клетке, требующие дополнительного обезболивания ‒ обычно разрешаются в течение 2‒3 дней, кровотечение, перфорация пищевода, образование свищей, гастроэзофагальный рефлюкс, аспирация, компрессия дыхательных путей.
Назогастральный зонд обеспечивает декомпрессию и может помочь проконтролировать тошноту, но необходимо избегать его длительного использования.
Непроходимость привратника двенадцатиперстной кишки
Стенты/бужи/зонды. Противопоказания для стентирования ‒ состояние пациента, перфорации кишечника с перитонитом, стеноз нижней трети прямой кишки (может вызвать тенезмы, недержание, риски миграции стента), множественные участки непроходимости ниже места стентирования, перитонеальный карциноматоз. Наиболее частые осложнения стентирования данного отдела ЖКТ: обструкция желчных путей (50%), миграция стента (до 14%), повторная непроходимость (до 10%), перфорация кишечника (от направляющей стента), некроз от давления, баллонная дилатация и др. (до 6%), кровотечение (5%), функциональные нарушения стента (неспособность пройти место сужения, проблемы с раскрытием, до 4%), прорастание опухолью (2%), фистула (1%). Смертность процедуры до 4%.
Гастроеюностомия. Обеспечивает более длительную выживаемость и более низкий риск необходимости повторного вмешательства, чем стентирование пациентов со злокачественной непроходимостью выходных отделов желудка. Однако в краткосрочной перспективе стентирование более благоприятно.
Проведение гастроеюностомии показано при долгосрочном прогнозе жизни.
Чрескожная гастростомия пациентов с непроходимостью гастродуоденального отдела или проксимальных отделов тонкого кишечника и постоянной рвотой может облегчить симптомы и производится в тех случаях, когда максимально возможное медикаментозное лечение неэффективно. Это позволит избежать необходимости длительного использования назогастрального зонда, декомпрессировать кишечник и облегчить тошноту и рвоту. Пациенты могут даже наслаждаться едой и питьем, эвакуируя желудочное содержимое через гастростому.
Абсолютные противопоказания для постановки гастростомы: портальная гипертензия, массивный асцит, предрасположенность к кровотечениям, активная язвенная болезнь желудка; относительные: множественные предыдущие хирургические вмешательства в области верхней части живота, колоностомия, инфицированные повреждения живота.
Осложнения чрезкожной гастростомы: кровотечения из перистомы или стенки кишечника, ретроперитонеальная/желудочная эрозия или изъязвление, перфорация или перитонит, фистула, миграция стента (может вызвать непроходимость выходной части желудка, панкреатит, холангит, обструкцию или перекрут катетера, попадание желудочного содержимого на кожу).
Непроходимость дистальных отделов тонкого/толстого кишечника
Данные исследований показывают, что выживаемость пациентов после стентирования и других хирургических вмешательств при непроходимости данного отдела ЖКТ составляет 56%, а продолжительность жизни не превышает 60 дней. Хирургические анастомозы с шунтированием могут облегчить состояние больного и улучшить качество жизни последних дней. Эти процедуры проводятся в случае, если медикаментозное лечение неэффективно, а ожидаемое время жизни несколько недель или месяцев.
Хирургическое вмешательство, например, паллиативная резекция, наложение анастомоза или колостомия эффективны для пациентов при наличии описанных ниже критериев:
Дополнительные важные показатели состояния, свидетельствующие в пользу хирургического лечения: отсутствие асцита, обусловленного карциноматозом; большой пальпируемой опухоли в брюшной полости; отдаленных метастазов, особенно в легких; плеврального выпота или данных печеночной и почечной недостаточности.
Осложнения после хирургических вмешательств достаточно высоки: фекальный свищ (7‒ 10%); повторная непроходимость (30‒40%); расхождение швов; сепсис.
Полезные советы
Во всех случаях: тщательный уход за полостью рта, лед для рассасывания.
Некоторые пациенты, ухаживающие за ними родственники или персонал озабочены ограничением поступления калорий с пищей через рот: в этом случае необходимо провести беседу.
Если обструкция частичная, рекомендовано изменение питания, например:
Большинство пациентов нуждаются в подкожных инфузиях лекарственных препаратов, так как прием и адсорбция медикаментов через рот неэффективны.
Необходимо регулярно пересматривать схему лечения, так как симптомы могут меняться и разрешаться спонтанно.
Благодарим за помощь в подготовке материалов:
Кравченко Т.В. (главного врача ГБУЗ ЦПП ДЗМ),
Гуркину С.П. (заместителя главного врача по организации стационарной помощи ГБУЗ ЦПП ДЗМ),
Ибрагимова А. Н. (руководителя филиала «Первый Московский Хоспис им. Веры Миллионщиковой» ГБУЗ ЦПП ДЗМ).
Скачать практическое руководство «Кишечная непроходимость в паллиативной помощи» в формате pdf можно здесь:
Острая кишечная непроходимость
Острая кишечная непроходимость – нарушение пассажа по тонкой или толстой кишке в результате появления механического препятствия или нарушения моторики кишечника. Патология требует экстренного лечения. Летальность при этом заболевании по оценкам разных авторов составляет 5-8%. В клинике НАКФФ для восстановления проходимости кишечника используется консервативная терапия, малоинвазивные процедуры и хирургические операции.
Тонкокишечная непроходимость
У большинства пациентов нарушение проходимости кишечника происходит на уровне тонкой кишки. В 70% случаев причина этой патологии – спаечный процесс. Спайки образуются после хирургических операций, реже – после травм, воспалительных процессов.
Кроме механической, бывает ещё и функциональная непроходимость, связанная с нарушением перистальтики. Она обычно вызвана воспалительными патологиями (включая перитонит), травмами, медицинскими препаратами.
Тонкокишечная непроходимость сопровождается тяжелыми водно-электролитными нарушениями. Особенно опасна странгуляционная форма, которая сопровождается отмиранием стенки кишки. Она требует проведения хирургической операции в течение 2 часов после поступления больного в стационар.
Обтурационная форма непроходимости более благоприятная. В 80% случаев эффекта удается достичь с помощью консервативной терапии. Если эффекта нет в течение 12 часов, проводят операцию.
Хирургическое лечение предполагает рассечение спаек для восстановления проходимости кишки. Операции могут проводиться как лапароскопическим, так и лапаротомным доступом (через большой разрез на животе). По возможности хирург отдает предпочтение малоинвазивной операции. Она технически более сложная, но уменьшает послеоперационную боль, ускоряет реабилитацию, сокращает время пребывания в больнице и уменьшает риск послеоперационных грыж. К тому же, после открытых операций образуется большое количество новых спаек, которые могут вызывать кишечную непроходимость в будущем.
Толстокишечная непроходимость
На непроходимость толстой кишки приходится всего 5% случаев заболевания. В основном они связаны с колоректальным раком.
Варианты лечения в таких ситуациях:
По возможности врач удаляет часть кишечника вместе опухолью и формирует анастомоз – сшивает концы кишки, чтобы восстановить непрерывность пищеварительного тракта.
Что делать при непроходимости кишечника при онкологии
Лечение рака толстой кишки, осложненного острой непроходимостью, до настоящего времени остается одним из сложных вопросов неотложной хирургии и онкологии [1—11]. При достижениях современной хирургии и интенсивной терапии количество летальных исходов и осложнений все же достигает 15—34 и 32—64% соответственно [7, 10, 11]. Остается высоким и процент паллиативных оперативных вмешательств [3, 5, 9]. При так называемых радикальных операциях, выполненных в экстренном порядке на высоте непроходимости, в большинстве наблюдений не удается из-за тяжести состояния больного или недостаточной подготовки хирургической бригады произвести онкологически обоснованное оперативное вмешательство в полном объеме [1]. Наряду с этим при раке толстой кишки, осложненным острой непроходимостью, практически не проводится предоперационная химиолучевая или интраоперационная внутрибрюшная и внутритазовая химиотерапия, в связи с чем отдаленные результаты остаются неутешительными, 5-летняя выживаемость зачастую не превышает 35—40% [6, 10].
Цель исследования — улучшение результатов лечения больных раком толстой кишки, осложненным острой непроходимостью, путем совершенствования хирургической тактики и создания условий для проведения комбинированных и комплексных методов лечения.
Материал и методы
Под нашим наблюдением находились 442 больных раком толстой кишки, осложненным острой непроходимостью. Все больные были госпитализированы в хирургические отделения Республиканской клинической больницы скорой медицинской помощи Владикавказа в экстренном порядке. В течение первых 24 ч поступили 83 (18,7%) больных, в сроки после 24 ч — остальные больные, в том числе 33,1% пациентов через 4 сут и более.
Среди больных мужчин было 254 (57,5%), женщин — 188 (43,5%). Возраст больных составил от 40 до 92 лет (в среднем 71,3±3,7 года). Пожилой возраст и поздняя госпитализация обусловили и большое количество сопутствующих заболеваний, и тяжелое состояние при поступлении. Только у 21 (4,7%) больного выявлена I степень тяжести физического состояния, у 161 (36,4%) — II степень, у 215 (48,6%) — III степень и у 45 (10,1%) больных — IV степень (классификация ASA).
У 250 (56,6%) больных опухоль локализовалась в ободочной кишке: у 32 (12,8%) — в восходящей ободочной кишке, у 15 (6,0%) — в поперечной ободочной, у 51 (20,4%) — в нисходящей и у 152 (60,8%) больных — в сигмовидной кишке. У 192 (43,4%) пациентов опухоль локализовалась в прямой кишке: у 24 (12,5%) больных — на расстоянии до 7 см от края анального канала, у 43 (22,4%) — от 7 до 12 см, у 125 (65,1%) — выше 12 см.
У 380 (85,9%) больных выявлена аденокарцинома различной степени дифференцировки, у 29 (6,6%) — недифференцированный рак, у 25 (5,7%) — муцинозная аденокарцинома, у 8 (1,8%) — перстневидно-клеточный рак.
У 192 (43,4%) больных раком толстой кишки, осложненным острой непроходимостью, имели место регионарные или отдаленные метастазы или распространение опухоли на соседние органы.
При обследовании всех поступивших больных, помимо общеклинических методов, применяли пальцевое исследование прямой кишки, обзорную рентгенографию брюшной полости, УЗИ, колоноскопию (ректороманоскопию) или ирригографию, в 248 наблюдениях выполнили компьютерную томографию.
Была использована разработанная в нашей клинике классификация острого нарушения проходимости при раке толстой кишки (В.З. Тотиков, 1993). Выделяли 4 стадии острой обтурационной толстокишечной непроходимости по клиническому течению на фоне декомпрессионной терапии. Разработали и использовали во всех 442 наблюдениях специальную лечебно-диагностическую программу (см. рисунок).

Результаты
Обследование больных начинали с общеклинических и лабораторных методов исследования. После общего осмотра у 47 (10,6%) больных была выявлена клиническая картина острой кишечной непроходимости и перитонита (IV стадия обтурационной толстокишечной непроходимости). В этих наблюдениях после предоперационной подготовки, направленной на коррекцию водно-электролитных и сердечно-сосудистых нарушений, в течение 2—3 ч выполнили оперативные вмешательства: в 5 — операцию Лахея, в 26 — операцию Гартмана, в 7 — операцию Микулича и в 9 — лапаротомию с наложением двуствольной колостомы. Из последних 9 пациентов 2 больным операбельным раком прямой кишки на втором этапе произвели ее экстирпацию (табл. 1).

Остальным 395 (89,4%) больным произвели обзорную рентгенографию органов брюшной полости. После выявления признаков обтурационной толстокишечной непроходимости в течение 6—7 ч назначали активную декомпрессионную и корригирующую терапию, по окончании которой во всех этих наблюдениях выполняли контрольную обзорную рентгенографию, а в 348 из них — ультразвуковое исследование органов брюшной полости.
После контрольной обзорной рентгенографии и УЗИ брюшной полости у 136 (34,4%) больных выявлена I стадия острой обтурационной толстокишечной непроходимости, т. е. прогнозировано временное, но полное разрешение непроходимости, что было подтверждено при наблюдении этих пациентов в течение 24—30 ч.
В последующем, вплоть до оперативного вмешательства, в качестве декомпрессионной терапии назначали только вазелиновое масло по 30 мл 3—4 раза в сутки на фоне бесшлаковой диеты и нутритивной поддержки. Только накануне операции вновь назначали очистительные клизмы. Кроме этого, в комплекс предоперационной подготовки были включены терапия, направленная на коррекцию метаболических и сердечно-сосудистых нарушений, лечение сопутствующих заболеваний и профилактика воспалительных осложнений.
После разрешения непроходимости во всех 136 наблюдениях выполнили ультразвуковое исследование и КТ для оценки локорегиональной распространенности опухолевого процесса и наличия метастазов.
В этой группе 4 больным дистальным раком прямой кишки была проведена крупнофракционная предоперационная лучевая терапия в суммарной очаговой дозе 25 Гр и 6 больным — лучевая терапия в дозе 50 Гр в комбинации с химиотерапией фторпиримидинами. Радикальное оперативное вмешательство этим больным выполняли после окончания химиолучевой терапии, во время которой больные получали специальную диету и вазелиновое масло по 30—50 мл 3—4 раза в день, а при необходимости и очистительные клизмы.
Остальным больным в течение 7—10 дней после разрешения непроходимости была произведена одноэтапная операция. В 6 наблюдениях при нерезектабельном раке наложена двуствольная колостома проксимальнее опухоли, в остальных наблюдениях выполнена радикальная или циторедуктивная одноэтапная операция. У 35 больных во время операции провели внутрибрюшную и у 4 пациентов — внутритазовую химиотерапию.
У 160 (40,5%) больных через 6—7 ч после декомпрессионной и корригирующей терапии на основании клинической картины, рентгенологических и ультразвуковых данных установлена II стадия острого обтурационного нарушения проходимости толстой кишки. У 42 из них предпринята попытка эндоскопической реканализации опухолевого канала. У 23 (54,8%) больных она была успешной, этим больным в дальнейшем проводили такое же лечение, как больным с I стадией. В 5 наблюдениях проведена предоперационная лучевая и химиолучевая терапия, в 6 — интраоперационная внутрибрюшная химиотерапия.
Остальным 138 (86,2%) больным оперативное вмешательство было выполнено в течение 24 ч после коррекции водно-электролитных, белковых и сердечно-сосудистых нарушений (см. табл. 1).В том числе 15 (9,4%) больным с анестезиологическим риском I— II степени по ASA и локализацией опухоли в правых отделах ободочной кишки произведена первичная резекция: 6 — гемиколэктомия с наложением анастомоза, 9 — операция Лахея.
В 122 (76,2%) наблюдениях наложили стому через минидоступ: двуствольную илеостому (27 больных), двуствольную трансверзостому в правом подреберье (81), одноствольную сигмостому (6) и двуствольную колостому над опухолью при нерезектабельном раке (8).
На втором этапе хирургического лечения 103 (64,4%) больным со II стадией обтурационного нарушения проходимости толстой кишки была выполнена резекция участка толстой кишки с опухолью с формированием анастомоза в области ранее наложенной стомы (табл. 2).

В 3 (1,9%) наблюдениях при локализации опухоли в правых отделах произведена правосторонняя гемиколэктомия с ликвидацией стомы и наложением анастомоза. 102 пациентам из 103 оперативные вмешательства были выполнены в течение 7—10 сут после коррекции метаболических и сердечно-сосудистых нарушений, еще 1 пациенту с локализацией опухоли в среднеампулярном отделе прямой кишки — после предоперационной химиолучевой терапии. Такая же тактика использована и у 6 (3,7%) пациентов с дистальной опухолью прямой кишки и ранее наложенной через минидоступ одноствольной сигмостомой. Последним 6 пациентам после окончания курса химиолучевой терапии выполнили экстирпацию прямой кишки.
Интраоперационно 36 (22,5%) больным была проведена внутрибрюшная и 5 (3,1%) пациентам — внутритазовая химиотерапия.
На втором этапе всем 9 (5,6%) больным после операции Лахея в течение 2—3 мес осуществляли реконструктивно-восстановительную операцию с закрытием стомы.
Третий этап — восстановление естественного пассажа — провели у 23 больных с илеостомой и у 102 пациентов с трансверзостомой (табл. 3).

Больным с трансверзостомой восстановительную операцию выполняли через 2—4 мес после радикального лечения, больным с двуствольной илеостомой на начальном этапе исследования — в такие же сроки, а в последующем при отсутствии воспалительных изменений в брюшной полости — через 10—15 дней после радикального этапа.
Из 99 больных с III стадией острого обтурационного нарушения проходимости толстой кишки у 44 предприняли попытку эндоскопической реканализации опухолевого канала, в 15 (34,1%) наблюдениях она увенчалась успехом, в связи с чем все 15 пациентов были оперированы в отсроченном порядке после дополнительного обследования и предоперационной подготовки (см. табл. 1). В 2 из этих наблюдений проведена предоперационная лучевая терапия и в 3 — интраоперационная внутрибрюшная химиотерапия. Из остальных 83 больных 15 (15,1%) в течение 12 ч была наложена декомпрессионная двуствольная илеостома, 49 (49,5%) — двуствольная трансверзостома, 3 (3,03%) — одноствольная сигмостома, 9 (9,1%) больным с нерезектабельной формой рака — двуствольная колостома над опухолью. При анестезиологическом риске не более II по ASA и правосторонней локализации опухоли 7 (7,1%) пациентам была выполнена радикальная операция: 5 — операция Лахея, 2 — правосторонняя гемиколэктомия с формированием анастомоза.
Второй этап хирургического лечения был выполнен 69 (69,7%) больным с III стадией острого обтурационного нарушения проходимости толстой кишки (см. табл. 2), 61 (61,6%) с декомпрессионной илео- или трансверзостомой: 59 пациентам произвели резекцию участка толстой кишки с опухолью и наложением анастомоза под протекцией стомы, 2 больным с локализацией опухоли в правых отделах — правостороннюю гемиколэктомию с ликвидацией стомы и наложением анастомоза.
В 58 наблюдениях из 61 радикальные оперативные вмешательства были выполнены в течение 7—10 сут после поступления на фоне коррекции метаболических и сердечно-сосудистых нарушений. Остальным 3 больным с локализацией опухоли в средне- и нижнеампулярном отделе прямой кишки оперативные вмешательства произведены после предоперационной лучевой и химиолучевой терапии. Во время радикального этапа 24 (24,2%) больным провели внутрибрюшную и 2 (2,0%) — внутритазовую химиотерапию.
После операции Лахея в 5 наблюдениях в течение 2—3 мес осуществлен второй восстановительный этап лечения.
Третий восстановительный этап был выполнен 10 (10,1%) пациентам с двуствольной илеостомой и 48 (48,5%) больным с двуствольной трансверзостомой (см. табл. 3). Больным с трансверзостомой восстановительные операции производили в течение 2—4 мес после первичного лечения. На начальном этапе исследования у 6 больных с двуствольной илеостомой вмешательство осуществляли в такие же сроки, а в последующем при отсутствии воспалительных изменений в брюшной полости (4 больных) — через 10—15 дней после радикального этапа.
После всех этапов хирургического лечения умерли 22 (5,0%) больных, из них на первом этапе 21 пациент, в том числе 13 с острым перитонитом. На втором радикальном этапе умер один больной, на третьем этапе летальных исходов не было. Послеоперационные осложнения на первом этапе были выявлены у 48 (10,8%) больных, на втором — у 37 (16,8%) и на третьем этапе — у 9 (5,6%) больных.
У 25 (37,3%) больных с локализацией рака в средне- и нижнеампулярном отделе прямой кишки провели лучевую или химиолучевую терапию. В 115 (26,0%) наблюдениях на этапе радикальных оперативных вмешательств осуществлена внутрибрюшная или внутритазовая химиотерапия. После радикального этапа послеоперационная системная химиотерапия была проведена в 342 (84,4%) наблюдениях. Радикальный этап всем пациентам (кроме 31 больного с острым перитонитом) был выполнен специально подготовленными хирургами, имеющими сертификат онколога.
Таким образом, предложенная классификация обтурационного нарушения проходимости толстой кишки и лечебно-диагностический алгоритм позволяют четко определить длительность предоперационной подготовки, объем и вид хирургического пособия, а также снизить частоту послеоперационных осложнений и летальных исходов.
Разработанный лечебно-диагностический алгоритм дает возможность создать условия для выполнения радикального этапа подготовленными специалистами и использования комбинированных и комплексных методов лечения рака толстой кишки, осложненного острой непроходимостью. Внедрение трехэтапных оперативных вмешательств с укороченным межоперационным периодом не увеличивает период реабилитации, позволяет снизить частоту несостоятельности швов анастомоза и отказаться от операции по типу Гартмана, а также избежать тяжелого реконструктивно-восстановительного этапа лечения.
Авторы заявляют об отсутствии конфликта интересов.
Комментарий
В преобладающем большинстве случаев острая кишечная непроходимость (ОКН) является осложнением рака толстой кишки и развивается у 15—20% больных, как правило, у пациентов старше 60 лет, отягощенных выраженными сопутствующими заболеваниями. По сравнению с плановыми операциями, экстренное вмешательство сопряжено с более высокими показателями осложнений, летальности и плохим прогнозом выживаемости. Больные с манифестацией рака толстой кишки в виде ОКН имеют в два раза более высокий риск смерти от основного заболевания, несмотря на попытку радикального лечения [5]. По данным L. Smothers и др. (2003), экстренное вмешательство является независимым негативным прогностическим фактором, увеличивающим число осложнений и летальности, связанных с операцией (64 и 34% соответственно) [6]. Помимо высокого уровня осложнений и послеоперационной летальности, в экстренной ситуации зачастую не представляется возможность выполнить оперативное вмешательство с соблюдением принципов онкологического радикализма. Остается неясным, могут ли на самом деле всегда безупречно быть реализованы эти принципы в сценарии ургентной хирургии. Следует принимать во внимание некоторые клинические и хирургические детали, осложняющие ход неотложного вмешательства по поводу ОКН: существующая опасность дальнейшего ухудшения состояния исходно «тяжелого» пациента; возможность удлинения времени оперативного вмешательства; трудность осуществления необходимой лимфодиссекции в условиях значительно расширенной толстой кишки; высокий риск интраоперационной перфорации кишечной стенки и загрязнения брюшной полости. Неотъемлемым атрибутом радикальной хирургической операции является достижение отрицательных границ резекции (R0). Как было показано, частота выполнения операций в объеме R1 в плановой хирургии составляет 10,4%, однако она удваивается при экстренных оперативных вмешательствах, достигая 23,6%. Наличие позитивных краев резекции ассоциировано с гораздо большим числом местного и отдаленного рецидивирования и худшей 5-летней безрецидивной и общей выживаемостью в сравнении с R0 операциями [2, 3]. В плановой хирургии многие из независимых факторов риска R1 резекции могут быть идентифицированы на этапе предоперационного обследования и обсуждены с участием мультидисциплинарной команды специалистов. Полученные данные способны привести к существенному изменению лечебной стратегии, например, к назначению неоадъювантной химиолучевой терапии, расширению объема резекции или выбору открытого, а не лапароскопического доступа. Такие решения являются ключевыми, позволяющими свести к минимуму риск нерадикальных вмешательств. В условиях ургентной операции такое планирование не представляется возможным, поэтому чрезвычайно актуальным является поиск методов лечения осложненных форм рака толстой кишки, позволяющих «вывести» пациента из группы ургентных больных и выполнить оперативное вмешательство, направленное на удаление злокачественной опухоли в плановом порядке.
В статье, опубликованной коллективом авторов из Северо-Осетинской государственной медицинской академии Минздрава РФ, анализируется опыт лечения одной из наиболее сложной и часто встречающейся в хирургической практике категории больных. Предложен лечебно-диагностический алгоритм, основанный на использовании собственной классификации острого нарушения проходимости при раке толстой кишки. ОКН рассматривается как стадийный процесс и, в зависимости от выраженности симптомов и эффекта от проводимой терапии, подразделялся на 4 стадии. Примененная лечебно-диагностическая программа напрямую зависела от стадии непроходимости. При четвертой — выполнялось экстренное оперативное вмешательство после короткой предоперационной подготовки, остальным же проводились лечебно-диагностические мероприятия. В случае успеха консервативного лечения операции выполнялись в отсроченном порядке через 7—10 дней. При неэффективности консервативных мероприятий, нарастании явлений кишечной непроходимости через 12—24 ч осуществлялись хирургические вмешательства. При отсутствии тяжелых осложнений со стороны первичной опухоли, таких как перфорация, абсцедирование, кровотечение, авторы в качестве первого этапа лечения формировали проксимальные разгрузочные илео- или колостомы. После стабилизации состояния больного и дообследования, вторым этапом выполняли резекцию толстой кишки с соблюдением онкологических принципов. При этом для протекции сформированного межкишечного анастомоза сохранялась ранее наложенная кишечная стома. Третьим этапом восстанавливалась непрерывность желудочно-кишечного тракта.
Идея трехэтапного лечения осложненного рака толстой кишки не нова. Формирование проксимальной кишечной стомы с целью разрешения толстокишечной непроходимости известна более 100 лет и широко применяется в современной хирургической практике у тяжелой категории пациентов. Отечественный хирург Г.Ф. Цейдлер (1898) предложил при нарушении кишечной проходимости, обусловленной раком левых отделов толстой кишки, не выполнять первым этапом широкую лапаротомию, а из минидоступа в правой подвздошной области формировать разгрузочную цекостому. Вторым этапом производилась резекция, после чего ликвидировался кишечный свищ. Метод предварительной декомпрессии был воплощен в жизнь австрийским хирургом H . Schloffer в 1903 г.
На сегодняшний день формирование цекостомы считает- ся необоснованным и порочным методом декомпрессии у пациентов с ОКН, так как эта операция не позволяет добиться полного отключения из пассажа дистальных отделов толстой кишки.
Современное обоснование операции Цейдлера—Шлоффера лежит в наличии высокого риска несоблюдения принципов онкологического радикализма во время экстренного хирургического вмешательства, что, безусловно, сказывается на результатах лечения этой категории больных. Так, по данным S. Ascanelli (2003), показатели 5-летней выживаемости составили 52% у больных, оперированных в плановом порядке, по сравнению с 39% у пациентов, подвергшихся неотложному хирургическому вмешательству [2]. Наиболее очевидным объяснением снижения общей выживаемости у пациентов, оперированных на фоне острой кишечной непроходимости, может служить дискредитация качества хирургической резекции.
Следует отметить, что указанная авторами стратегия лечения полностью коррелирует с клиническими Рекомендациями по лечению пациентов с острой кишечной непроходимостью опухолевой этиологии [1]. Данные рекомендации были утверждены на заседании Профильной комиссии «Колопроктология» Экспертного Совета Минздрава России с участием представителей Ассоциации колопроктологов России, Ассоциации онкологов России, Российского общества хирургов 23 октября 2014 г. в рамках Всероссийской научно-практической конференции «Актуальные вопросы колопроктологии» (Смоленск). Стадии кишечной непроходимости, взятые авторами в основу классификации ОКН, соотносятся с предложенными в Рекомендациях, а именно первая стадия отображает компенсированную ОКН, вторая — субкомпенсированную, четвертая — декомпенсированную, третья — занимает промежуточное положение между субкомпенсированной и декомпенсированной и отличается по наличию у больного органных дисфункций.
В представленной статье наглядно демонстрируются преимущества использования лечебно-диагностического алгоритма, предлагаемого авторами и представленного в клинических Рекомендациях, который позволяет улучшить результаты лечения больных с острой опухолевой кишечной непроходимостью.
Единственным ограничением этой работы служит ее ретроспективный и описательный характер. На сегодняшний день существует очевидная необходимость в проведении мультицентровых проспективных исследований, направленных на улучшение результатов лечения больных с осложненным колоректальным раком и оценивающих не только непосредственные, но и отдаленные результаты хирургических вмешательств при ОКН опухолевого генеза.
Руководитель отдела онкологии и хирургии ободочной кишки ФГБУ «ГНЦК им. А.Н. Рыжих» МЗ РФ д.м.н., проф. С.И. Ачкасов