Неоперабельная опухоль головного мозга: современные подходы к лечению
Хирургическая операция – основной метод лечения больных с доброкачественными опухолями и один из наиболее эффективных способов борьбы с абсолютным большинством злокачественных новообразований, обнаруженных на ранних стадиях. Однако если патологический очаг находится в головном мозге, он может быть признан неоперабельным даже тогда, когда «ведет себя» неагрессивно, растет медленно и выявляется своевременно.
К неоперабельным опухолям головного мозга относят новообразования, удаление которых хирургическим путем связано с угрозой для жизни пациента, высоким риском его инвалидизации или резкого прогрессирования заболевания.
В том числе, такой диагноз может быть поставлен, если:
Чем больше из вышеперечисленных особенностей присуще конкретному новообразованию, тем выше вероятность, что в диагнозе может появиться фраза «неоперабельная опухоль головного мозга», которую человек нередко воспринимает, как приговор. Эти опасения нельзя назвать беспочвенными, ведь еще несколько десятилетий назад у такого пациента действительно было мало шансов победить болезнь или, хотя бы, замедлить ее развитие.
Причины неэффективности химиотерапевтического и лучевого лечения устаревшими методами
В связи с особой организацией и функциями центральной нервной системы, эффективность облучения опухоли мозга на традиционных радиотерапевтических установках была крайне низкой, равно как и польза от приема химиопрепаратов предыдущего поколения. Происходило это потому, что:
С появлением в арсенале нейроонкологов новых технологий, оборудования и препаратов ситуация кардинальным образом изменилась.
Современные подходы к лечению больных с неоперабельными опухолями головного мозга
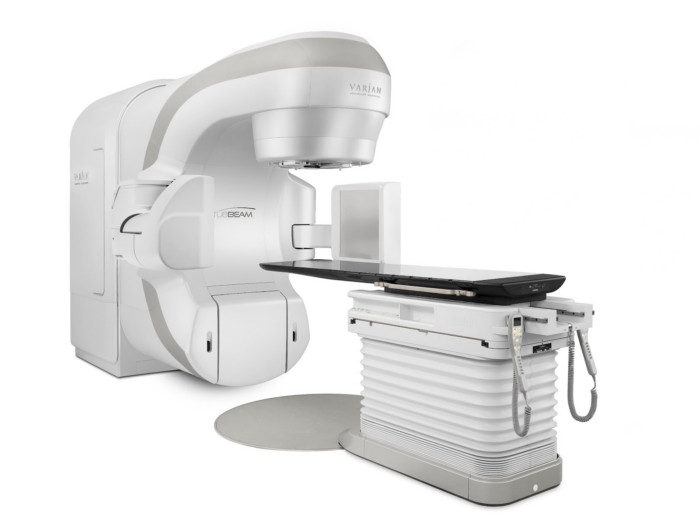
Решить проблему с эффективным и безопасным лучевым лечением позволило внедрение в клиническую практику радиохирургических аппаратных комплексов Гамма-нож и Кибер-нож, систем TrueBeam и Triology с инновационными линейными ускорителями, томотерапевтических установок с многолепестковыми коллиматорами, а также открытие центров протонной терапии.
Выбор наиболее подходящего метода, аппарата и схемы лечения определяется с учетом особенностей технологии, опухоли и больного.
С помощью конформной лучевой терапии на установке TrueBeam STx можно быстро и эффективно разрушать неоперабельные новообразования большого размера и сложной формы
Современные препараты и схемы лечения и щадяще. Это дает возможность свести к минимуму вероятность и тяжесть побочных эффектов химиотерапии. Кроме того, в последнее время были синтезированы лекарства, способные успешно преодолевать гематоэнцефалический барьер.
Используемая технология дает надежду значительному числу пациентов с глубокорасположенными/труднодоступными опухолями головного мозга, которым было отказано в оперативном лечении, поскольку оно имело неоправданно высокий риск повреждения жизненно важных отделов головного мозга.
При этом также снижается риск инфицирования, не требуется длительного пребывания в стационаре (1 день по сравнению с 5-10 днями после открытой операции на головном мозге), уменьшается время восстановления, практически не требуется удаления волос и почти не остается рубцов.
Профессор K.Ashkan, нейрохирург клиники Харли Стрит, одной из наиболее авторитетных онкологических клиник Великобритании, подчеркнул, что: «Технология Visualase объединяет лазерную хирургию и робототехнику с использованием принципа «замочной скважины». Точность лазерной абляции обеспечивается МРТ-контролем в реальном времени и роботизированной системой управления ROSA. Гибкий катетер диаметром 1,65 мм и неглубокий костный фиксатор обеспечивают широкий хирургический доступ. Все это позволяет безопасно лечить опухоли головного мозга в местах, которые ранее считались недоступными. Минимально инвазивный характер вмешательства позволяет быстро восстановиться после терапии с минимальной продолжительностью пребывания в больнице. Visualase будет полезен пациентам с целым рядом неврологических и нейрохирургических расстройств, особенно с эпилепсией и опухолями головного мозга».
Таким образом, сегодня шанс на выход в ремиссию с сохранением качества жизни есть даже в самых тяжелых ситуациях – в том числе и у больных, ранее считавшихся безнадежными.
Немного о терминах и ошибочных выводах
У не имеющих медицинского образования пациентов или их родственников иногда возникают сомнения в необходимости удаления опухолевого узла с помощью радиохирургической установки. Связано это с тем, что во врачебном заключении не написано (и не может быть написано) «неоперабельный рак головного мозга», а идет речь об опухоли, новообразовании, очаге неопластического роста и др. Особенно много вопросов вызывает обоснованность облучения доброкачественной опухоли.
В данном случае людей вводят в заблуждение особенности медицинской терминологии. Нужно иметь в виду, что в тканях мозга нет клеток эпителия, которые способны переродиться и дать начало истинной раковой опухоли – карциноме. То есть, рака мозга как такового не существует. Но данное обстоятельство отнюдь не означает, что обнаруженный очаг безобиден. Напротив, высокозлокачественные опухоли мозга отличаются крайне агрессивным «поведением», хотя и не относятся к раковым.
Более того, в ряде случаев доброкачественные узлы могут доставлять не менее серьезные проблемы. Например, если они нарушают кровообращение, сдавливают центры нервной и нейрогуморальной регуляции.
Прогнозы
Эффективность лечения больных с неподлежащими удалению новообразованиями мозга зависит от ряда факторов, среди которых:
Если вам требуется второе мнение для уточнения диагноза или плана лечения, отправьте нам заявку и документы для консультации, или запишитесь на очную консультацию по телефону.
Неоперабельная опухоль
Содержание Скрыть
Примерно 1/3 больных с онкологическими заболеваниями ставят диагноз «неоперабельная опухоль», когда удаление обширных очагов поражения не представляется возможным при помощи хирургического вмешательства. В таких ситуациях специалисты принимают решение о применении других методов лечения. Однако прогнозы в любом случае будут неблагоприятными.
Что такое
Неоперабельная опухоль значит, что злокачественный процесс находится на третьей или четвертой стадии развития и сопровождается распространением метастазов на рядом расположенные внутренние органы и ткани.
На этом этапе новообразование может поражать печень, головной мозг, легкие, почки и костные структуры. Атипичные клетки распространяются через кровоток и лимфоток.
При выборе методов проведения терапевтических мероприятий в обязательном порядке необходимо учитывать такие особенности проявленных клинических признаков, что может послужить отказом в проведении операции, поскольку в итоге полностью удалить злокачественную операцию все равно не удастся. Очаги все равно останутся и произойдет их дальнейшее развитие и распространение.
Основное отличие неоперабельной опухоли от операбельной прежде всего заключается в том, что в первом случае невозможно полностью извлечь раковое новообразование, в то время как во втором такая возможность есть (рак, как правило, находится на 1-2 стадии). Кроме того, при неоперабельности онкопатологии нет никаких шансов на благоприятные прогнозы.
Причины
Невозможность проведения хирургического вмешательства специалисты объясняют следующими причинами:
Согласно статистическим данным, неоперабельный рак в большинстве случаев выявляется в головном мозге. Это объясняется тем, что раковое новообразование расположено в труднодоступном месте и находится близко к нервным ганглиям.
Методы лечения
В случае когда специалисты ставят диагноз «неоперабельная опухоль», для ее лечения применяются альтернативные терапевтические методы, основная задача которых заключается в том, чтобы устранить выраженность проявленной клинической картины, продлить жизнь больному насколько это возможно.
Что такое первичный рак неизвестного происхождения?
Раковая опухоль возникает в случаях, когда клетки начинают бесконтрольно расти. Такую особенность могут приобрести клетки практически любого органа. Кроме того, по мере роста опухоли они с током крови или лимфы могут переноситься в другие области тела, оседать там и давать начало росту новых очагов. Такие очаги называют вторичным раком, или метастазами, а начальную опухоль, соответственно, первичным раком.
Метастазы в любых органах классифицируют в зависимости от того, из какого органа изначально происходит опухоль. Например, вторичный очаг рака легких в печени все равно будет называться раком легких, только получит приставку «вторичный». Иногда не получается определить, в каком именно органе сначала возникла опухоль. Однако при исследовании выявляются ее метастазы в других частях тела. Если их первичный очаг определить не удается, то врачи говорят про первичный рак неизвестного происхождения, или скрытый первичный рак.
Пример выявления
Скрытый первичный рак встречается нечасто. Более того, в ходе дальнейших обследований первичный очаг может обнаружиться. Если так происходит, то опухоль более не считается первичным раком неизвестного происхождения. Ей присваивают название в соответствии с органом происхождения и, опираясь на новые данные, модифицируют схему лечения онкологического заболевания.
На практике это происходит следующим образом:
Однако в ряде случаев даже самое тщательное обследование не позволяет обнаружить первичный очаг. Более того, его не всегда получается найти даже при патологоанатомическом исследовании.
Типы раковых опухолей
Обычно опухоли классифицируют по их первичной локализации. Однако их также можно сгруппировать по типам клеток, по тому, как раковые клетки выглядят под микроскопом. Знание типа клетки может дать врачам ключ к пониманию того, из каких тканей или органов происходит данная опухоль.
Карциномы
Карцинома — это рак, который происходит из клеток, выстилающих внутреннюю или внешнюю поверхности различных органов нашего тела. Такие клетки называются эпителиальными. Наиболее распространенные типы карцином:
1) Плоскоклеточный рак
Самым ярким примером плоских клеток являются клетки, встречающиеся на поверхности кожи. Кроме того, они составляют часть слизистых оболочек многих полых органов. Плоскоклеточный рак может возникать в ротовой полости, в горле, пищеводе, легких, прямой кишке, на шейке матки, во влагалище и некоторых других органах.
2) Аденокарциномы
Эти злокачественные новообразования развиваются из железистых клеток, то есть из тех, которые способны производить какие-либо вещества. Железистые клетки входят в состав очень многих органов нашего тела, в том числе и тех, которые формально не считаются железами. Например, большинство видов раковых опухолей желудка, кишечника и толстой кишки представляют собой именно аденокарциномы и примерно 4 из 10 случаев рака легких также являются аденокарциномами.
Другие виды злокачественных опухолей
Из других типов клеток раковые новообразования возникают реже. К таким опухолям относятся:
Итак, при первичном раке неизвестного происхождения не всегда получается установить орган, где изначально возникла опухоль. Однако, исследуя под микроскопом клетки вторичного очага, чаще всего удается отнести их к одной из пяти категорий:
В дальнейшем эта информация поможет более точно идентифицировать опухоль и в конечном итоге обнаружить ее первичный очаг.
Зачем нужно искать первичный очаг?
Основная причина для поисков начальной опухоли — выбор правильной тактики лечения. Вторичные метастатические очаги состоят из тех же клеток, что и начальная опухоль, даже если развиваются в совершенно других органах. Значит, для их лечения будут эффективны те же препараты, что и для терапии первичного рака, а не те, которые используются при лечении онкопатологий органа, где развился метастаз.
Это имеет особенно важное значение при некоторых формах рака, которые хорошо поддаются лечению определенными химиотерапевтическими или гормональными препаратами. Например, такими особенностями характеризуются многие опухоли молочной железы. Их можно эффективно лечить гормональными средствами. А значит, такие же препараты подойдут и для терапии их метастазов в костях, головном мозге, печени.
К сожалению, предугадать развитие злокачественного заболевания пока практически невозможно. А потому наиболее эффективным способом борьбы с опухолями является выявление рака на 1 стадии развития. В этом случае успешному лечению поддаются более 90% всех злокачественных новообразований. Обнаружить опухоль на начальных этапах возникновения можно только при помощи периодических скринигов. Такие скрининговые программы действуют и в медицинском центре «Анадолу». На первичной консультации специалист-онколог оценит риск развития у вас онкологического заболевания и составит индивидуальный план прохождения профилактических обследований для ранней диагностики рака.
Материал подготовлен по согласованию с врачом «Анадолу», терапевтом и медицинским онкологом Шерефом Комурджу.
Злокачественное новообразование: причины появления, виды и стадии развития
Существует более двухсот разновидностей онкологических заболеваний, которые могут развиваться в любой области человеческого организма. Болезнь провоцируется неконтролируемым появлением атипичных мутировавших клеток, что со временем вызывает нарушение работы отдельных органов и систем организма, а также ухудшает общее самочувствие человека.
Проявление симптомов зависит от того, где расположено злокачественное новообразование и какова стадия его развития. Основными симптомами становятся: общая слабость, ухудшение аппетита, резкая потеря веса, субфебрильная температура, чрезмерная потливость, озноб.
Лечение и шансы на полное выздоровление зависят от стадии злокачественных новообразований, их вида и реакции на различные препараты. Чтобы предотвратить появление онкологии или быстро ее обнаружить, важно знать причины болезни и первые симптомы. Если есть подозрения на злокачественное новообразование, рекомендуется обратиться за консультацией опытного врача-онколога. Наилучшую помощь оказывают в иностранных клиниках.
В Турции пациентам обеспечивается максимально эффективное лечение, быструю и точную диагностику, демократичные цены на услуги.
Причины злокачественных новообразований
Ученые определили ряд причин злокачественных новообразований, способных спровоцировать развитие рака. Для удобства их принято разделять на две большие группы: эндогенные и экзогенные.
Рассмотрим подробнее каждую из них.
Эндогенные причины злокачественных новообразований:
Экзогенные причины злокачественных новообразований:
Виды злокачественных новообразований
Злокачественное образование по строению в первую очередь зависит от тканей, в которых оно сформировалось. По этому признаку различают следующие виды злокачественных новообразований:
По принципу деления злокачественных клеток выделяют гистологические, клинические и морфологические виды опухолей.
По сложности строения бывают простые (образование из одного типа ткани) или сложные виды злокачественных новообразований. Также рак различают по органу или системе, в которых он сформировался: костей, кишечника, яичников, кожи, желудка, молочных желез, предстательной железы, шейки матки, легких и т.п.
Виды злокачественных новообразований по строению клеток, на основе которых они развиваются:
Стадии злокачественных новообразований
По степени агрессивности болезни и ее распространению по организму, различают 4 стадии злокачественных новообразований.
Рассмотрим признаки каждой из них:
Стадии злокачественных новообразований определяются после тщательного обследования и консультации врача-онколога.
Химиоэмболизация печени
Химиоэмболизация печени (называемая также трансартериальной химиоэмболизацией, сокращенно ТАХЭ) – это эндоваскулярный хирургический метод, позволяющий приостановить рост раковой опухоли путем остановки кровотока в питающей опухоль артерии в сочетании с подведением к раковым узлам химиопрепаратов. Химиоэмболизация печени принадлежит к процедурам интервенционной хирургии.
Специфика методики состоит в использовании препаратов сразу двух типов, вводимых в сосуд:
Преимущества химиоэмболизации
Благодаря своей специфике химиоэмболизация, во-первых, наносит «двойной удар» по раковой опухоли. Во-вторых, она дает возможность, используя химиопрепарат в высоких, эффективных дозах, минимизируя при этом вред, наносимый его токсичным эффектом организму в целом. Это обусловлено тем, что при химиоэмболизации химиопрепарат не попадает в системный кровоток – эмболизирующий препарат обеспечивает его доставку непосредственно к раковому узлу.
С учетом того, что рак печени, в отличие от ряда других онкологических заболеваний, практически не восприимчив к системной химиотерапии и химиопрепараты в борьбе с ним эффективны только тогда, когда вводятся в саму печеночную артерию, химиоэмболизация печени дает существенные преимущества.
Одна из главных опасностей злокачественных опухолей печени заключается в том, что рано или поздно они приводят к острой почечной недостаточности, и именно она становится во многих случаях причиной летального исхода. С помощью химиоэмболизации можно не только остановить рост опухоли, но и поддерживать приемлемое качество жизни пациента, сохраняя способность печени функционировать на достаточном уровне.
Химиоэмболизация печени хорошо сочетается с другими методами локальной деструкции злокачественной опухоли – стереотаксической лучевой терапией и радиочастотной аблацией – и ее можно проводить повторно по необходимости, что делает ТАХЭ важной частью комплексной борьбы с раком печени. Может применяться химиоэмбользация и как самостоятельный метод.
В каких случаях проводится химиоэмболизация печени
Проведение химиоэмболизации возможно как при первичном (холангиокарцинома, гепатоцеллюлярная карцинома), так и при метастатическом раке печени. Метастатические очаги в печеночной ткани как правило возникают при раке легких, толстой кишки, молочной железы и простаты.
Важно понимать, что химиоэмболизация является локальным вспомогательным, не радикальным, методом в борьбе с раком печени. Цель ТАХЭ заключается в том, чтобы затормозить рост опухоли, уменьшить ее размеры и позволить печени продолжить функционировать, продлив тем самым жизнь пациенту.
Отправьте документы на почту cc@nacpp.ru. Возможность проведения лечения рассмотрит главный врач клиники Антон Александрович Иванов, онколог-хирург, кмн
Химиоэмболизацию рекомендуют в тех случаях:
Медицинский директор, врач онколог-хирург, к.м.н
Противопоказания для химиоэмболизации печени
Химиоэмболизация обычно не рекомендуется при следующих состояниях:
Также существует ряд случаев, в которых эффективность ТАХЭ потенциально сомнительна:
В отдельных случаях химиоэмболизация может проводиться, несмотря на риски, со сниженной дозой эмболизирующего препарата.
Виды химиоэмболизации печени
На данный момент существуют в общей сложности три вида химиоэмболизации.
При масляной химиоэмболизации, которая начала применяться еще в 80-х годах, в питающий опухоль сосуд вводится масляный рентгеноконтрастный препарат, в котором в свою очередь заключен химиопрепарат. Однако масляный раствор не может блокировать кровоток непосредственно в опухолевой ткани, и с его помощью крайне сложно добиться необходимой высокой концентрации химиопрепарата, доставленного к опухоли. По этой причине эффективность этого вида ТАХЭ довольно низкая. Но его преимущество заключается в том, что масляная химиоэмболизация может быть проведена даже при 70% поражения печеночной ткани. Через полтора – два месяца масляная ТАХЭ проводится повторно. Количество необходимых повторных процедур обычно не менее трех.
В начале XXI века появилась методика химиоэмболизации микросферами. Изобретенные эмболизирующие препараты на основе микросфер, накапливающих, а затем высвобождающих химиопрепарат, позволили повысить доставляемую к опухоли концентрацию химиопрепарата. Именно это делает ТАХЭ микросферами существенно более эффективным видом. Повторная процедура при необходимости возможна уже через 4 недели. Однако данный вид химиоэмболизации применим только в случае, если область поражения не больше 50%.
Нам доверяют 9500 пациентов ежегодно.
Также возможно проведение комбинированной ТАХЭ. Она представляет собой сочетание двух описанных выше видов химиоэмболизации. Сначала производится ТАХЭ микросферами, а на втором этапе можно применить на остаточной опухоли масляную химиоэмболизацию.
Препараты для химиоэмболизации печени
В настоящее время химиоэмболизацию печени микросферами проводят двумя препаратами: DC Bead и Hepaspheres.
Микросферы DC Bead, производящегосябританской компанией Biocompatibles, изготовлены из поливинилалкоголя. Они могут иметь диаметр от 100 до 900 микрон: каждый вариант размера соответствует диаметру сосуда, в котором нужно перекрыть кровоток. Доксорубицин – основной применяемый для ТАХЭ химиопрепарат – высвобождается из микросфер DC Bead в течение двух недель.
В Hepaspheres, выпускаемом американской Biosphere Medical, микросферы состоят из сополимера винилацетата и метилакрилата. Химиопрепарат тот же, что и в DC Bead, – доксорубицин. Hepaspheres выпускается с микросферами 30–60, 50–100, 100–150 или 150–200 микрон в диаметре. В воде размер микросфер увеличивается в 4 раза.
Медицинский директор, врач онколог-хирург, к.м.н
Как проводится химиоэмболизация печени
Как правило, химиоэмболизация проводится под общим наркозом, но также возможно и погружение пациента в состояние седации. С помощью специальных датчиков контролируются артериальное давление и сердечный ритм пациента.
Через небольшой надрез в верхней части бедра в бедренную артерию вводится катетер. Следя за продвижением с помощью рентгена, катетер подводят к печеночной артерии. Когда катетер достигает ее, через него вводится рентгеноконтрастный раствор, позволяющий оценить расположение сосудов. Когда кончик катетера оказывается непосредственно в ветви артерии, питающей опухоль, вводится эмболизирующий препарат вместе с химиопрепаратом.
После этого делаются рентгеновские снимки, чтобы удостовериться, что препарат введен правильно. Затем катетер извлекается, на место разреза накладывается повязка.
Длится ТАХЭ около 1–1,5 часов. Для снижения риска возникновения осложнений применяются
Эффективность химиоэмболизации печени
Для оценки результата проведенной химиоэмболизации через 4 недели после первой процедуры делается КТ или МРТ с контрастированием сосудов. Если в сосудах отсутствует контрастное вещество, это означает гибель опухолевых клеток. Через полтора – два месяца производится вторая процедура с контрольным обследованием.
Если контрастное вещество проходит в сосуды, осуществляется повторная процедура с контрольным обследованием уже через 4 недели, чтобы не растягивать интервал между второй и третьей процедурой.
Эффективность химиоэмболизации довольно высока: примерно в 2/3 случаев удается заметно сократить размеры опухоли или вовсе остановить ее рост. В зависимости от типа рака эффект цикла ТАХЭ сохраняется в течение 10–14 месяцев.
Если через полгода после цикла химиоэмболизации рост опухоли возобновляется, ТАХЭ можно повторить.
Согласно клиническому исследованию, проведенному в Барселоне с участием 27 пациентов, цикл химиоэмболизации печени продлил жизнь на год 92% людей, на два — 89%. Выживаемость в течение трех лет после цикла ТАХЭ, по результатам исследования 71 пациента в Афинах, — 76,4%. Для ряда пациентов ТАХЭ становится возможностью дождаться своей очереди на трансплантацию.
Осложнения после химиоэмболизации печени
Возможные осложнения после химиоэмболизации могут быть связаны либо с токсичностью химиопрепарата, либо с селективной сосудистой манипуляцией. В большинстве случаев побочные эффекты ограничиваются подташниванием, болевыми ощущениями в месте катетеризации сосуда, кратковременным ухудшением самочувствия. Хотя также возможны
Однако современные технологии и высокая квалификация врачей позволяют максимально снизить риски. Серьезные осложнения после ТАХЭ в настоящее время возникает только у 5% пациентов.
Последние новости
Последние статьи
Рейтинг: 4.0/5 Голоса: 1