Что такое тиреотоксикоз (гипертиреоз)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Курашова О. Н., эндокринолога со стажем в 27 лет.
Определение болезни. Причины заболевания
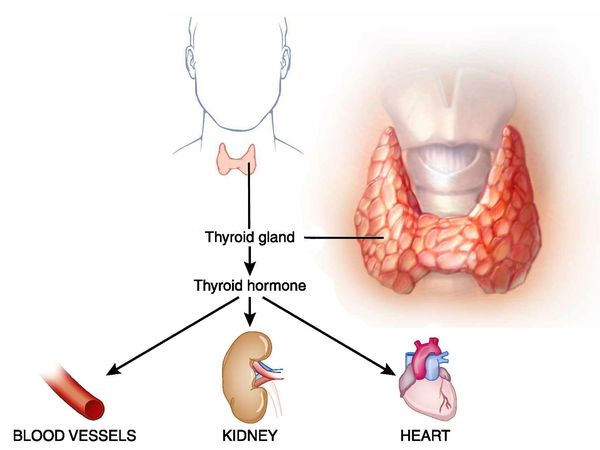
Тиреотоксикоз (гипертиреоз) — гиперметаболический процесс, вызванный избытком тиреоидных гормонов в организме и их токсическим воздействием на различные органы и ткани. Клинически характеризуется увеличением щитовидной железы и поражением других систем и органов. [3] [5] [11]
Первые описания этой патологии были найдены в работах персидского врача Джурджани, созданных в 1100 году. [5] [11]
Данный синдром встречается как у женщин (до 2%), так и у мужчин (до 0,2%). Чаще он возникает у людей в возрасте 20-45 лет.
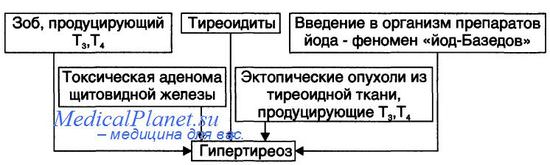
Причин возникновения тиреотоксикоза множество. К основным относятся:
Провоцирующим фактором синдрома является дополнительное количество йода, поступающее в организм при самостоятельном использовании йодных добавок.
Состояние тиреотоксикоза при диффузно-токсическом зобе является аутоиммунным заболеванием. Обычно оно развивается в результате избыточной выработки антител к рецептору тиреотропного гормона (ТТГ), производимого гипофизом.
Возникновение тиреотоксического состояния возможно при возникновении функциональной автономии уже существующего узла щитовидной железы — одно- и многоузлового зоба. Это заболевание развивается достаточно долго, в основном у людей, старше 45 лет. Так, в отсутствие воздействия ТТГ — основного физиологического стимулятора [7] [8] — узлы синтезируют количество тиреогормонов, превышающее потребность организма. [5] [6] [11]
Симптомы тиреотоксикоза (гипертиреоза)
При опросе пациентов с подозрением на повышенную функцию щитовидной железы выявляются:
Повышенное количество тиреогормонов влияет на сердечную деятельность
Что нельзя делать при тиреотоксикозе щитовидной железы
а) Общие. Нарушение толерантности к жаре, повышенное потоотделение, тремор, приливы, нарушения сна.
б) Психологические. Нервозность, эмоциональная лабильность, тревога, агрессивность, бред.
в) Сердечно-сосудистые. Сильные сердцебиения, тахикардия, суправентрикулярные нарушения ритма.
г) Дыхательные. Диспноэ, дисфония.
д) Желудочно-кишечные. Повышенный аппетит, потеря веса, усиленная перистальтика.
е) Репродуктивные. Гинекомастия, нерегулярные менструации.
ж) Кости. Остеопороз.
з) Другое. Офтальмопатия, дермопатия.
2. Каковы причины гипертиреоза?
Наиболее частой формой гипертиреоза является болезнь Грейвса (Graves) (90%), которая развивается вследствие выработки антител, стимулирующих рецепторы к тиротропину. У десяти процентов пациентов в группе среднего и пожилого возраста гипертиреоз развивается вследствие болезни Пламмера (Plummer) (токсического узлового зоба), которая характеризуется наличием узлов, функционирующих независимо от нормальной (но принципу обратной связи) регуляции.
К менее частым формам гипертиреоза относятся тиреоидит (подострый, «немой», послеродовый), в случае которого воспаление приводит к повышению высвобождения тироксина и трийодтиронина. Ятрогенный гииерпаратиреоз развивается вследствие избыточного введения тироксина или трийодтиронипа.
Реже причиной гипертиреоза становятся неонатальный гипертиреоз, тиреотропинома, экзогенный йод. Очень редко причиной гипертиреоза становятся рак щитовидной железы, хориокарципома, кистовидная опухоль, эмбриональная тестикулярная карцинома и опухоль яичника.
3. Как необходимо проводить обследование при гипертиреозе?
Для гипертиреоза характерно сочетание низких уровней тиротроиина и высоких уровней тироксина в сыворотке. Если уровень тироксина сыворотки в норме, то высокий уровень трийодтиронина указывает на интоксикацию трийодтиронином, а нормальный уровень трийодтиронипа исключает гипертиреоз.
Нормальный уровень тиротропина сыворотки почти всегда исключает гипертиреоз. Высокий уровень тиротропина в сочетании с повышением свободного тироксина указывает на тот редкий случай, когда у пациента развилась тиротронин-продуцирующая опухоль гипофиза.
Уровень общего тироксина сыворотки может повышаться одновременно с увеличением сывороточного тиреоид-связывающего глобулина. Это происходит во время беременности, при лечении эстрогенами и у пациентов с наследственным повышением уровня тиреоид-связывающего глобулина.
Для подтверждения токсического узлового зоба выполняют радионуклидное сканирование, которое демонстрирует накопление изотопа в одном узле железы или неоднородное накопление более чем в одном гинерфуикционирующем узле. Сцин-тиграфия позволяет обнаружить низкое поглощение радиоактивного йода или отсутствие его поглощения в случае тиреоидита.
4. Каковы три возможных способа лечения?
Антитиреоидные препараты, радиоактивный йод и оперативное лечение.
5. Какие препараты используются в лечении гипертиреоза? Каков их механизм действия?
Метимазол (активный метаболит карбимазола) и пропилтиоурацил являются основой терапии. Цель лечения — либо достигнуть в процессе лечения ремиссии болезни Грейвса, либо эутиреоидпого состояния перед лечением радиоактивным йодом или операцией. Оба препарата снижают органификацию йода и сцепление йодтиронинов.
Пропилтиоурацил также подавляет периферическую монодейодипацию тироксина (ТЦ в трийодтиронии (Т3). Оба препарата также уменьшают сывороточную концентрацию антител к рецепторам тиротропина и усиливают активность Т-супрессоров. Таким образом, они могут оказывать иммуносупрессивное действие. Лечение начинается с 20 мг/суг метимазола или со 100 мг нропилтиоурацила 3 раза в день.
Дозу можно уменьшить после 6 недель терапии, если у пациента отмечаются клиническое и биохимическое улучшение. Терапия обычно длится 2 года. Необходимо следить за возникновением у пациента побочных эффектов, таких как сыпь, зуд, агранулоцитоз, гепатит, холесгатическая желтуха и волчаночноподобный синдром. Антагонисты бета-адренорецепторов облегчают клинические проявления болезни. Они не должны использоваться в монотерапии, за исключением коротких периодов перед лечением радиоактивным йодом или операцией. Наиболее часто назначают Надолол (80 мг в день) и атенолол (100 мг/депь).
Йод, применяемый в виде раствора Люголя (водный раствор 5% йода и 10% йодида калия по 0,3 мл/день) или йодида калия (60 мг 3 раза в день), подавляет высвобождение тиреоидного гормона. Такую терапию используется короткими курсами для подготовки к операции, после лечения радиоактивным йодом для ускорения снижения уровня гормона и для лечения тиреотоксического криза.
6. Каковы исходы лекарственной терапии?
Длительная ремиссия гипертиреоза Грейвса в процессе антитиреоидной лекарственной терапии наступает у 50% пациентов. Рецидив наиболее часто развивается в течение первых 6 месяцев после прекращения лечения.
7. Каковы показания и цели лечения радиоактивным йодом?
Лечение радиоактивным йодом относится к терапии выбора рецидива, наступившего после лечения антитиреоидными препаратами. Целью терапии радиоактивным йодом является устранение гипертиреоза путем разрушения тиреоидной ткани; при этом должно сохраниться достаточное количество ткани, чтобы избежать гипотиреоза.
8. Каков режим терапии радиоактивным йодом?
Обычная доза радиоактивного йода равна 10 мКю. Если гипертиреоз не излечился, то необходимо повторить дозу через 6 месяцев. Предварительное лечение антитиреоидными препаратами позволяет добиться эутиреоидного состояния. Препараты необходимо отменить за 4 дня до терапии радиоактивным йодом и возобновить их прием через 4 дня после лечения. Стероиды останавливают прогрессирование офтальмопатии. Преднизолон используется в дозе 0,5 мг/кг веса с третьего дня после лечения радиоактивным йодом в течение месяца. Дозу снижают на протяжении 2 месяцев.
Беременность относится к абсолютным противопоказаниям. Женщинам детородного возраста необходимо провести тест на беременность перед началом лечения и избегать беременности в течение 6 месяцев после лечения. Радиоактивный йод может обострять офтальмопатию.
9. Каковы исходы лечения радиоактивным йодом?
До наступления эутиреоза проходят месяцы. После того как эутиреоз достигнут, возврат к гипертиреозу происходит редко. Гипотиреоз, единственный серьезный побочный эффект, зависит от дозы. Он развивается со скоростью 3% в год, поражая 50% пациентов через 10 лет и почти 100% через 25 лет.
10. Кому показана тиреоидэктомия по поводу гипертиреоза?
а) Беременным пациенткам, которых трудно лечить медикаментозно.
б) Пациентам с большим зобом и низким захватом радиоактивного йода.
в) Детям.
г) Пациентам, не соблюдающим назначенную терапию.
д) Пациентам с узлами, подозрительно похожими па рак.
е) Пациентам со сдавлением трахеи или пищевода.
ж) Пациентам, озабоченным косметическими дефектами.
з) Пациентам с офтальмопатией.
11. Как нужно готовить больного к операции?
Любого пациента с гипертиреозом до операции необходимо привести в эутиреоидное состояние. Больного можно лечить с помощью антитиреоидных препаратов и йодида калия. Антагонисты бета-адренорецепторов также можно использовать отдельно или в комбинации с вышеупомянутыми режимами.
12. Каков объем вмешательства при тиреоидэктомии?
К двум типам операций при болезни Грейвса относятся субтотальная тиреоидэктомия или практически тотальная тиреоидэктомия. Целями субтотальной тиреоидэктомии являются: сохранить 4-8 г хорошо кровоснабжаемой ткани железы и избежать гипотиреоза. Однако из-за небольшого риска рецидива (10%) некоторые хирурги выполняют практически тотальную тиреоидэктомию. При болезни Пламмера в случае одностороннего поражения добиться эутиреоидного состояния позволяет лобэктомия или частичная тиреоидэктомия, а при множественных поражениях — контралатеральная субтотальная тиреоидэктомия.
13. Как часто после операции развивается гипотиреоз?
У всех пациентов, перенесших практически тотальную тиреоидэктомию, развивается гипотиреоз, и они нуждаются в заместительной терапии тироксином. Гипотиреоз развивается у 50% пациентов, подвергшихся субтотальной тиреоидэктомии.
14. Какое лечение необходимо при токсическом узловом зобе?
Гипертиреоз вследствие токсического узлового зоба характеризуется постоянным течением без спонтанной ремиссии; антитиреоидные препараты не подходят для длительной терапии. Наиболее часто используется радиоактивный йод. Большие дозы (50 мКи) сводят к минимуму риск рецидива гипертиреоза у пациентов старшей возрастной группы со значительными сердечно-сосудистыми симптомами гипертиреоза.
Видео методики оценки щитовидной железы пальпацией
15. Какое лечение необходимо в случае гипертиреоза вследствие тиреоидита?
Подострый тиреоидит следует подозревать, если пациент жалуется на боль и повышенную чувствительность при пальпации в области щитовидной железы. Гипертиреоз обычно умеренный и длится короткий период времени (недели). Пациентов лечат антагонистами бета-адренорецепторов и салицилатами или глюкокортикоидами. Может развиться гипотиреоз, но он обычно проходит.
16. Какое лечение необходимо при тиреотоксическом кризе?
Тиреотоксический криз необходимо лечить в условиях отделения интенсивной терапии. Основные мероприятия включают восполнение жидкости, антипиретические средства (ацетаминофен) и диету. К специфическим мероприятиям относятся подавление пропилтиоурацилом синтеза Т4 и конверсии Т4 в Т3. Пропилтиоурацил назначают в дозе 100 мг перорально, через назогастральный зонд или ректально каждые 6 часов.
Йодиды подавляют высвобождение Т4 (насыщенный раствор йодида калия, 5 капель перорально или через пазогастральный зонд каждые 6 часов). Стероиды (дексаметазоп 2 мг каждые 6 часов) также подавляют высвобождение Т4 и превращение его в Т3. Антагонисты бета-адренореценторов (пропранолол или эсмолол) позволяют контролировать сердечно-сосудистую деятельность. Последним средством выбора является выведение тиреоидных гормонов с помощью плазмафереза, переливания крови или диализа.
17. Кто выполнил первую тиреоидэктомию?
Иоганн фон Микулич-Радески (Johann von Mikulicz-Radecki) произвел первую тиреоидэктомию в 1885 г.
18. Какой хирург был удостоен Нобелевской премии за работу, посвященную болезням щитовидной железы?
Теодор Кохер (Teodor Kocher) был удостоен Нобелевской премии в области медицины в 1909 г. Он достиг успеха в снижении высокого уровня смертности при тиреоидэктомии до менее чем 1%. Наиболее значительным достижением его было описание послеоперационного гипотиреоза как cachexia strumipriva.
Учебное видео гормоны щитовидной железы в норме и при болезни
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Тиреотоксикоз (гипертиреоз): причины, симптомы, диагностика, лечение
Тиреотоксикоз – патологическое состояние, вызванное избытком гормонов щитовидной железы. Другое название этого заболевания – гипертиреоз. Состояние противоположно гипотиреозу, при котором наблюдается дефицит тиреоидных гормонов.
Причины тиреотоксикоза
Симптомы гипертиреоза
Самое главное в организме на всех уровнях – баланс. На примере с работой щитовидной железы это видно особенно отчетливо: как недостаток гормонов, так и их дефицит разрушителен для организма.
Группы риска
С заболеванием сталкивается 1-2 человека из тысячи. Женщины заболевают тиреотоксикозом чаще (7-10% против 2-3% у мужчин), с возрастом частота этого состояния может достигать 21%.
В первую очередь в группе риска женщины старше 30 лет.
Другая категория – лица, употребляющие в пищу слишком много йода. Это касается в первую очередь йодсодержащих добавок и лекарственных препаратов.
В группе риска также люди, у близких родственников которых диагностированы заболевания эндокринной системы.
Диагностика тиреотоксикоза
Пациенту, который подозревает у себя нарушения щитовидной железы, необходимо обратиться к терапевту. Врач проведет первичный осмотр и оценит вероятность того, что состояние и симптомы действительно связаны с эндокринной системой, назначит обследование. По результатам обследования будет понятно, есть ли необходимость в лечении. Если такая необходимость возникнет, может потребоваться консультация эндокринолога.
Возможен и другой путь: пациент может сразу обратиться к эндокринологу. Это не возбраняется, но самостоятельная диагностика редко бывает эффективной. Симптомы, которые характерны для заболеваний щитовидной железы, могут быть и при заболеваниях других органов. Возможно, приоритет может быть смещен в сторону обследования сердечно-сосудистой системы или других органов – в зависимости от конкретной ситуации.
Профилактическую диагностику щитовидной железы рекомендуется проходить раз в 2-3 года, если человек здоров: если не было ранее проблем с этим органом и если ни у кого из близких родственников нет эндокринных нарушений. В ином случае нужно проверять щитовидку раз в год или чаще, по указанию врача.
Проверить функцию щитовидной железы также нужно женщинам, планирующим беременность.
Результаты исследований оцениваются вместе с общим анамнезом. Врач уточнит наличие эндокринных заболеваний у близких родственников, было ли облучение головы или шеи, спросит, в каком регионе проживает пациент и какой диеты он придерживается.
По результатам анализов и общего осмотра могут быть назначены дополнительные обследования.
Лечение гипертиреоза
Осложнения тиреотоксикоза
Длительное заболевание негативно сказывается на состоянии костей: снижается их плотность, увеличивается риск переломов. Особенно опасно для женщин в периоде менопаузы, когда кости ослабевают из-за гормональной перестройки, а гипертиреоз только усугубляет ситуацию.
Также возможны сердечно-сосудистые нарушения с риском тромбоэмболических осложнений. Без своевременной диагностики и лечения заболевания щитовидной железы разрушают весь организм.
Лечение тиреотоксикоза
Тиреотоксикоз обусловлен избыточной секрецией тиреоидных гормонов щитовидной железой и встречается при многих клинических состояниях. Причинами развития тиреотоксикоза могут быть: диффузный токсический зоб (ДТЗ, болезнь Грейвса, болезнь Базедова); аутоим
Тиреотоксикоз обусловлен избыточной секрецией тиреоидных гормонов щитовидной железой и встречается при многих клинических состояниях. Причинами развития тиреотоксикоза могут быть: диффузный токсический зоб (ДТЗ, болезнь Грейвса, болезнь Базедова); аутоиммунный тиреоидит в фазе тиреотоксикоза; функциональная автономия (токсическая аденома, многоузловой токсический зоб); йод-индуцированный тиреотоксикоз; резистентность к тиреоидным гормонам; ТТГ-продуцирующая аденома; гестационный транзиторный тиреотоксикоз; метастазы рака, продуцирующие тиреоидные гормоны; Struma ovarii; ятрогенный тиреотоксикоз; тиреотоксическая стадия подострого тиреоидита (де Кервена).
При наличии у пациента клинических симптомов тиреотоксикоза, прежде чем приступать к лечению, очень важно точно установить причину его развития, поскольку от этого будет зависеть адекватность выбранного метода терапии.
Гормональными маркерами гиперфункции, равно как и других заболеваний щитовидной железы, являются тиреотропный гормон (ТТГ) и свободный тироксин (св.Т4). В тех случаях когда при исследовании ТТГ оказывается сниженным, а св. Т4 в пределах нормы, проводится определение свободного трийодтиронина (св.Т3) с целью диагностики Т3-тиреотоксикоза (рис.1). На следующем этапе диагностики необходимо установить причину тиреотоксикоза. В медицинской практике нам наиболее часто приходится наблюдать пациентов с аутоиммунными заболеваниями щитовидной железы — ДТЗ и аутоиммунный тиреоидит. ДТЗ обусловлен выработкой тиреостимулирующих иммуноглобулинов (ТСИ), которые связываются с рецептором ТТГ на мембранах тиреоцитов и через активацию циклического аденозинмонофосфата постоянно стимулируют повышенную секрецию тиреоидных гормонов. Исследование антител к рецептору ТТГ (АТ-рТТГ) не только позволяет подтвердить диагноз ДТЗ, но и дифференцировать его с аутоиммунным тиреоидитом (АИТ).
Показания для определения АТ-рТТГ в клинической практике
В практике врача уже стало традиционным определение антител к тиреоглобулину (АТ-ТГ) и к тиреопероксидазе (АТ-ТПО). Выявление этих антител позволяет легко решить проблему диагностики либо в пользу АИТ, либо — ДТЗ. На этот факт следует обратить особое внимание, поскольку АТ-ТГ и АТ-ТПО могут обнаруживаться в достаточно большом количестве как у больных АИТ, так и у пациентов с ДТЗ. Более того, по данным исследований, эти антитела могут выявляться у части здоровых людей и у пациентов с заболеваниями щитовидной железы неаутоиммунного генеза. И наконец, не во всех случаях при АИТ и ДТЗ антитела можно обнаружить. Следовательно, проводить диагностику на основании только одного признака и тем более решать вопрос о целесообразности назначения лечения не представляется возможным. В диагностике АИТ помимо определения АТ-ТПО большое значение имеет ультразвуковое исследование щитовидной железы (УЗИ).
Неравномерное диффузное снижение эхогенности ткани служит надежным признаком АИТ, но тем не менее не позволяет дифференцировать его с ДТЗ, для которого характерным являются те же изменения по УЗИ. Таким образом, диагноз АИТ должен основываться на комплексе клинических и лабораторно-диагностических признаков. УЗИ щитовидной железы позволяет определить объем ткани, наличие узлового образования, что очень важно, поскольку у части пациентов эти показатели могут повлиять на выбор стратегии лечения.
Сцинтиграфия щитовидной железы у больных тиреотоксикозом проводится при подозрении на наличие функциональной автономии (токсическая аденома, многоузловой токсический зоб), загрудинный зоб, нефункциональные участки более 1–1,5 см.
Лечение ДТЗ (болезни Грейвса)
В настоящее время существуют три метода лечения ДТЗ: консервативный; радиоактивным йодом ( 131 I); хирургический.
Каждый из этих методов имеет свои показания, а также противопоказания и должен назначаться каждому пациенту индивидуально.
1. Консервативное лечение
Консервативную терапию назначают больным с небольшим диффузным увеличением щитовидной железы (по объему — 35–40 мл) без симптомов сдавления.
У пациентов с большим объемом щитовидной железы и/или узловыми образованиями по размерам более 1,0-1,5 см, а также с тяжелыми осложнениями тиреотоксикоза консервативную терапию используют в качестве медикаментозной подготовки к хирургическому лечению. При планировании радиойодтерапии пациентам также предварительно назначают консервативное лечение.
На фоне тиреостатической терапии эутиреоидное состояние наступает уже через 3–5 нед от начала лечения. В течение последующих 12–24 мес поддерживающей эутиреоз терапии примерно у 20–40% пациентов развивается ремиссия заболевания.
К сожалению, у части пациентов примерно через год вновь «расцветает» клиника тиреотоксикоза. Таким больным нецелесообразно назначать повторные длительные курсы консервативной терапии. Вероятнее всего, ТСИ продолжают вырабатываться в большом количестве и стимулировать щитовидную железу к избыточной продукции тиреоидных гормонов. В подобных случаях проводят курс медикаментозной подготовки, а затем, в зависимости от размеров и морфологических изменений ткани щитовидной железы, назначают либо терапию 131 I, либо оперативное лечение. Прогноз ремиссии или возможного рецидива тиреотоксикоза после проведения курса тиреостатической терапии можно определить по уровню АТ-рТТГ. Исследование антител проводится перед полной отменой препаратов. Риск рецидива тиреотоксикоза у пациентов возрастает при повышенном уровне АТ-рТТГ, чаще рецидивы наблюдаются в течение первого года после окончания лечения.
Для лечения ДТЗ на протяжении многих лет используются препараты из группы тионамидов: тиамазол (тирозол, мерказолил, тиамазол-филофарм, метизол, метимазол) и пропилтиоурацил (пропицил). C появлением дозировки тирозола 10 мг количество принимаемых таблеток можно уменьшить в 2 раза, что создает дополнительное удобство для пациентов. Механизм тиреостатического действия заключается в подавлении синтеза тиреоидных гормонов на стадиях органификации и комплексирования. Пропилтиоурацил частично подавляет превращение Т4 в Т3 за счет ингибирования 5’-монодейодиназы. Лечение тиреостатическими препаратами начинают с относительно высоких доз: 30–40 мг тиамазола или его аналогов 2–3 приема в день в течение дня или 300 мг пропилтиоурацила — 3–4 приема в день. После достижения эутиреоза дозу постепенно снижают до поддерживающей: тиамазол до 5–10 мг в день, пропилтиоурацил до 50–100 мг 1–2 приема в день (рис). Достижение эутиреоидного состояния оценивается по исчезновению клинических симптомов тиреотоксикоза и уровню св. Т4. Определять уровень ТТГ нецелесообразно, поскольку на протяжении нескольких месяцев он может оставаться подавленным. Дополнительно в лечении ДТЗ используют β-адреноблокаторы, которые подавляют тканевое превращение Т4 в Т3. Пропранолол назначают по 60–120 мг/сут 3–4 приема в день, атенолол — 50–100 мг/сут, конкор — 5–10 мг/сут однократно. В клинической практике существует два варианта назначения тиреостатических препаратов: в виде монотерапии или в комбинации с левотироксином (эутирокс, L-тироксин, тиро-4). В последнем варианте пациенту по достижению эутиреоидного состояния (оценивается по уровню Т4) подключают левотироксин в дозе 25–50 мкг. Исследования показывают, что на фоне комбинированной поддерживающей терапии в течение 18–24 мес достигается более стойкая блокада секреции тиреоидных гормонов.
При лечении тиреостатическими препаратами у пациентов могут развиться побочные эффекты в виде аллергических реакций (зуд, крапивница и др.). Одним из наиболее серьезных осложнений является агранулоцитарная реакция. Поэтому пациентам рекомендуется проводить общий анализ крови в первые 7–10 дней после начала лечения, а в дальнейшем — 1 раз в мес. К другим крайне редким тяжелым побочным эффектам относится тромбоцитопения, острый некроз печени.
2. Терапия радиоактивным йодом
Во многих странах мира радиойодтерапия — наиболее часто рекомендуемый метод лечения как ДТЗ, так и других форм токсического зоба, в частности функциональной автономии. Необходимо отметить, что 131 I назначают больным в любом возрасте (дети, пациенты молодого, среднего и пожилого возраста). Единственным противопоказанием для радиойодтерапии является беременность и грудное вскармливание. Спорным остается вопрос о лечении 131 I пациентов ДТЗ в сочетании с эндокринной офтальмопатией. Согласно результатам рандомизированного исследования, у части больных ДТЗ терапия 131 I способствовала прогрессированию эндокринной офтальмопатии. У пациентов, получающих радиойодтерапию, ремиссия тиреотоксикоза наступает в 90–95% случаев. Рецидив заболевания возможен у 3–5% больных, что требует проведения повторного курса радиойодтерапии. Радиоактивный йод принимают перорально в виде натриевой соли 131 I в растворе или капсулах: 131 I быстро поступает в щитовидную железу, вызывая деструкцию тиреоцитов посредством β-излучения. Чаще всего возникает вопрос о выборе больших или малых доз радиойода. Как известно, большие дозы неминуемо приводят к развитию гипотиреоза, использование же малых доз сопряжено с возможностью сохранения клиники тиреотоксикоза. Многолетние исследования за пациентами показали, что однократная доза радиоактивного йода, рассчитанная на полное разрушение щитовидной железы, излечивает тиреотоксикоз у 90% больных. Применение малых доз сохраняет эутиреоидное состояние в течение 10 лет после радиойодтерапии лишь у 25–30% больных. К сожалению, из-за дефицита 131 I нам довольно редко приходится пользоваться этим методом в лечении больных с тиреотоксикозом.
3. Хирургическое лечение
Показаниями для оперативного лечения больных с тиреотоксикозом служат большие размеры зоба, непереносимость тиреостатиков, рецидив тиреотоксикоза после проведенной консервативной терапии, загрудинно расположенный зоб. При наличии показаний возможно хирургическое лечение в I и II триместрах беременности, которое заключается в проведении субтотальной резекции щитовидной железы с оставлением минимального количества (объема) ткани. Однако нередко возникает проблема с определением этого минимального объема ткани. Если оставить меньше 4 г тиреоидной ткани, то неминуемо разовьется гипотиреоз, и тогда возникает необходимость в назначении заместительной терапии левотироксином. В тех случаях когда ткани оставляют больше 4–6 г, довольно часто после операции сохраняются клинические симптомы тиреотоксикоза, возможно, не столь выраженные. Это состояние иногда называют «ложный рецидив». Большой объем оставшейся после операции тиреоидной ткани создает условия для продолжения избыточной секреции тиреоидных гормонов под стимулирующим влиянием ТСИ. Подобная хирургическая тактика, с одной стороны, повышает риск развития осложнений, в частности мерцательной аритмии, а с другой — нередко заканчивается повторной операцией. Согласно вышеизложенному, если пациенту показано оперативное лечение, то целесообразно проводить максимально субтотальную резекцию щитовидной железы, оставляя не более 3 мл ткани. Безусловно, это требует высокой квалификации хирурга, поскольку, как известно, оперативное лечение сопряжено с развитием ряда осложнений, таких как парез возвратного нерва, удаление паращитовидных желез. Операцию следует проводить на фоне эутиреоидного состояния, достигнутого с помощью тиреостатической терапии. При непереносимости тиреостатиков используют β-адреноблокаторы или йод (насыщенный раствор калия йодида или раствор Люголя — 8–10 капель в день в течение 10–12 дней до операции).
Лечение аутоиммунного тиреоидита в фазе тиреотоксикоза
Довольно часто АИТ верифицируется как ДТЗ, поскольку клинические симптомы идентичны, а АТ-ТГ и АТ-ТПО выявляются почти с одинаковой частотой при одном и другом заболевании. Определение АТ-рТТГ в настоящее время пока еще доступно не во всех городах России. Лечение тиреотоксической стадии АИТ проводится чаще консервативно (при отсутствии аргументированных показаний в пользу оперативного вмешательства), при этом в терапии используют β-адреноблокаторы или же их комбинацию с тиреостатическими препаратами. Следует заметить, что тиреотоксикоз на фоне АИТ имеет некоторые особенности: быстрый эффект при приеме тиреостатических препаратов с развитием медикаментозного гипотиреоза; в ряде случаев волнообразное течение заболевания со сменой состояний тиреотоксикоза и эутиреоза.
Лечение функциональной автономии (токсическая аденома, узловой и многоузловой токсический зоб)
Пациентам с тиреотоксической формой функциональной автономии назначают тиреостатические препараты (тирозол, мерказолил, тиамазол-филофарм, метизол, метимазол, пропицил) с целью подготовки к оперативному лечению. В нашей стране из-за дефицита лечебного 131 I больных с функциональной автономией оперируют, хотя во многих странах мира основным методом лечения этих состояний является радиойодтерапия. Автономные участки тиреоидной ткани хорошо захватывают радиойод, который разрушает только эти участки ткани щитовидной железы. Большинство пациентов в дальнейшем переходят в эутиреоидное состояние. Радиойодтерапия предпочтительна особенно у больных пожилого возраста. К операции прибегают при большом объеме автономной ткани щитовидной железы (более 3 см в диаметре).
ТТГ-индуцированный тиреотоксикоз (резистентность к тиреоидным гормонам и ТТГ-продуцирующая аденома гипофиза)
Синдром генерализованной резистентности встречается довольно редко (в литературе описаны около 600 случаев). В связи с тем что у человека чувствительность органов и тканей к тиреоидным гормонам неодинакова, у одного и того же пациента могут развиваться как эутиреоидное, гипотиреоидное, так и гипертиреоидное состояния. Резистентность периферических тканей способствует компенсаторному повышению секреции тиреоидных гормонов, сохраняя, таким образом, эутиреоидное состояние. Если гипофиз оказывается более резистентным по сравнению с периферическими тканями, то развиваются клинические симптомы тиреотоксикоза, которые очень трудно поддаются медикаментозному лечению. Исследования показали, что лечебным эффектом обладает 3,5,3’-трийодтироуксусная кислота. Особенностью этого синдрома является отсутствие подавления ТТГ даже при использовании сверхбольших доз L-Т4, поэтому снижение ТТГ с помощью тиреоидных гормонов абсолютно неэффективно. При обнаружении ТТГ-продуцирующей аденомы гипофиза показано оперативное лечение.
Подострый тиреоидит (де Кервена) развивается спустя некоторое время (4–6 нед) после перенесенной вирусной инфекции. В течении подострого тиреоидита различают тиреотоксическую стадию, которая сменяется гипотиреоидной стадией, а затем в большинстве случаев тиреоидная функция полностью восстанавливается. Назначение β-адреноблокаторов (пропранолол, атенолол, бетаметазон) снимает симптомы тиреотоксикоза, применение препаратов из группы тионамидов не требуется. Пациентам рекомендуется лечение глюкокортикоидами. Преднизолон назначают по 30–40 мг ежедневно в течение 2–3 нед с последующим постепенным снижением дозы на 5 мг в нед. Возможен и другой вариант назначения глюкокортикоидов — 30–40 мг ежедневно в течение 10–12 дней с последующим переводом на прием через день в этой же дозе на протяжении 6–8 нед. Прогноз заболевания, как правило, благоприятный.
Нередко в кардиологической практике пациентам с нарушениями ритма назначают ритмиодарон, амиодарон, кордарон, седакорон. Следует отметить, что эти лекарственные средства способны изменять уровень тиреоидных гормонов у исходно эутиреоидных пациентов. Более чем у 50% больных, принимающих постоянно амиодарон, повышен уровень Т4 (в среднем на 44% по сравнению с базальным уровнем за счет нарушения превращения Т4 в Т3). Следовательно, изолированное повышение Т4 при терапии амиодароном нельзя интерпретировать как диагностический признак тиреотоксикоза. Тем не менее примерно у 5–20% пациентов эти препараты вызывают гипертиреоз, который обычно сопровождается дальнейшим повышением уровня Т4 на фоне значительного снижения уровня ТТГ с развитием симптомов тиреотоксикоза. Наиболее информативный контроль функции щитовидной железы при длительной терапии амиодароном или кордароном оказывается при условии определения ТТГ. Пациентам с «амиодароновым» тиреотоксикозом к терапии подключают β-адреноблокаторы.
Тиреотоксикоз при беременности повышает риск выкидыша, преждевременных родов и рождения плода с малой массой тела. У женщины при этом чаще развивается токсикоз, а в ряде случаев сердечная недостаточность. Одной из наиболее распространенных причин тиреотоксикоза у беременных женщин является ДТЗ. Оптимальным вариантом при его развитии на фоне беременности является ее прерывание. Однако если женщина настаивает на сохранении беременности, то обычно назначают пропилтиоурацил в дозе 25–50 мг в два приема, поскольку при приеме мерказолила у плода иногда наблюдается дефект кожи на голове. Кроме того, пропилтиоурацил имеет более короткий период полужизни и вызывает меньше осложнений по сравнению с тионамидами. В случае использования тионамидов следует назначать минимально эффективные дозы (5–10 мг тирозола в сут) с ежемесячным контролем свободных фракций тиреоидных гормонов. Большие дозы препаратов могут привести к развитию зоба и гипотиреоза у плода. Слабое стимулирующее действие на щитовидную железу оказывает хорионический гонадотропин (ХГ), концентрация в крови которого на ранних сроках беременности возрастает.
У незначительного числа беременных женщин именно ХГ способствует развитию транзиторного тиреотоксикоза. Это состояние не требует лечения. Относительно тяжелый тиреотоксикоз может наблюдаться при пузырном заносе или хориокарциноме.
В этих случаях пузырный занос удаляют или принимают меры, направленные на хориокарциному.
Послеродовый тиреоидит развивается спустя 1–3 мес после родов. Симптомы тиреотоксикоза носят транзиторный характер, сменяясь в дальнейшем гипотиреозом со спонтанной ремиссией через 6–8 мес. Транзиторная стадия тиреотоксикоза не требует лечения, а в гипотиреоидной стадии назначают левотироксин в дозе, которая способствует нормализации ТТГ.
Л. В. Кондратьева, кандидат медицинских наук, доцент
РМАПО, Москва