Илеональный анастомоз. Анастомоз кишечника как метод лечения язвенного колита.
1. Что такое илеональный анастомоз?
2. Как проводится операция?
Иногда анастомоз кишечника проводится в два этапа. Вначале врач удаляет толстую кишку, делает отверстие в брюшной полости и присоединяет подвздошную кишку к отверстию. Через это отверстие переработанная пища выводится из организма в специальные мешки. Процесс называется илеостомией. На втором этапе анастомоза кишечника из подвздошной кишки формируют мешок (резервуар) и прикрепляют к анальному отверстию. Восстановление после каждой операции занимает от 1 до 2 недель. Две стадии можно объединить в одну операцию, если врач считает это допустимым.
Илеональный анастомоз при лечении неспецифического язвенного колита, как правило, дает хорошие результаты. 8 из 10 человек не имеют проблем после проведения процедуры. Большинство пациентов отмечают улучшение качества жизни после операции.
3. Когда операцию не проводят?
Операцию илеонального анастомоза не проводят пациентам, у которых мышцы прямой кишки не работают должным образом, а также людям с диагностированным раком прямой кишки.
4. Риски при анастомозе кишечника
Как и любая операция, илеональный анастомоз сопряжен с некоторыми рисками. У 25-30 человек из 100 после операции могут наблюдаться следующие осложнения:
У 10 из 100 пациентов могут возникнуть сексуальные проблемы. У женщин, перенесших эту операцию, меньше шансов забеременеть (риск бесплодия).
В большинстве случаев анастомоз кишечника проводят пациентам, которые склонны к развитию рака, и их заболевание не поддается лечению медикаментозными средствами.
Заболевания 
Область применения 
Диагностика 
Наши цены 
Мы стараемся оперативно обновлять данные по ценам, но, во избежание недоразумений, просьба уточнять цены в клинике.
Данный прайс-лист не является офертой. Медицинские услуги предоставляются на основании договора.
Удаление опухоли прямой кишки
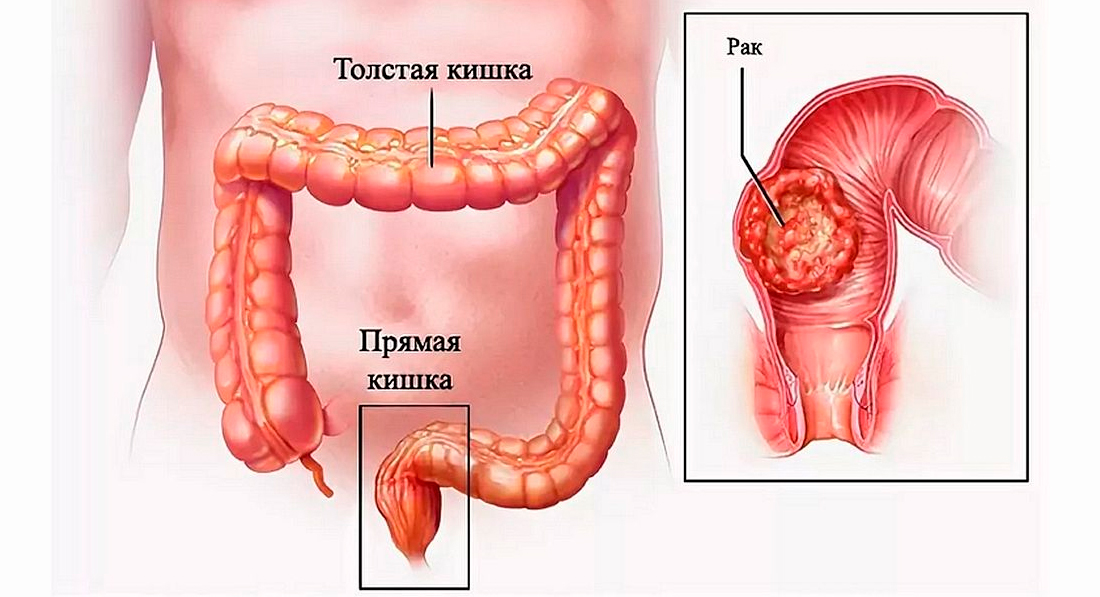
В прямой кишке чаще, чем в других отделах желудочно-кишечного тракта, образуются опухоли, на их долю приходится около 30-40% от всех опухолей Толстой кишки. Появляющиеся в дистальном отделе Толстой кишки, разные по структуре, скорости роста, сопровождающиеся различными симптомами, они могут быть доброкачественными или злокачественными. Полипы, аденомы, единичные или множественные — любая из этих опухолей, независимо от свойств, подлежит удалению.
Почему опухоли прямой кишки нужно удалять
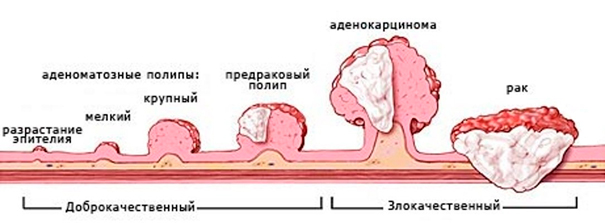
Если речь идет о полипах, то следует учитывать, что они относятся к облигатным предраковым состояниям, вероятность злокачественного перерождения составляет 3-20%, но риск трансформации возрастает с увеличением полипа. При длительном существовании полипа большого размера вероятность озлокачествления составляет 40-85%.
Что касается аденом, то прямой зависимости между размером аденомы и частотой развития рака нет. Однако риск малигнизации резко возрастает при длительном их существовании. Кроме озлокачествления, опухоли доброкачественного характера могут вызывать различные осложнения: кровотечения, нарушение проходимости каловых масс, флегмоны и др.
Раковая опухоль при отсутствии качественного лечения может стать причиной различных осложнений. Симптомы, постепенно нарастающие, как правило, ухудшают качество жизни пациента. Злокачественные образования могут стать причиной таких осложнений, как обтурационная кишечная непроходимость, абсцесс, флегмона, перитонит. Распространение раковых клеток по всему организму при отсутствии лечения ухудшает прогноз, сокращая продолжительность жизни пациента.
Виды операций при опухолях прямой кишки
Удаление доброкачественной опухоли прямой кишки небольшого размера или с выраженной ножкой может быть проведено при колоноскопии или ректороманоскопии с использованием электроэксцизии или электрокоагуляции.
При удалении крупных, на широком основании или стелющегося вида опухолей использование эндоскопического оборудования сопряжено с риском осложнений: перфорации, кровотечения, несостоятельности швов в дальнейшем и др. К тому же необходимость постоянной инсуффляции (подачи) газа в кишку при эндоскопическом удалении опухоли прямой кишки может стать причиной некачественной экспозиции, что приведет к дефекту кишечной стенки. Многие специалисты в таком случае прибегают к лапаротомии, в ходе которой опухоль иссекается. Я их иссекаю лапароскопически через несколько проколов под контролем колоноскопии ( гибридная операция)
При наличии множественных доброкачественных опухолей, при имеющихся полипах с высоким риском озлокачествления, а также при развитии осложнений (например, при некрозе или непроходимости кишечника) возможно проведение резекции части кишки. При полипозе наследственного происхождения рекомендована субтотальная колэктомия, в этом случае для беспрепятственного пассажа кишечного содержимого формируется колостома.
Для удаления злокачественной опухоли прямой кишки существуют различные методики: резекция, трансанальное иссечение опухоли, при запущенной стадии — эвисцерация таза. При выборе тактики хирургического удаления опухолей прямой кишки важно учитывать: локализацию опухоли, ее размеры, степень прорастания кишечной стенки, распространение на регионарные лимфатические узлы, рост опухоли (экзофитная, эндофитная форма), наличие метастазирования в другие органы.
При удалении злокачественного образования операция состоит из нескольких этапов:
Задать вопросы и записаться на консультацию можно
по телефону: 222-10-87
или заполните форму ниже
Спасибо, ваш вопрос успешно отправлен, скоро мы с вами свяжемся!
Мой подход к лечению опухолей прямой кишки
Если это возможно, я всегда отдаю предпочтение сфинктеросохраняющей операции. Для сохранения анального жома в ходе хирургического вмешательства используются разные виды операций. При наличии опухолей доброкачественного характера или на начальной стадии рака прямой кишки для удаления опухоли я использую разработанную мною технику — трансанальную эндоскопическую операцию с использованием специального запатентованного устройства — эспандера, и эндоскопических сшивающих аппаратов (США).
По разработанной мною методике при отсутствии распространения процесса на всю кишечную стенку я провожу резекцию части кишки вместе с опухолью в пределах подслизистого слоя, после чего дефект закрывается с помощью ручного эндоскопического шва. При глубокой инвазии я провожу клиновидное иссечение патологического участка с прошиванием кишечной стенки по всей толщине с использованием эндоскопического сшивающего аппарата ENDO-GIA-30 (США). Часть кишки при этом прошивается и отсекается. При этом способе удаление опухоли, локализованной на расстоянии не более 8 см от ануса, проводится быстро и надежно.
Преимущества авторской методики
Удаление злокачественной опухоли прямой кишки — основные моменты
В зависимости от локализации опухоли может быть использована методика передней резекции, брюшно-анальной резекции с низведением левых отделов ободочной кишки и т.д. Локализация опухоли выше 7 см от ануса является показанием к сфинктеросохраняющей операции. При расположении злокачественного образования в нижнеампулярном отделе прямой кишки рекомендована экстирпация.
При лечении больных со злокачественными опухолями прямой кишки я использую технику тотальной мезоректальной эксцизии — ТМЭ. В основе технологии — выделение прямой кишки в бессосудистой зоне, между собственной фасцией и париетальной фасцией таза. В клетчатке, расположенной в собственной фасции — мезоректуме, находятся лимфоузлы, которые при раке поражены метастазами. Благодаря использованию техники ТМЭ выживаемость пациентов увеличилась до 80%, а частота рецидива сократилась в 5-7 раз и не превышает 3-5% (в отличие от традиционного способа, используемого большинством хирургов, когда рецидив возникает в 25%).
При проведении операций по удалению опухоли в прямой кишке мои усилия направлены на сохранение непрерывности кишечной трубки. Если это возможно, я формирую колоректальный анастомоз, соединяющий концы кишки после резекции. При проведении третьего — восстановительного этапа, во время которого формируется межкишечное соустье, я активно использую современные сшивающие аппараты, что минимизирует количество таких послеоперационных осложнений, как несостоятельность швов анастомоза и стриктура кишки. Кроме того, использование сшивающих аппаратов позволяет проводить предельно низкую резекцию кишки, такой подход позволяет 80-85% пациентов сохранить функцию сфинктера. Если вследствие обширной зоны поражения сделать это невозможно, кишечная стома выводится на брюшную стенку. В таком случае восстановительная операция может быть проведена через несколько месяцев.
В зоне операции расположены многочисленные нервные и сосудистые волокна, повреждение которых приведет к развитию урогенитальных осложнений. Для их предупреждения я использую различные приемы, например, так называемую нервосохраняющую технику (nerve-sparing technique — NST). Также повышает безопасность операции использование современного эндоскопического оборудования.
Стоимость операции по удалению опухоли прямой кишки складывается из ряда факторов. Учитывается, прежде всего, объем хирургического вмешательства, имеющиеся на момент операции осложнения, требующие более длительного и масштабного лечения и т.п. Поэтому обращение к врачу, не дожидаясь развития осложнений — возможность сохранить здоровье и избежать затратного лечения.
При выборе клиники следует обратить внимание на оснащенность современным оборудованием и используемые методики. Проведение операций по современным технологиям, с использованием инновационного оборудования — это непродолжительный период госпитализации и быстрое восстановление. В нашей клинике пациенты проводят около трех дней, в большинстве случаев восстановление занимает около 2-3 недель. Но самое главное, что после малотравматичных операций на кишечнике, проводимых по современным технологиям опытными специалистами, пациенты в большинстве случаев имеют возможность вернуться к качественному уровню жизни.
На протяжении более чем 25 лет я занимаюсь лечением пациентов с различными заболеваниями кишки, в том числе прямой. За это время я разработал несколько уникальных методик, которые успешно применяются в различных клиниках. Мною лично проведено более 300 лапароскопических операций при различных заболеваниях прямой кишки и более 100 трансанальных эндоскопических вмешательств. Результаты изложены в монографии «Малоинвазивная хирургия толстой кишки». Моему авторству также принадлежат многочисленные научные публикации, размещенные в рецензируемых изданиях: отечественных и зарубежных. Я также регулярно провожу семинары и мастер-классы, темой которых является хирургическое удаление опухолей кишечника.
Всегда ли формирование аппаратного анастомоза при передней резекции гарантирует восстановление непрерывности кишечника?
Отделение колопроктологии с хирургией тазового дна ФГБУ «Российский научный центр хирургии им. Б.В. Петровского РАМН»
Department of coloproctology with pelvic floor surgery, Federal state government-financed institution «Russian Research Center of Surgery named after acad. B.V. Petrovsky Russian Academy of Medical Science»
Цель исследования
Проанализировать причины и частоту оставления толстокишечных стом, созданных с профилактической или лечебной целью после выполнения передних резекций с формированием аппаратного колоректального анастомоза по поводу рака прямой кишки.
Материал и методы
Проанализированы результаты лечения 215 пациентов, перенесших переднюю резекцию прямой кишки с формированием аппаратного колоректального анастомоза в период с июня 2006 г. по июнь 2011 г.
Результаты
Aim of investigation
To analyze causes and frequency of non-closure of colonic stomas created for prophylactic or medical reasons after anterior resections with stapled colorectal anastomosis for cancer of the rectum.
Material and methods
Results of treatment of 215 patients after anterior rectal resection with formation of stapled colorectal anastomosis from June, 2006 to June, 2011 were analyzed.
Results
Creation of colorectal anastomoses after anterior and low anterior resections is quite often accompanied by formation of «temporary» protective stoma to reduce consequences of possible anastomotic leak (AL). Nevertheless, in some patients these «temporary» stomas are never reversed.. By the moment of discharge from hospital 111 (52%) patients had colostomies: in 103 of them were preventive double-barrelled transverse colostomies were created at primary surgical intervention, the remaining 8 patients underwent colostomy formation in postoperative period because of development of AL. Average follow-up was 32,3 months (12 to 70 months). Among 111 patients the restorative operations were done in 96 (86,5 %). At multivariant analysis the following factors were identified as predictors of non-closure of stoma after anterior resection: death due to disease progression (correlation coefficien = 0,24) and chemotherapy treatment (correlation coefficient = 0,22).
Conclusions
The risk of «temporary» stoma nonclosure even in specialized center is 13,5%. When sphincter-sparing operations are performed for all stages of rectal cancer the most essential risk factors of non-closure of stoma were progression of disease and chemotherapy treatment and patient death related to it, and patient’s death.
При временном выключении из пассажа участка кишечника, несущего анастомоз, формируется двуствольная стома, если же анастомоз разобщается, то отведение кишечного содержимого осуществляется путем формирования одноствольной стомы [9]. Между тем четкое представление о том, какова вероятность сохранения естественного хода кишечника в случае, если планируется проведение передней резекции, позволит мультидисципли-нарному консилиуму правильно спланировать возможные варианты лечения, а хирургу выстроить отношения с пациентом и его родственниками еще на дооперационном этапе. Актуальность такого рода знаний объясняется тем, что недооценка вероятности формирования и невозможности последующего закрытия стомы в процессе хирургического лечения первичной опухоли, часто в комплексе с переоценкой хирургом собственных сил, являются основными слагаемыми того, что несостоятельность анастомоза (НА) после резекции прямой кишки нередко становятся трагедией как для пациента и его близких, так и для врача, выполнявшего операцию.
Целью настоящего исследования является анализ причин и частоты оставления толстокишечных стом, созданных с профилактической или лечебной целью после выполнения передних и низких передних резекций с формированием аппаратного колоректального анастомоза по поводу рака прямой кишки.
Материал и методы исследования
Анализу подвергнуты материалы проспективно заполняемой базы данных, а также истории болезни пациентов, пролеченных в отделении колопроктологии с хирургией тазового дна РНЦХ им. Б.В. Петровского РАМН в период с июня 2006 г. по июнь 2011 г.
Критериями включения в исследование были: первичный гистологически подтвержденный рак прямой кишки и выполнение сфинктеросохраняющего резекционного вмешательства в объеме R0. Критериями исключения служили:
Таким образом, были отобраны больные, у которых выполнено вмешательство по поводу рака прямой кишки с сохранением анального сфинктера и формированием аппаратного колоректального анастомоза с применением различных циркулярных степлеров — DST (Covidien, США), KYGW (Kangdi, Китай), CDH (Ethicon Endosurgery, США). По способу сбора материала исследование является проспективно-ретроспективным, по типу наблюдения — когортным.
Для проведения анализа использовались следующие данные из электронной базы и архивных историй болезни: пол, возраст пациента, индекс массы тела (ИМТ), заболевание сахарным диабетом и дивертикулезом, индекс Американской ассоциации анестезиологов ASA, информация о проведении химио-, лучевой или химиолучевой терапии, высота расположения опухоли, параметры опухолевого процесса и его осложнения (непроходимость, анемия, гипопротеинемия), характер хирургического вмешательства (сочетанное, комбинированное), объем лимфодиссекции, формирование превентивной колостомы, частота и характер развития НА, объем лечебных мероприятий по ее устранению (консервативная терапия, малоинвазивные методы лечения, повторное хирургическое вмешательство), время закрытия стомы (если она формировалась), причины ее поздней ликвидации или отказа от закрытия, а также мероприятия, направленные на лечение полости в зоне несостоятельности швов анастомоза, дата последнего визита и наличие признаков возврата заболевания, при наступлении летального исхода — дата и причина смерти, при выявлении местного рецидива рака прямой кишки — дата, локализация и распространенность заболевания.
Для оценки НА использована классификация, предложенная в 2010 г. Международной исследовательской группой по изучению рака прямой кишки. Согласно классификации выделены три степени тяжести данного осложнения: степень А — соответствует несостоятельности без клинических проявлений, выявляемой, как правило, при контрольной проктографии; степень В — для купирования осложнения требуется проведение антибактериальной терапии и/или миниинвазивных (консервативных) мероприятий; степень С — необходимо повторное хирургическое вмешательство [17].
В случае подозрения на НА в раннем послеоперационном периоде выполнялась проктография с использованием водорастворимого контрастного вещества. По показаниям для определения скрытых затеков и абсцессов проводили компьютерную томографию органов малого таза. Состояние сформированного аппаратного колоректального анастомоза в поздние сроки наблюдения (более 30 дней после операции) определяли с помощью проктографии жидкой бариевой взвесью.
Учитывая, что работа основана на ретроспективном анализе проспективно собираемого клинического материала, подписание пациентом информированного согласия для участия в исследовании и одобрение этическим комитетом не требовались.
При сравнении межгрупповых параметров количественные признаки оценивали при помощи i-критерия Стьюдента, качественные признаки — с использованием точного теста Фишера. Для определения факторов риска отказа от выполнения восстановительной операции применяли метод множественной логистической регрессии и составление корреляционной матрицы с последующим многофакторным анализом и расчетом коэффициента корреляции (КК). Выживаемость пациентов рассчитывали по методу Каплана-Майера. Статистически значимыми считали различия при значениях р
Университет
Николай Сивец, заведующий хирургическим отделением 6-й ГКБ Минска, доктор мед. наук, профессор кафедры военно-полевой хирургии БГМУ:
— Спаечной болезнью называют патологические состояния, связанные с образованием спаек в брюшной полости при ряде заболеваний, при травматических повреждениях внутренних органов, в т. ч. при операционной травме. Относится к числу еще не решенных проблем абдоминальной хирургии. В большинстве случаев — неизбежный брак именно хирургии, а не хирурга. Врач, спасая больного от одного смертельного заболевания, вынужденно способствует возникновению нового.
Большой вклад в изучение спаечной болезни внес Н. И. Пирогов, первым в России выполнивший операцию под эфирным наркозом по поводу странгуляционной тонкокишечной непроходимости. В 1914 году немецкий хирург Эрвин Пайр опубликовал 157 случаев спаек брюшной полости после различных вмешательств и впервые поставил вопрос о необходимости профилактики развития спаек. Исследования продолжили В. А. Оппель, Ю. М. Дедерер, В. А. Блинов.
С развитием хирургии шире становился диапазон операций. Чаще возникали и болезненные состояния, обозначаемые как спайки, спаечная непроходимость, спаечная болезнь. Изучение процесса спайкообразования показало, что болезненные состояния, сопровождающие образование спаек, дают значительные варианты клинических проявлений, обозначаемых симптомокомплексом спаечной болезни. Установлено: в основе спаечного процесса лежат нарушения функции брюшины, связанные с гипоксией, развивающейся вследствие длительного воспалительного процесса, что приводит к нарушению ее фибринолитической функции (А. Н. Дубяга, 1987; Р. А. Женчевский, 1989; D. M. Scott-Combes, 1995; J. N. Thompson, 1995; S. A. Whawell, 1995).
Наличие спаек приводит к снижению качества жизни, хроническим болям в животе, бесплодию у женщин, угрожает кишечной непроходимостью. По данным ряда авторов, 1% перенесших операции на органах брюшной полости ежегодно лечатся от спаечной болезни. Внутрибрюшные сращения после манипуляций хирурга на органах брюшной полости возникают в 80–90% случаев. Частота развития рецидива острой спаечной непроходимости кишечника — 30–69%, повторные операции усугубляют состояние и приводят к летальным исходам в 13–55% случаев.
Существует множество классификаций спаечной болезни, однако в практической работе чаще всего применяется классификация по Д. П. Чухриенко.
Масштабы спаечного процесса — от тотального до образования отдельных тяжей, фиксированных в двух точках. Как правило, спаечный процесс сильнее выражен в зоне операции. Часто петли кишок припаиваются к послеоперационному рубцу или фиксируются к стенкам послеоперационного грыжевого мешка.
Клинические проявления — от незначительных болей в животе до тяжелых форм острой кишечной непроходимости. Одна из основных жалоб — постоянная боль по всему животу без четкой локализации. Также отмечаются тошнота, нередко рвота, вздутие живота, урчание в кишечнике, затруднение отхождения газов и стула, желудочно-кишечный дискомфорт. Имеют место функциональные расстройства со стороны других органов, вовлеченных в спаечный процесс. При спаечной болезни с преобладанием болевого синдрома характерных изменений показателей периферической крови, функций печени, органов ЖКТ обычно не наблюдается.
Для установления диагноза «спаечная болезнь» необходимо провести рентгенологическое обследование ЖКТ, т. к. наличие лапаротомий в анамнезе еще не говорит о присутствии спаек в брюшной полости. Рентгенодиагностика основывается на обнаружении деформаций, необычной фиксации, сращений с брюшной стенкой в полипозиционном исследовании.
Лапароскопия до недавнего времени была противопоказана из-за высокого риска повреждения внутренних органов. Сейчас ее применяют при спаечной болезни как с диагностической, так и с лечебной целью.
Нередко эффективной в плане диагностики оказывается фиброколоноскопия.
Лабораторные данные не дают ничего патогномоничного.
Лечение трудное: никогда нельзя быть уверенным, что лапаротомия, произведенная при спаечной болезни, ликвидирует причины, вызвавшие спаечный процесс.
Вмешательства чаще выполняются по экстренным показаниям. В плановом порядке оперируются пациенты с хронической обтурационной и рецидивирующей спаечной непроходимостью.
В сложной ситуации оказывается хирург при наличии плотного конгломерата кишечных петель. Рациональным будет наложение выключающего обходного анастомоза; радикальным, оптимальным для больного — резекция всего конгломерата.
Самая серьезная проблема — рецидивирующая спаечная непроходимость кишечника, собственно спаечная болезнь.
Операции различны — в зависимости от характера сращений и вида кишечной непроходимости. Наиболее частая — разделение спаек. Плоскостные спайки, вызывающие перегибы, перетяжки, образование двустволок, рассекают. Соединительнотканные тяжи иссекают у места их прикрепления. Десерозированные поверхности на кишке перитонизируют путем наложения узловых швов на стенку кишки. При рубцовых спайках, деформирующих петли кишок без нарушения питания стенки, обычно накладывают обходные анастомозы между петлями тонких кишок, между тонкой и толстой кишкой, реже — между отделами толстой.
Важен выбор доступа. Многих оперируют не по разу — передняя брюшная стенка у них с рубцами. Поэтому лучшим доступом большинство хирургов считает нижнесрединную лапаротомию, которая при необходимости может быть расширена кверху. Доступ через старый операционный рубец чреват вскрытием просвета кишки.
Разрезы передней брюшной стенки должны быть достаточными. Брюшину не следует грубо захватывать и вытягивать на края раны; салфетки, введенные в брюшную полость, не фиксировать к брюшине. Необходимо избегать обширной эвентрации кишечных петель и высыхания висцеральной брюшины, их покрывающей. Кишечные петли укрывать влажными салфетками, смоченными изотоническим раствором хлорида натрия. Во время операции нужен тщательный гемостаз, а излившаяся кровь должна быть своевременно эвакуирована. Важно предупреждать попадание на париетальную и висцеральную брюшину растворов йода, спирта, масел, мелких инородных тел, сухих антибиотиков.
Случай из практики
Больной К., 55 лет. Врач по специальности. Обратился в хирургическое отделение 6-й ГКБ Минска в плановом порядке для консультации с направительным диагнозом «спаечная болезнь брюшной полости с эпизодами кишечной непроходимости». Жалуется на периодическое вздутие живота, приступы болей последние 3 месяца, тошноту, задержку отхождения газов и стула.
В 1971 году в возрасте 10 лет оперирован по поводу острого деструктивного аппендицита с разлитым перитонитом. Проведена аппендэктомия, брюшная полость дренирована. Через 2 недели повторно оперирован в связи с развившейся ранней послеоперационной спаечной кишечной непроходимостью. Выполнена лапаротомия, спайки разделены.
Спустя 10 лет оперирован в одной из клиник Минска по поводу острой спаечной кишечной непроходимости: лапаротомия, спайки рассечены, кишечная непроходимость ликвидирована. Через год в другой клинике снова оперирован по поводу острой спаечной кишечной непроходимости. Имел место массивный спаечный процесс в брюшной полости. Войти в полость удалось только путем иссечения внутренних листков влагалищ прямых мышц живота в мезогастрии.
При ревизии органов брюшной полости выявлено массивное распространение спаек по петлям тонкого и толстого кишечника с вовлечением в процесс большого сальника, париетальной и висцеральной брюшины. В правой половине брюшной полости обнаружен конгломерат из петель тонкого кишечника, слепой, восходящей и правой половины поперечно-ободочной кишки. Попытка выделить петли кишечника из конгломерата безуспешна. Операция завершена наложением обходного илеотрансверзоанастомоза «бок в бок».
Пациент выписан по выздоровлению. Около 20 лет выраженных симптомов нарушения пассажа по кишечнику не было.
Медленное ухудшение началось приблизительно 3 года назад, в течение последних 6 месяцев — интенсивное. Задержка стула и газов на 2–3 дня стала постоянным явлением. Пациент отказался от твердой и грубой пищи, стал есть мало. За 2 месяца до обращения в 6-ю ГКБ Минска принимал только жидкую пищу — часто, небольшими порциями. Для обеспечения пассажа по кишечнику менял положение тела и массировал переднюю брюшную стенку. Началось похудание, снижение работоспособности. В последние 3 недели рацион включал жидкие супы, детские гомогенизированные смеси и жидкий шоколад.
При первичном осмотре — пациент c пониженным питанием, однако без признаков истощения. Кожа обычной окраски, суховатая. Легкие, сердце — без особенностей. Живот не вздут. Имеются рубцы после аппендэктомии и верхнесреднесрединной лапаротомии. При пальпации живот мягкий, слабо болезненный в мезогастрии. По правому боковому каналу определяется инфильтрат без четких границ. Симптомы раздражения брюшины отрицательные.
Клинический диагноз при поступлении: «спаечная болезнь брюшной полости с хроническим нарушением пассажа по кишечнику».
Общеклинические анализы пациента без существенных отклонений.
На рентгенограмме легочные поля без видимых инфильтративных изменений. Усилен, обогащен легочной рисунок в прикорневых отделах, корни малоструктурные, несколько расширены. Сердце не расширено. Аорта уплотнена, развернута.
Выполнена фиброколоноскопия, к которой пациент во избежание острой спаечной кишечной непроходимости готовился сам в течение 2 дней (отказ от питания и питья; ни фортранс, ни очистительные клизмы не применялись). Проблем для осмотра кишечника при колоноскопии не возникло. Эндоскоп введен в купол слепой кишки. Просвет кишки обычный. В нем до печеночного угла незначительное количество промывных вод. Стенки кишки эластичны. Перистальтика, складки не изменены. Слизистая оболочка блестящая, розовая. Сосудистый рисунок в норме. Баугиниева заслонка хорошо выражена. Интубирован терминальный отдел подвздошной кишки. Просвет обычный, на слизистой уплощенные эрозии под фибрином. В просвете восходящей кишки большое количество сформированных каловых масс. В поперечно-ободочной кишке широкое устье илеотрансверзоанастомоза. Эндоскоп проведен в отводящую кишку на глубину 40–50 см. Просвет обычный. На слизистой множественные плоские эрозии на грани изъязвлений, под фибрином. Биопсия (3 фрагмента). Интубирована приводящая кишка на глубину до 35 см (без особенностей).
Заключение: состояние после наложения илеотрансверзоанастомоза (функционирует). Диффузный эрозивный илеит отводящей кишки (болезнь Крона?).
Рентгенологическое исследование кишечника с пассажем сернокислого бария решено не выполнять, дабы не спровоцировать острую спаечную кишечную непроходимость. Клиническая картина и данные колоноскопии достаточные для принятия обоснованного решения о выполнении хирургического вмешательства в плановом порядке.
Пациент оперирован под эндотрахеальным наркозом. Иссечен старый операционный рубец. Верхнесрединная лапаротомия с обходом пупка слева. Свободная брюшная полость как таковая отсутствует. Массивный спаечный процесс после предыдущих операций. К передней брюшной стенке на всем протяжении операционного рубца «вмурованы» петли тонкого кишечника, поскольку брюшина передней брюшной стенки была удалена на предыдущей операции. С техническими трудностями выполнена мобилизация проксимального отдела тонкой кишки. Кишка имеет ригидную стенку, диаметр около 6 см. Выявлено, что в 150 см от трейцевой связки имеется илеотрансверзоанастомоз. Дальнейшая мобилизация позволила установить в области илеотрансверзоанастомоза конгломерат петель тонкого кишечника. Конгломерат разделен, однако сами петли тонкого кишечника со стороны слепой кишки рубцово изменены и признаны функционально несостоятельными. Пальпаторно определяется стриктура отводящего сегмента илеотрансверзоанастомоза. Прослежен ход тонкой кишки от трейцевой связки до илеотрансверзоанастомоза. Последний наложен антиперистальтически.
По правому боковому каналу имеется конгломерат петель тонкого кишечника, не разделенный на предыдущей операции. Попытка его разделения оказалась безуспешной. В результате тщательной ревизии установлено, что причиной нарушения пассажа по тонкой кишке являются множественные ее спайки и перегибы, конгломерат кишечных петель по правому боковому каналу, а также стриктура илеотрансверзоанастомоза. Спайки, насколько это возможно, разъединены. Петли кишечника расправлены по левой половине брюшной полости. Справа разделить петли тонкого кишечника без их повреждения нереально. Показана правосторонняя гемиколэктомия. Единым блоком мобилизован конгломерат кишечных петель, включающий около 80 см рубцово-измененной, со спайками подвздошной кишки, слепую, восходящую и правую половину поперечно-ободочной кишки с илеотрансверзоанастомозом. Правосторонняя гемиколэктомия выполнена. Сформирован изоперистальтический илеотрансверзоанастомоз «конец в конец» двухрядным швом. Анастомоз проходим, наложен без натяжения. Ушито «окно» в брыжейке кишечника. Частично восстановлена целостность брюшины правого бокового канала. Дренажная трубка по правому боковому каналу и в малый таз, а также по левому боковому каналу. Брюшная полость осушена. Рана передней брюшной стенки послойно ушита с наложением механического кожного шва. Повязка. Длительность операции — 9 часов 15 минут.
Макропрепарат: рубцово-измененные петли тонкого кишечника (около 80 см подвздошной кишки), слепая, восходящая и половина поперечно-ободочной с илеотрансверзоанастомозом общей длиной около 140 см.
Гистологическое заключение: фрагменты тонкой и толстой кишок с десквамацией эпителия в просвете, геморрагиями, очаговыми некробиотическими изменениями слизистого слоя толстой кишки, скудной лимфолейкоцитарной инфильтрацией в слизистом и подслизистом слоях. Со стороны серозы — разрастание фиброзной ткани с неоангиогенезом, лейкоцитарной инфильтрацией. В краях резекции — аналогичные изменения. Брыжейка с полнокровными сосудами, лимфатическими узелками с синусовым гистиоцитозом, участками фиброзной ткани.
Заключительный клинический диагноз: хроническая спаечная болезнь брюшной полости с тотальным спаечным процессом и нарушением пассажа по кишечнику. Рубцовая стриктура илеотрансверзоанастомоза.
Операция: лапаротомия, ликвидация спаечного процесса, правосторонняя гемиколэктомия с резекцией илеотрансверзоанастомоза и формированием нового илеотрансверзоанастомоза «конец в конец».
Послеоперационный период протекал гладко, дренажи удалены на 3-и–4-е сутки, рана зажила первичным натяжением. Пациент выписан с выздоровлением. Стул на день выписки и позже — 3 раза в сутки. Признаков нарушения пассажа по кишечнику в ближайшем послеоперационном периоде не отмечается.
1. Операции при длительно протекающей спаечной болезни органов брюшной полости с хроническим нарушением пассажа по кишечнику предпочтительнее проводить в плановом порядке, в дневное время, подготовленной хирургической бригадой.
2. Во избежание повреждения петель тонкого кишечника лучшим доступом следует считать нижнесрединную лапаротомию, которая при необходимости может быть расширена кверху.
3. Рационально накладывать выключающий обходной анастомоз; радикальный, оптимальный для больного вариант — резекция всего конгломерата.
4. Оперируя пациента со спаечной болезнью, необходимо соблюдать ряд известных мер, предупреждающих рецидив спайкообразования.
Медицинский вестник, 18 июля 2016