Что значит неспаренные электроны в основном состоянии
Селивёрстова Алиса Андреевна
Подготовка к:
OnLine
Материал по химии
Данные понятия стоит изучить для выполнения типовых тестовых заданий №1 и №3, так же это поможет понять тему «Ковалентные связи», которая часто встречается в задании №4 ЕГЭ по химии.
Валентность – это количество связей, которые способен образовать химический элемент за счёт объединения своих неспаренных электронов с неспаренными электронами других элементов.
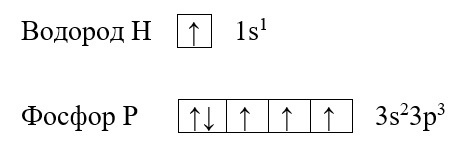
Для наилучшего понимания этой темы необходимо изобразить структуру атомов нескольких элементов, например, фосфора и водорода:
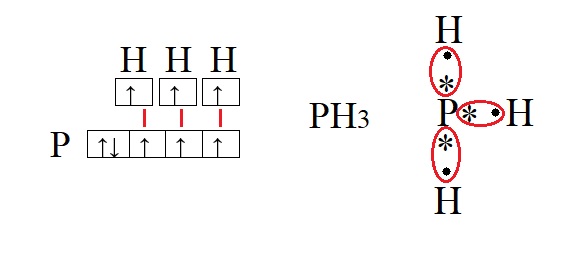
Обе предложенные схемы описывают образование химической связи между фосфором и водородом. Раз фосфору необходимо приобрести пару для целых трёх своих электронов. А водород может «предложить» только один электрон, то к одному атому фосфора может присоединиться три атома водорода. На рисунке справа знаком «*» обозначены неспаренные электроны фосфора, а точками – неспаренные электроны водорода, между которыми и образуется связь (обозначена красным цветом). Связь, при которой происходит объединение электронов в общие пары называется ковалентной, эта связь достаточно прочная и является одной из самых распространённых связей.
Водород содержит один неспаренный электрон, до завершения внешней электронной оболочки ему не хватает всего одного электрона (так как водород имеет только один энергетический уровень, его первый уровень одновременно является и последним, на первом уровне может поместиться только два электрона). Фосфору для полной внешней электронной оболочки не хватает трех электронов, на схеме выше видно, что у него три неспаренных электрона. В таких случаях элементы могут вступать в своеобразных химический «симбиоз»: объединять электроны в общее пользование. При этом неспаренные электроны будут принадлежать одновременно обоим элементам. Данный процесс можно изобразить следующим образом:
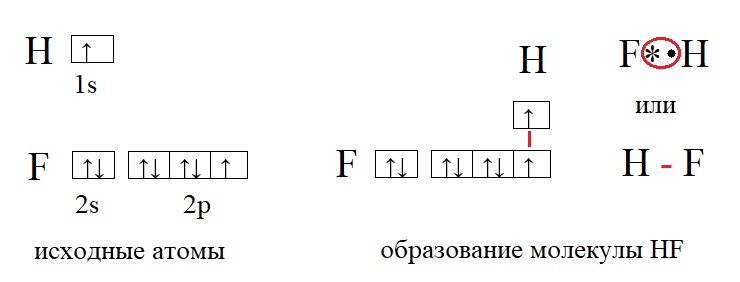
В качестве примеров образования таких связей приведём еще несколько молекул:
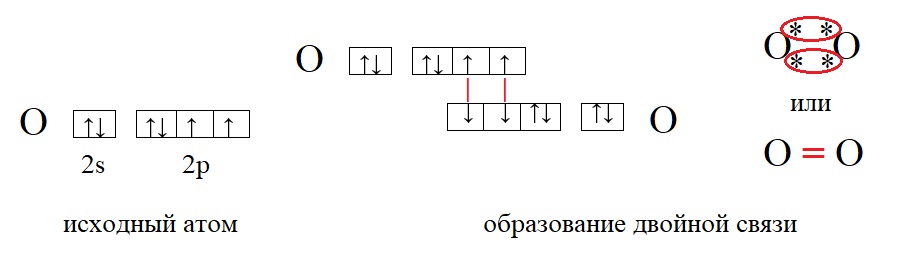
У фтора и у водорода по одному неспаренному электрону, поэтому их валентность равна единице. Валентность записывают римскими цифрами, она не имеет заряда, а отражает лишь количество связей, которые способен образовать элемент. Так валентность фтора I, валентность водорода тоже I. Между такими элементами образуется одна связь. Но есть элементы, способные образовывать гораздо большее количество связей, а значит иметь большую валентность, например:
У кислорода в данном примере валентность равна II, это значит, что каждый атом кислорода способен образовать две связи.
Возбуждённое состояние атома.
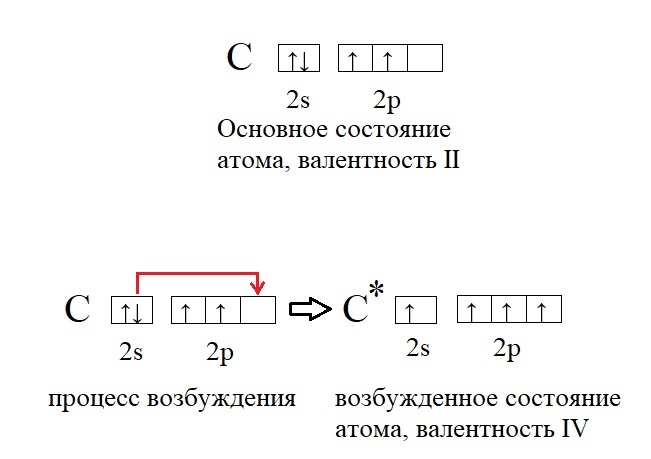
Углерод – один из самых важных элементов на планете Земля, без него невозможна жизнь. Каждая молекула органического вещества содержит четырехвалентный углерод. В чем же подвох? Дело в том, что в основном своём состоянии углерод содержит лишь два неспаренных электрона и способен проявлять валентность II, а не IV, как в органических молекулах или углекислом газе. Однако существует процесс «распаривания» электронов – перенос одного из электронов пары на другую орбиталь, при это валентность повышается:
Не только углерод, но и многие другие элементы способны переходить в возбужденное состояние. У большинства элементов, точнее у тех элементов, что имеют три и более энергетических уровня (то есть находятся ниже второго периода в ПС) на внешнем уровне есть свободная d-орбиталь, на ней в основном состоянии нет электронов, но она может принимать их при возбуждении:
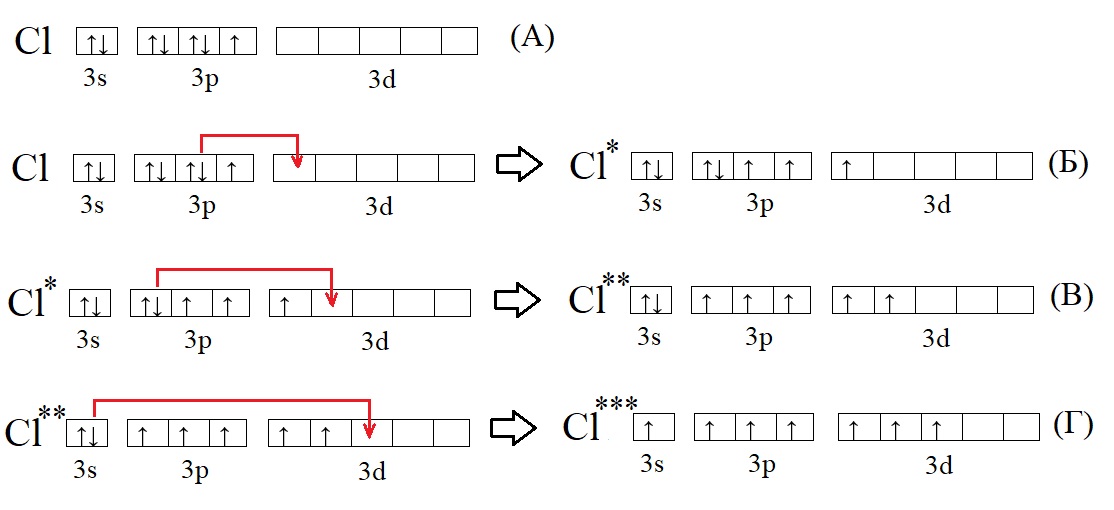
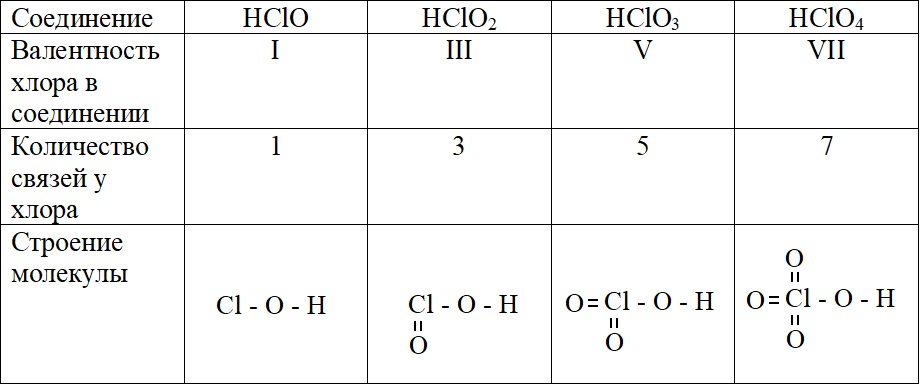
А – основное состояние атома хлора, есть один неспаренный электрон, такая структура соответствует валентности I. Первую валентность хлор имеет в соединениях HCl и HClO.
Б – первое возбужденное состояние хлора, есть три неспаренных электрона, это соответствует валентности III (HClO2).
В – второе возбужденное состояние, пять неспаренных электронов определяют способность проявлять в таком состоянии валентность V (HClO3).
Г – третье валентное состояние, есть семь неспаренных электронов, в таком состоянии хлор может образовывать семь ковалентных связей (HClO4)
Высшая валентность определяется номером группы, в которой стоит элемент, но есть исключения: азот, кислород и фтор. Для этих элементов не характерна высшая валентность, соответствующая номеру группы. Это объясняется тем, что у этих элементов электроны располагаются на двух энергетических уровнях, а свободная d-орбиталь, которая может принять электроны при их распаривании есть у элементов, имеющих три и более энергетических уровня.
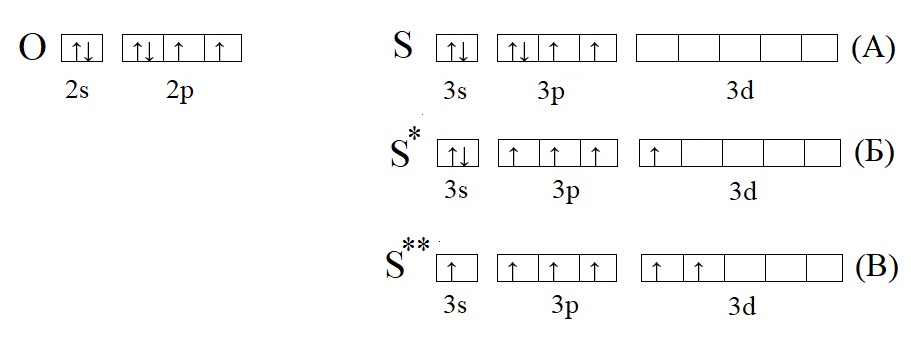
Сравним кислород с серой, у которой есть свободная d-орбиталь:
Кислород из-за отсутствия свободной орбитали не способен проявлять валентность выше II, тогда как у серы есть три валентных состояния: основное, соответствует валентности II (H2S); первое возбужденное, соответствует валентности IV (H2SO3 и SO2); второе возбужденное состояние, соответствует валентности VI (H2SO4, SO3).
Решение задания №3 ЕГЭ по химии
Пример 1.
Для выполнения заданий 1 – 3 используйте следующий ряд химических элементов:
Ответом в заданиях 1 – 3 является последовательность цифр, под которыми указаны химические элементы в данном ряду.
Решение: Электроны могут перераспределяться только внутри одного уровня, общая сумма электронов внешнего уровня, в приведенной в задании формуле, равно пяти, следовательно элемент относится к VА-группе. Это фосфор, азот и мышьяк. Азот не имеет свободную d-орбиталь (см. выше), поэтому выпадает из ответа.
Основное и возбужденное состояние атома
Как известно, атомы могут вступать в химические реакции с другими атомами, с образованием химических связей, путем отдачи/принятия своих/чужих электронов, которые называются валентными (см. Валентность).
В Периодической таблице химических элементов Д. И. Менделеева все атомы отображены в их основном состоянии (состоянии с минимальной энергией). Основное состояние атома описывается электронной конфигурацией атома, согласно его положению в Периодической таблице (см. Таблицу электронных конфигураций атомов химических элементов по периодам.
В определенных ситуациях, некоторые атомы, получая энергию извне, переходят в, так называемое, возбужденное состояние, в котором пребывают относительно короткое время, поскольку возбужденное состояние является нестабильным, после чего возбужденный атом отдает энергию и возвращается в свое основное (стабильное) состояние.
Рассмотрим основное и возбужденное состояние атома на конкретных примерах.
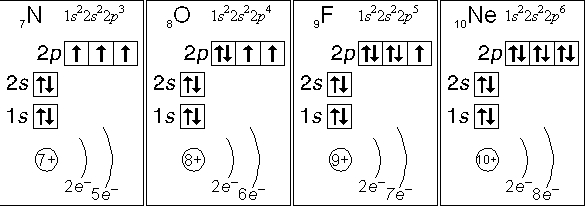
Рис. Электронные конфигурации атомов азота, кислорода, фтора, неона.
Азот, кислород, фтор и неон не могут иметь возбужденного состояния по той простой причине, что они не имеют свободной орбитали с более высокой энергией, на которую могли бы «перескакивать» спаренные электроны с орбиталей с меньшей энергией.
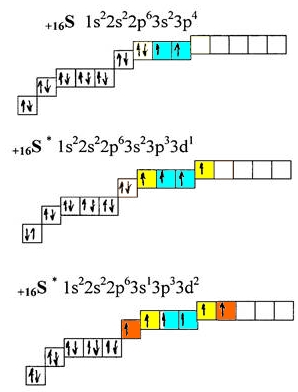
Рис. Возбужденное состояние атома серы.
В основном состоянии атом серы имеет 2 валентных электрона (голубой цвет). Как видно из вышеприведенного рисунка, получая энергию извне, у атома серы могут появляться еще 2 (желтый цвет) или 4 (желтый+оранжевый) дополнительных валентных электрона, при этом общее кол-во валентных электронов увеличивается до 4 или 6 соответственно.
Если вам понравился сайт, будем благодарны за его популяризацию 🙂 Расскажите о нас друзьям на форуме, в блоге, сообществе. Это наша кнопочка:
Код кнопки: 
Политика конфиденциальности Об авторе
Атомы и электроны
Атомно-молекулярное учение
Описываемая модель атома называется «планетарной» и была предложена в 1913 году великими физиками: Нильсом Бором и Эрнестом Резерфордом
Запомните, что в невозбужденном состоянии атом содержит одинаковое число электронов и протонов. Так у кальция (порядковый номер 20) в ядре находится 20 протонов, а вокруг ядра на электронных орбиталях 20 электронов.
Я еще раз подчеркну эту важную деталь. На данном этапе будет отлично, если вы запомните простое правило: порядковый номер элемента = числу электронов. Это наиболее важно для практического применения и изучения следующей темы.
Электронная конфигурация атома
Электроны атома находятся в непрерывном движении вокруг ядра. Энергия электронов отличается друг от друга, в соответствии с этим электроны занимают различные энергетические уровни.
Состоит из s-подуровня: одной «s» ячейки (2s 2 ) и p-подуровня: трех «p» ячеек (2p 6 ), на которых помещается 6 электронов
Состоит из s-подуровня: одной «s» ячейки (3s 2 ), p-подуровня: трех «p» ячеек (3p 6 ) и d-подуровня: пяти «d» ячеек (3d 10 ), в которых помещается 10 электронов
Состоит из s-подуровня: одной «s» ячейки (4s 2 ), p-подуровня: трех «p» ячеек (4p 6 ), d-подуровня: пяти «d» ячеек (4d 10 ) и f-подуровня: семи «f» ячеек (4f 14 ), на которых помещается 14 электронов
Зная теорию об энергетических уровнях и порядковый номер элемента из таблицы Менделеева, вы должны расположить определенное число электронов, начиная от уровня с наименьшей энергией и заканчивая к уровнем с наибольшей. Чуть ниже вы увидите несколько примеров, а также узнаете об исключении, которое только подтверждает данные правила.
Подуровни: «s», «p» и «d», которые мы только что обсудили, имеют в определенную конфигурацию в пространстве. По этим подуровням, или атомным орбиталям, движутся электроны, создавая определенный «рисунок».
Правила заполнения электронных орбиталей и примеры
Должно быть, вы обратили внимание на некоторое несоответствие: после 3p подуровня следует переход к 4s, хотя логично было бы заполнить до конца 4s подуровень. Однако природа распорядилась иначе.
Запомните, что, только заполнив 4s подуровень двумя электронами, можно переходить к 3d подуровню.
Теперь мы располагаем указанное количество электронов на энергетических уровнях, руководствуясь правилами заполнения.
Обращаю ваше особе внимание: на 2p-подуровне углерода мы расположили 2 электрона в разные ячейки, следуя одному из правил. А на 3p-подуровне у серы электронов оказалось много, поэтому сначала мы расположили 3 электрона по отдельным ячейкам, а оставшимся одним электроном дополнили первую ячейку.
Внешний уровень и валентные электроны
Тренировка
Потренируйтесь и сами составьте электронную конфигурацию для магния и скандия. Определите число электронов на внешнем (валентном) уровне и число неспаренных электронов. Ниже будет дано наглядное объяснение этой задаче.