аспирация желудочного содержимого что это
Синдром Мендельсона: не раскисай
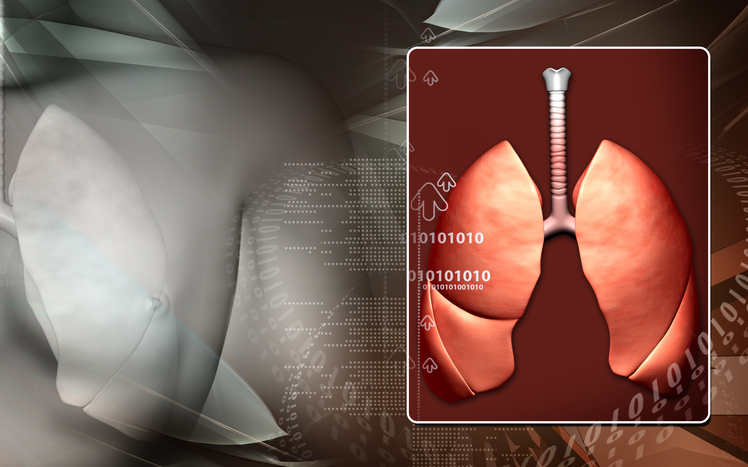
Анестезиолог-реаниматолог Юлия Егорова о причинах и последствиях поражения легких кислым содержимым желудка
Повреждение легких при аспирации кислого желудочного содержимого известно врачам более полутора веков. Впервые аспирацию рвотными массами как причину смерти описал шотландский акушер-гинеколог Джеймс Янг Симпсон в 1848 году, указание на это осложнение при анестезии появилось в литературе пятью годами позже. В 50‑х годах прошлого века вошел в обиход термин «химический пневмонит». Систематическое изучение осложнений, вызванных аспирацией, провел в 1946 году американский акушер Кертис Мендельсон. Благодаря его исследованиям были разработаны меры профилактики у рожениц, а также клинически разделены банальная обтурация дыхательных путей и симптомокомплекс, вызванный химическим повреждением слизистой бронхов и альвеол, который и получил название синдрома Мендельсона. По мере совершенствования диагностики стало очевидно, что проблема осложнений аспирации желудочного содержимого — не прерогатива одного акушерства, и актуальна для других разделов медицины.
Синдром Мендельсона часто имеет ятрогенную природу, информация о нем может утаиваться врачами, поэтому достоверной информации о распространенности синдрома нет.
Механизмы развития
Кислое содержимое желудка может попадать в дыхательные пути при рвоте либо в результате регургитации, пассивного затекания в ротоглотку, обусловленного слабостью сфинктеров пищевода. В иностранной литературе термин «регургитация» иногда сопровождается определением «немая» или «молчаливая», поскольку этот вариант гораздо более труден для диагностики и может пройти незамеченным.
Риск аспирации повышают:
Опасная ситуация для возникновения болезни Мендельсона — это вводный наркоз, особенно при выполнении его в экстренных ситуациях, неподготовленным пациентам и беременным женщинам. Высок риск аспирации при оказании первой помощи, транспортировке и уходе за тяжелыми пациентами.
При попадании содержимого желудка в дыхательные пути клиническая картина зависит от его количества и рН. При небольшой, в пределах 30 мл, аспирации жидкости с рН более 2,5 нарушения дыхания не возникает или имеет транзиторный характер. При попадании более кислого содержимого патогенез нарушений дыхания обусловлен не столько механическим препятствием, сколько немедленными рефлекторными реакциями. Ларинго- и бронхоспазм возникают в первые же минуты воздействия кислоты на слизистую бронхов. Ларингоспазму сопутствует брадиаритмия, возникающая как вагусный рефлекс. Рефлекторные изменения носят резкий, но непродолжительный характер и в течение короткого времени регрессируют, особенно при небольшом объеме аспирации. Впоследствии химический ожог слизистой вызывает отек стенки бронхов и повышенную экссудацию, что сопровождается явлениями аспирационного пневмонита и интерстициального отека легочной ткани. Выраженность повреждения легких зависит от объема поражения и варьирует от преходящих нарушений до респираторного дистресс-синдрома взрослых (РДСВ).
Симптомы синдрома Мендельсона
Течение синдрома Мендельсона отражает патогенез. В первые минуты возникает одышка, тахипноэ, цианоз. Возможно выслушивание дистантных сухих свистящих хрипов. Аускультативная картина богатая, включает большое количество свистящих сухих хрипов, возможно выслушать влажные крупнопузырчатые хрипы и единичные «немые» участки. Показатели сатурации и газового состава крови ухудшаются, возникает гипоксемия и гиперкапния. В общем, клиническая картина напоминает приступ бронхиальной астмы, терапия требуется патогенетическая. Также необходимо принять все меры по удалению аспирированных масс из дыхательных путей.
Санационные бронхоскопии с промыванием можно отложить до купирования острого состояния.
Далее клиническая картина синдрома Мендельсона обусловлена наличием химического ожога слизистой дыхательных путей. Пораженные участки некротизируются, возникает повышенная экссудация, явления интерстициального отека. Эта стадия более трудна для диагностики, потому что нередко аспирация, как ятрогенное осложнение, умалчивается или в процессе транспортировки тяжелого пациента и противошоковых мероприятий остается незамеченной. В таком случае врач сталкивается с труднообъяснимым снижением показателей дыхания, не связанным с основным заболеванием. Клинически и аускультативно это интерстициальный отек легких — гипоксия, потребность в ИВЛ с ПДКВ, сухие высокотональные свистящие хрипы. Рентгенологически — картина интерстициального отека легочной ткани с преимущественным поражением правого легкого, возможные участки ателектазов. Бронхоскопическая картина может отражать различные степени поражения слизистой бронхов, от гиперемии до некрозов. Специфической терапии для лечения синдрома Мендельсона не существует, однако установление диагноза помогает определить причину дыхательной недостаточности, подобрать рациональный режим ИВЛ и определяет настороженность в отношении бактериальных осложнений.
Профилактика синдрома Мендельсона в анестезиологии
Профилактика синдрома Мендельсона гораздо более эффективна, чем его лечение.
В плановом порядке важно соблюдать правила подготовки пациентов к оперативному вмешательству и инвазивным манипуляциям. Перед любым наркозом и медикаментозной седацией желудок должен быть пустым. Важно не только провести беседу с пациентом о необходимости голода перед манипуляцией, но и уточнить непосредственно перед вмешательством, соблюдались ли эти рекомендации. Если, несмотря на запрет, пациент употреблял твердую пищу или более чем 150 мл жидкости менее чем за 4 часа до манипуляции — плановую операцию или исследование следует отменить.
В экстренных случаях нельзя пренебрегать установкой желудочного зонда и промыванием желудка, даже несмотря на то что наличие зонда само по себе ослабляет нижний пищеводный сфинктер. В акушерстве необходимо соблюдать полный комплекс мер по подготовке к родам для улучшения пассажа пищи по ЖКТ и снижения кислотности содержимого желудка.
При вводном наркозе необходимо убедиться в наличии в операционной работающего электроотсоса. Для индукции анестезии по возможности стоит отказаться от применения миорелаксантов короткого действия и отдавать предпочтение препаратам, подавляющим глоточный и рвотный рефлексы.
При оказании первой помощи пациентам с нарушениями сознания следует контролировать положение пациента. При возникновении рвотных движений необходимо незамедлительно применить прием Селлика — давление на перстневидный хрящ с одновременной фиксацией трахеи в среднем положении. При возникновении рвоты — наклонить голову пациента, после чего очистить ротоглотку от остатков рвотных масс.
Транспортировку пациентов с нарушением сознания нужно осуществлять либо после интубации трахеи с раздутой манжеткой эндотрахеальной трубки либо с применением ларингеальной маски или специальных воздуховодов, исключающих как западение языка, так и аспирацию желудочного содержимого в дыхательные пути.
Необходим строгий врачебный контроль манипуляций по сестринскому уходу за тяжелыми пациентами. Перемена положения пациента при профилактике пролежней и смене постельного белья, зондовое кормление и другие манипуляции могут спровоцировать рефлюкс желудочного содержимого с развитием аспирации.
Нашли ошибку? Выделите текст и нажмите Ctrl+Enter.
Как предотвратить аспирацию
Эта информация разъясняет, что вы можете сделать для предотвращения аспирации, когда вы едите, пьете или получаете питание через зонд.
Об аспирации
Аспирация — это попадание пищи или жидкости в дыхательные пути вместо пищевода. Пищевод — это трубчатый орган, по которому пища и жидкости проходят из полости рта в желудок. Аспирация может произойти, когда вы едите или пьете, либо когда получаете питание через зонд. Она также возможна при рвоте или изжоге.
Вы можете быть подвержены риску аспирации, если вы испытываете проблемы при глотании. Это происходит из-за того, что пища или жидкость может застрять в задней части горла и попасть в дыхательные пути. Аспирация может вызвать пневмонию, респираторные инфекции (инфекции носа, горла или легких) и другие проблемы со здоровьем.
Признаки аспирации
Признаки аспирации включают:
Вы и ухаживающее за вами лицо должны следить за этими признаками до, во время и после употребления пищи или напитков, либо во время питания через зонд.
Если у вас появился любой из этих признаков, прекратите есть, пить или получать питание через зонд. Незамедлительно позвоните своему медицинскому сотруднику.
Профилактика аспирации
Следуйте нижеприведенным рекомендациям для предотвращения аспирации при употреблении пищи и напитков через рот:
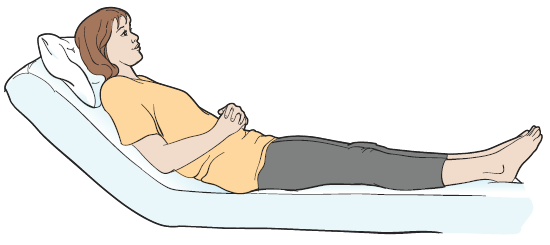
Рисунок 1. Сидячее положение под углом 45 градусов
Следуйте нижеприведенным рекомендациям для предотвращения аспирации при получении питания через зонд :
Сохранение ритма приема пищи
Во избежание аспирации важно не торопиться при приеме пищи. Чтобы не съесть больше, чем сможете переварить, соблюдайте следующие рекомендации:
Если у вас возникнут вопросы, позвоните клиническому врачу-диетологу по номеру 212-639-7312 или квалифицированному специалисту по питанию по номеру 212-639-6984.
Когда следует обращаться к своему медицинскому сотруднику
Свяжитесь с медицинским сотрудником, если у вас появятся какие-либо из перечисленных ниже симптомов:
При появлении проблем с дыханием или возникновении любой другой чрезвычайной ситуации незамедлительно позвоните по номеру 911 или поезжайте в ближайший пункт неотложной медицинской помощи.
Синдром Мендельсона – острый аспирационный пневмонит, развивающийся вследствие попадания в дыхательные пути кислого желудочного содержимого. Чаще возникает как осложнение анестезиологического пособия. Клиника синдрома Мендельсона разворачивается в считанные часы и включает в себя одышку, лихорадку, дыхательную недостаточность, присоединение бактериальной пневмонии. Синдром диагностируется на основании клинических, аускультативных и рентгенологических данных. Первая помощь предполагает аспирацию содержимого из дыхательных путей, устранение бронхоспазма, перевод больного на ИВЛ, проведение лечебной бронхоскопии. В дальнейшем назначается противоотечная и антибактериальная терапия.
МКБ-10
Общие сведения
Причины
Единственно возможной причиной синдрома Мендельсона является аспирация содержимого желудка, повреждающее действие которого связано с высокой кислотностью химуса. Агрессивный субстрат приводит к сильнейшему химическому ожогу и отеку слизистой дыхательных путей, быстрому разрушению эпителия бронхиол и альвеол и пропотеванию транссудата в альвеолы. Это сопровождается развитием некардиогенного отека легких и респираторного дистресс-синдрома (гипоксемической формы дыхательной недостаточности).
В некоторых случаях вместе с желудочным соком в дыхательные пути могут попадать частички непереваренной пищи, вызывающие механическую закупорку бронхов среднего калибра (асфиктическая форма дыхательной недостаточности). В обоих случаях в конечном итоге развивается бронхиальная обструкция.
Для возникновения клиники синдрома Мендельсона достаточно попадания в респираторный пути даже небольшого объема (20-30 мл) желудочного сока с низким рН. Самые тяжелые повреждения отмечаются при аспирации большого количества кислого содержимого (>0,4 мл/кг), имеющего рН 5.
Факторами, предрасполагающими к аспирации или регургитации содержимого желудка и развитию синдрома Мендельсона, выступают нарушения сознания, обусловленные общим наркозом, алкогольным или наркотическим опьянением, действием седативных препаратов, ЧМТ, комой. Чаще всего синдром Мендельсона возникает как осложнение экстренных хирургических вмешательств (чаще брюшнополостных операций и кесарева сечения), когда не уделяется должного внимания подготовке ЖКТ. Дополнительными факторами риска служат повышение внутрибрюшного давления (у беременных в III триместре, больных ожирением, при парезах кишечника), заболевания ЖКТ (язвенная болезнь желудка и ДПК, эзофагит, гастрит, расширение пищевода, дивертикул пищевода, грыжа пищеводного отверстия диафрагмы).
Симптомы
Клиника синдрома Мендельсона разворачивается очень быстро, в течение нескольких часов. Патологические изменения проходят три фазы: острого ларинго- и бронхиолоспазма, частичного купирования бронхиолоспазма и нарастания острой дыхательной недостаточности.
В первые минуты после аспирации в результате рефлекторного сужения бронхиол возникает кашель, экспираторная одышка, цианоз кожных покровов, тахикардия, снижение АД. Первую фазу синдрома Мендельсона нередко ошибочно принимают за приступ бронхиальной астмы. В легких прослушиваются разнокалиберные влажные и свистящие хрипы; происходит повышение ЦВД, набухание вен шеи. Быстро развивается ОДН I—III ст.; уже на первом этапе возможен летальный исход от асфиксии.
Вторая фаза знаменуется самопроизвольным частичным расширением бронхиол и некоторым клиническим улучшением. Состояние больного временно стабилизируется: уменьшается одышка, снижается давление. Примерно через 48 часов наступает третья фаза синдрома Мендельсона. В этот период быстро нарастают явления бронхиолита и пневмонита, что вызывает новое ухудшение состояния больного и прогрессирование дыхательной недостаточности. Присоединяются бактериальные осложнения – развивается аспирационная пневмония (лихорадка, кашель с мокротой, лейкоцитоз). Летальный исход обычно наступает от отека легких.
Диагностика
Для клинической диагностики синдрома Мендельсона имеет значение характерная триада симптомов (тахипноэ, тахикардия, цианоз), а также невозможность устранить гипоксемию даже при подаче чистого кислорода (данный признак указывает на шунтирование венозной крови). При мониторинге газового состава крови отмечается снижение РаО2 до 35-45 мм рт. ст. Аускультативная картина характеризуется наличием множественных свистящих хрипов (в нижних отделах – крипитирующих хрипов).
При проведении бронхоскопии выявляется отек и гиперемия слизистой, наличие в просвете бронхов аспирированной жидкости, нередко с комочками пищи. На рентгенограммах легких видны очаги гиповентиляции, диффузное затемнение легочных полей («шоковое легкое»). С присоединением вторичной бактериальной пневмонии появляются очаги инфильтрации.
Лечение синдрома Мендельсона
Неотложная помощь должна быть оказана больному сразу после установления факта аспирации желудочного содержимого. В первую очередь необходимо немедленно удалить аспират из полости рта и дыхательных путей с помощью электроотсоса. После этого производится интубация трахеи и перевод больного на ИВЛ в режиме гипервентиляции с ингаляцией 100% кислорода. В дальнейшем выполняется зондовое опорожнение желудка и санационная бронхоскопия: для бронхоальвеолярного лаважа используется стерильный физраствор. Лечение больного синдромом Мендельсона осуществляется в ОРИТ совместно анестезиологами-реаниматологами и пульмонологами.
С целью ликвидации бронхиолоспазма вводится атропин, эуфиллин, преднизолон или дексаметазон, орципреналин. Обязательно производится перкуссионный массаж грудной клетки. Для нейтрализации высокой кислотности осуществляются щелочные ингаляции раствора гидрокарбоната натрия. Проводится инфузия электролитных растворов, глюкозы, свежезамороженной плазмы, альбумина; стимуляция диуреза. Антибиотикотерапия показана для профилактики и лечения аспирационной пневмонии. Экстубация производится после восстановления спонтанного дыхания и самостоятельной способности поддержания адекватного газообмена.
Прогноз и профилактика
Летальные исходы при возникновении синдрома Мендельсона наблюдаются в 60% случаев, а в акушерской практике – более чем в 70% случаев. Чтобы предотвратить это грозное осложнение, перед экстренными операциями необходимо эвакуировать желудочное содержимое с помощью зонда (за исключением тех случаев, когда это противопоказано – например, при желудочном кровотечении). Перед плановыми операциями запрещается прием пищи и жидкости за 10-12 часов до вмешательства, при необходимости назначается прием антацидов, Н2-блокаторов и прокинетиков. Во избежание синдрома Мендельсона необходимо соблюдение правильного алгоритма анестезиологического пособия во время экстренных хирургических вмешательств.
Протокол лечения пациентов с острым панкреатитом
Протокол разработан на основе рекомендаций Российского общества хирургов и приказа Департамента здравоохранения города Москвы № 320 (2011г.)
Классификация острого панкреатита, формулировка диагноза.
1. Острый алкогольно-алиментарный панкреатит.
2. Острый билиарный панкреатит (холелитиаз, парафатериальный дивертикул дивертикул, папиллит, описторхоз ).
3. Острый травматический панкреатит (вследствие травмы поджелудочной железы, в том числе операционной или после ЭРХПГ).
4. Другие этиологические формы (аутоиммунные процессы, сосудистая недостаточность, васкулиты, лекарственные, инфекционные заболевания), аллергические, дисгормональные процессы при беременности и менопаузе, заболевания близлежащих органов.
1. Острый панкреатит лёгкой степени. Панкреонекроз при данной форме острого панкреатита не образуется (отёчный панкреатит) и органная недостаточность не развивается.
2. Острый панкреатит тяжёлой степени. Характеризуется наличием органной и полиорганной недостаточности, перипанкреатического инфильтрата, формированием псевдокист, развитием инфицированного панкреонекроза (гнойно-некротического парапанкреатита).
Диагностика острого панкреатита.
Диагностическая программа включает в себя: клиническую, лабораторную и инструментальную верификацию диагноза острого панкреатита; стратификацию пациентов на группы в зависимости от тяжести заболевания; построение развернутого клинического диагноза.
Верификация диагноза острого панкреатита включает в себя: физикальное исследование – оценка клинико-анамнестической картины острого панкреатита; лабораторные исследования – общеклинический анализ крови, биохимический анализ крови (в т.ч. а-амилаза, липаза, билирубин, АлАТ, АсАТ, ЩФ, мочевина, креатинин, электролиты, глюкоза), общеклинический анализ мочи, коагулограмма, группа крови, резус-фактор; обзорная рентгенограмма брюшной полости (увеличение диаметра петель тонкой кишки, уровни жидкости), рентгенография грудной клетки (гидроторакс, дисковидные ателектазы, высокое стояние купола диафрагмы, гипергидратация паренхимы, картина ОРДС), ЭКГ; УЗИ брюшной полости – оценка наличия свободной жидкости, оценка состояния поджелудочной железы (размеры, структура, секвестры, жидкостные включения), оценка состояния билиарного тракта (гипертензия, конкременты), оценка перистальтики кишечника.
Пациентам с предположительным клиническим диагнозом острого панкреатита показано выполнение ЭГДС (дифференциальный диагноз с язвенным поражением гастродуоденальной зоны, осмотр БДС).
Стратификация пациентов по степени тяжести острого панкреатита по следующим критериям:
1. Тяжелый панкреатит (более одного из критериев):
Пациенты с тяжелым панкреатитом госпитализируются в отделение хирургической реанимации.
Пациенты с панкреатитом легкого течения госпитализируются в хирургическое отделение.
Лечение пациентов с острым панкреатитом легкого течения.
Базисный лечебный комплекс:
В динамике ежедневно оцениваются: критерии ССВР, а-амилаза. Требования к результатам лечения: купирование болевого синдрома, клинико-лабораторное подтверждение разрешения активного воспалительного процесса.
Отсутствие эффекта от проводимой анальгетической и спазмолитической терапии в течение 12-48 часов, быстро прогрессирующая желтуха, отсутствие желчи в ДПК при ЭГДС, признаки билиарной гипертензии по данным УЗИ свидетельствуют о стеноза терминального отдела холедоха (вклиненный конкремент БДС, папиллит). В этом случае показано проведение ЭПСТ. При остром панкреатите ЭПСТ производится без ЭРХПГ!
Мониторинг общесоматического и локального статуса пациентов с тяжелым острым панкреатитом:
Лечебная тактика у пациентов с острым панкреатитом тяжелого течения в фазу панкреатогенной токсемии.
Основным видом лечения острого панкреатита в фазе токсемии является комплексная интенсивная консервативная терапия.
Базисная терапия острого панкреатита дополняется следующими компонентами:
— интенсивное ингибирование секреции поджелудочной железы (октреотид 300 мкг x 3 раза в сутки подкожно или 1000 мкг в сутки непрерывной инфузией) до нормализации показателей а-амилазы и липазы;
— продленная эпидуральная анестезия;
— доза инфузионных растворов должна быть не менее 40-60 мл/кг массы тела больного в сутки; высокообъемная инфузионная терапия включает в себя сбалансированные кристаллоидные растворы и коллоидные растворы (в сочетании кристаллоидов и коллоидов 2:1);
— реологически активная терапия: коллоиды в сочетании с антиагрегантами, НФГ (15-20 тыс. ед. в сутки) или НМГ; введение антиоксидантов;
— экстракорпоральная детоксикация: продленная вено-венозная гемодиафильтрация и серийный плазмаферез;
— установка ниппельного зонда энтерального питания за дуодено-еюнальный переход с одновременной установкой назо-гастрального зонда для желудочной декомпрессии; введение в первые 24-48 часов в тонкую кишку электролитных растворов (1 – 2 литра/сут); последующее энтеральное питание олигомерными и полимерными питательными смесями;
— обеспечение смешанной парентерально-энтеральной нутритивной поддержки с калоражем не менее 2000 ккал в сутки.
Хирургическая тактика:
Оперативные вмешательства лапаротомным доступом в фазу ферментной токсемии противопоказаны. По показаниям применяются малоинвазивные вмешательства – чрезкожные пункции и дренирования, лапароскопия, ЭПСТ.
Чрескожная пункция и дренирование острых жидкостных скоплений под контролем УЗИ позволяет снизить уровень эндогенной интоксикации.
Пункции подлежат очаги острых жидкостных скоплений, располагающиеся в сальниковой сумке, забрюшинной клетчатке, и в случаях, когда лапароскопическое дренирование острых жидкостных скоплений в брюшной полости невозможно (тяжесть состояния больного, больной перенес раннее несколько операций на брюшной полости, гигантская вентральная грыжа).
Экстренная декомпрессия желчевыводящих путей у больных острым билиарным панкреатитом показана при: отсутствии эффекта от проводимой консервативной терапии в течение 6-12 часов; вклиненном конкременте БДС; нарастании явлений механической желтухи; прогрессировании явлений острого холецистита и/или холангита.
При диагностированном резидуальном или рецидивном холедохолитиазе, холедохолитиазе на фоне хронического калькулезного холецистита, остром обтурационном холангите, папиллите или папиллостенозе показано проведение ЭПСТ без ЭРХПГ! При невозможности проведения ЭПСТ показана чрескожная чреспеченочная микрохолецистостомия под контролем УЗИ. При невозможности добиться адекватной декомпрессии из вышеописанных доступов показана чрескожная чреспеченочная холангиостомия. В случае вклинения конкремента в области большого дуоденального сосочка предпочтение отдается эндоскопической папиллогомии.
Показания к лапароскопии:
— клиническая картина перитонита с наличием УЗ-признаков свободной жидкости в брюшной полости;
— необходимость проведения дифференциальной диагностики с другими острыми заболеваниями органов брюшной полости.
Лечебная тактика у пациентов с тяжелым панкреатитом в фазу асептической секвестрации.
Клинико-морфологической формой острого панкреатита в фазе асептической секвестрации является постнекротическая псевдокиста поджелудочной железы, срок формирования которой составляет от 4 недель и в среднем до 6 месяцев.
Исходы острого панкреатита в фазу асептической секвестрации:
4) Инфицирование зон панкреатогенной деструкции (развитие гнойных осложнений).
Диагностические критерии фазы асептической секвестрации:
— уменьшение степени выраженности ССВР, отсутствие признаков инфекционного процесса;
— УЗ-признаки и КТ-признаки асептической деструкции в очаге поражения (сохраняющееся увеличение размеров поджелудочной железы, нечеткость ее контуров и появление жидкости в парапанкреатической и забрюшинной клетчатке c последующим формированием псевдокист, визуализация секвестров в ткани поджелудочной железы и в парапанкреатической клетчатке).
Лечение в фазу асептической секвестрации.
Хирургическая тактика у пациентов с острым панкреатитом в период асептических деструктивных осложнений.
Показание к оперативным вмешательствам – наличие отграниченных парапанкреатических жидкостных скоплений (с секвестрами или без таковых).
Приоритетным является выполнение малоинвазывных чрезкожных вмешательств под УЗ-контролем или КТ-контролем.
Чрезкожные пунции под УЗ-контролем показаны при наличии жидкостных образований объемом не более 100 мл. Систематические пункции могут послужить окончательным методом хирургической помощи или позволить отложить выполнение радикальной операции.
Чрезкожное дренирование под УЗ-контролем проводится при наличии жидкостных скоплений объемом более 100 мл. Дренирование кисты предусматривает аспирационно-промывную санацию полости кисты и оценку адекватности дренирования с помощью динамической фистулографии.
Оперативные вмешательства лапаротомическим и (или) люмботомическим доступом проводятся при наличии технических ограничений к безопасному выполнению пункционных вмешательств (расположение на предполагаемой траектории вмешательства ободочной кишки, селезенки, крупных сосудов, плеврального синуса); при преобладании в жидкостном скоплении или острой псевдокисте тканевого компонента (секвестров).
При очаговом процессе следует использовать мини-лапаротомию (параректальную, трансректальную, косую в подреберье) или мини-люмботомию. При распространенном процессе следует использовать широкую срединную лапаротомию, широкую люмботомию или их сочетание.
В условиях завершенной секвестрации и полной некросеквестрэктомии операция должна завершатся «закрытым» дренированием образовавшейся полости 2-х просветными дренажами, по числу отрогов полости, которые выводятся на брюшную стенку вне операционной раны. Рана ушивается наглухо. В послеоперационном периоде проводится аспирационно-промывное лечение до облитерации полости.
При незавершенной секвестрации и неполной некрсеквестрэктомии операция должна завершатся «открытым» дренированием 2-х просветными дренажами по числу отрогов полости, выводимыми вне раны через контрапертуры и введением тампонов в образовавшуюся полость через операционную рану. Рана частично ушивается и формируется бурсооментостома или люмбостома для доступа к очагу деструкции при последующих программных санациях. По дренажам проводится аспирационно-промывное лечение, перевязки с дополнительной некрсеквестрэктомией и сменой тампонов до очищения полости с последующим наложением вторичных швов на рану и переходом на закрытое дренирование.
Лечебная тактика у пациентов с тяжелым панкреатитом в фазу гнойно-септических осложнений.
Клинико-морфологическими проявлениями острого панкреатита в фазу гнойно-септических осложнений являются:
Диагностические критерии фазы гнойно-септических осложнений:
1. Клинико-лабораторные проявления инфекционного процесса: прогрессирование клинико-лабораторных показателей ССВР на 3 неделе заболевания; высокие показатели маркеров острого воспаления (С-реактивного белка – более 120 г/л и прокальцитонина – более 2 нг/мл); лимфопения, увеличение СОЭ, повышение концентрации фибриногена; ухудшение состояния больного по интегральным оценочным системам.
2. Инструментальные критерии нагноения: КТ-признаки (нарастание в процессе наблюдения жидкостных образований, в очаге панкреатогенной деструкции и/или наличие пузырьков газа) и/или положительные результаты бактериоскопии, полученные при тонкоигольной пункции.
Хирургическая тактика у пациентов с острым панкреатитом в фазу гнойно-септических осложнений.
При развитии гнойных осложнений показано срочное хирургическое вмешательство.
Малоинвазивные пункционные вмешательства (пункция и дренирование) показаны при наличии четко отграниченных гнойных скоплений (жидкостные скопления, панкреатический абсцесс, инфицированная псевдокиста) без выраженного тканевого компонента (секвестров). Оптимальным следует считать установку в полость гнойника двух дренажей с последующей установкой промывной системы.
Оперативные вмешательства лапаротомным и люмботомическим доступом показаны в случаях значительной распространенности процесса в забрюшинной клетчатке или при отграниченном процессе с наличием в полости гнойника крупных некротических фрагментов. Основным методом санации гнойно-некротических очагов является некрсеквестрэктомия, которая может быть как одномоментной, так и многоэтапной.
Оптимальным доступом является внебрюшинный, в виде люмботомии с продлением разреза на брюшную стенку по направлению к прямой мышце живота, что позволяет при необходимости, дополнить этот доступ лапаротомией.
Способ завершения операции зависит от адекватности некрсеквестрэктомии. При полном удалении некротических тканей возможно «закрытое» дренирование двухпросветными дренажами по числу отрогов полости с выведением дренажей через контрапертуры на брюшной стенке. Через дренажи в послеоперационном периоде проводится аспирационно-промывная санация.
При неполном удалении некротических тканей следует применять «открытое» дренирование двухпросветными дренажами по числу отрогов полости, в сочетании с тампонированием полости через операционную рану и оставлением доступа для последующих программных ревизий и некрэктомий в виде оментобурсостомы и (или) люмбостомы. Через дренажи в послеоперационном периоде проводится аспирационно-промывная санация.
Контроль за адекватностью дренирования и состоянием (размерами) дренированных полостей должен проводиться с помощью фистулографии, УЗИ и КТ каждые 7 суток. Неэффективность дренирования (по клинико-инструменальным данным) или появление новых гнойных очагов служит показанием к повторной операции с дополнительной некрэктомией и дренированием.
При развитии аррозивного кровотечения в очаге гнойной деструкции следует произвести ревизию зоны кровотечения, удалить секвестры, прошить место кровотечения (временный гемостаз) и выполнить перевязку сосудов на протяжении вне гнойного очага (окончательный гемостаз). Накладывать швы на стенку сосуда в зоне дефекта в гнойной запрещено. При невозможности лигирования сосудов вне гнойного очага показана дистальная резекция поджелудочной железы и спленэктомия.
Антибактериальная терапия при остром панкреатите.
• Антибиотикопрофилактика не показана у пациентов с тяжелым острым панкреатитом в фазе ферментной токсемии.
• У пациентов в фазе гнойно-септических осложнений эмпирической терапией считается:
Пиперациллин-тазобактам 4.5 г в/в каждые 6 часов
Цефепим 1 г в/в каждые 8 часов ПЛЮС метронидазол 500 мг в/в каждые 8 часов
Ципрофлоксацин 400 мг в/в каждые 12 часов ПЛЮС метронидазол 500 мг в/в каждые 8 часов
Проникновение селективных антибиотиков в поджелудочную железу.
Хорошее (>40%): фторхинолоны, карбапенемы, цефтазидим, цефепим, метронидазол, пиперациллин-тазобактам