Железо — общая характеристика элемента, химические свойства железа и его соединений

Основные степени окисления — +2, +3
Простое вещество железо — ковкий металл серебристо-белого цвета с высокой химической реакционной способностью: железо быстро корродирует при высоких температурах или при высокой влажности на воздухе. В чистом кислороде железо горит, а в мелкодисперсном состоянии самовозгорается и на воздухе.
Химические свойства простого вещества — железа:
Ржавление и горение в кислороде
1) На воздухе железо легко окисляется в присутствии влаги (ржавление):
Накалённая железная проволока горит в кислороде, образуя окалину — оксид железа (II, III):
2) При высокой температуре (700–900°C) железо реагирует с парами воды:
3) Железо реагирует с неметаллами при нагревании:
Fe + S – t° → FeS (600 °С)
4) В ряду напряжений стоит левее водорода, реагирует с разбавленными кислотами НСl и Н2SO4, при этом образуются соли железа(II) и выделяется водород:
Fe + 2HCl → FeCl2 + H2 (реакции проводятся без доступа воздуха, иначе Fe +2 постепенно переводится кислородом в Fe +3 )
В концентрированных кислотах–окислителях железо растворяется только при нагревании, оно сразу переходит в катион Fе 3+ :
(на холоде концентрированные азотная и серная кислоты пассивируют железо).
Железный гвоздь, погруженный в голубоватый раствор медного купороса, постепенно покрывается налетом красной металлической меди
5) Железо вытесняет металлы, стоящие правее его в ряду напряжений из растворов их солей.
Амфотерность железа проявляется только в концентрированных щелочах при кипячении:
и образуется осадок тетрагидроксоферрата(II) натрия.
Техническое железо — сплавы железа с углеродом: чугун содержит 2,06-6,67 % С, сталь 0,02-2,06 % С, часто присутствуют другие естественные примеси (S, Р, Si) и вводимые искусственно специальные добавки (Мn, Ni, Сr), что придает сплавам железа технически полезные свойства — твердость, термическую и коррозионную стойкость, ковкость и др.
Доменный процесс производства чугуна
Доменный процесс производства чугуна составляют следующие стадии:
а) подготовка (обжиг) сульфидных и карбонатных руд — перевод в оксидную руду:
б) сжигание кокса при горячем дутье:
в) восстановление оксидной руды угарным газом СО последовательно:
г) науглероживание железа (до 6,67 % С) и расплавление чугуна:
В чугуне всегда в виде зерен присутствуют цементит Fe2С и графит.
Производство стали
Передел чугуна в сталь проводится в специальных печах (конвертерных, мартеновских, электрических), отличающихся способом обогрева; температура процесса 1700-2000 °С. Продувание воздуха, обогащенного кислородом, приводит к выгоранию из чугуна избыточного углерода, а также серы, фосфора и кремния в виде оксидов. При этом оксиды либо улавливаются в виде отходящих газов (СО2, SО2), либо связываются в легко отделяемый шлак — смесь Са3(РO4)2 и СаSiO3. Для получения специальных сталей в печь вводят легирующие добавки других металлов.
Получение чистого железа в промышленности — электролиз раствора солей железа, например:
(существуют и другие специальные методы, в том числе восстановление оксидов железа водородом).
Чистое железо применяется в производстве специальных сплавов, при изготовлении сердечников электромагнитов и трансформаторов, чугун — в производстве литья и стали, сталь — как конструкционный и инструментальный материалы, в том числе износо-, жаро- и коррозионно-стойкие.
FеО + Н2 =Н2O + Fе (особо чистое) (350°С)
FеО + С(кокс) = Fе + СО (выше 1000 °С)
FеО + СО = Fе + СO2 (900°С)
Получение в лаборатории: термическое разложение соединений железа (II) без доступа воздуха:
FеСОз = FеО + СO2 (490-550 °С)
2(Fe II Fe2 III )O4 = 6FеО + O2 (выше 1538 °С)
(Fe II Fe2 III )O4 + 4Н2 = 4Н2O + 3Fе (особо чистое, 1000 °С)
Получение: сгорание железа (см.) на воздухе.
В природе — оксидная руда железа магнетит.
Оксид железа(III) Fе2О3. Амфотерный оксид с преобладанием основных свойств. Красно-коричневый, имеет ионное строение (Fе 3+ )2(O 2- )3. Термически устойчив до высоких температур. Не образуется при сгорании железа на воздухе. Не реагирует с водой, из раствора выпадает бурый аморфный гидрат Fе2O3 nН2О. Медленно реагирует с кислотами и щелочами. Восстанавливается монооксидом углерода, расплавленным железом. Сплавляется с оксидами других металлов и образует двойные оксиды — шпинели (технические продукты называются ферритами). Применяется как сырье при выплавке чугуна в доменном процессе, катализатор в производстве аммиака, компонент керамики, цветных цементов и минеральных красок, при термитной сварке стальных конструкций, как носитель звука и изображения на магнитных лентах, как полирующее средство для стали и стекла.
Уравнения важнейших реакций:
Получение в лаборатории — термическое разложение солей железа (III) на воздухе:
В природе — оксидные руды железа гематит Fе2O3 и лимонит Fе2O3 nН2O
Гидроксид железа (II) Fе(ОН)2. Амфотерный гидроксид с преобладанием основных свойств. Белый (иногда с зеленоватым оттенком), связи Fе — ОН преимущественно ковалентные. Термически неустойчив. Легко окисляется на воздухе, особенно во влажном состоянии (темнеет). Нерастворим в воде. Реагирует с разбавленными кислотами, концентрированными щелочами. Типичный восстановитель. Промежуточный продукт при ржавлении железа. Применяется в изготовлении активной массы железоникелевых аккумуляторов.
Уравнения важнейших реакций:
Получение: осаждение из раствора щелочами или гидратом аммиака в инертной атмосфере:
Метагидроксид железа FеО(ОН). Амфотерный гидроксид с преобладанием основных свойств. Светло-коричневый, связи Fе — О и Fе — ОН преимущественно ковалентные. При нагревании разлагается без плавления. Нерастворим в воде. Осаждается из раствора в виде бурого аморфного полигидрата Fе2O3 nН2O, который при выдерживании под разбавленным щелочным раствором или при высушивании переходит в FеО(ОН). Реагирует с кислотами, твердыми щелочами. Слабый окислитель и восстановитель. Спекается с Fе(ОН)2. Промежуточный продукт при ржавлении железа. Применяется как основа желтых минеральных красок и эмалей, поглотитель отходящих газов, катализатор в органическом синтезе.
Соединение состава Fе(ОН)3 не известно (не получено).
Уравнения важнейших реакций:
2FеО(ОН) + ЗН2 = 4Н2O+ 2Fе (особо чистое, 500—600 °С)
Получение: осаждение из раствора солей железа(Ш) гидрата Fе2О3 nН2O и его частичное обезвоживание (см. выше).
В природе — оксидная руда железа лимонит Fе2O3 nН2О и минерал гётит FеО(ОН).
Феррат калия К2FеО4. Оксосоль. Красно-фиолетовый, разлагается при сильном нагревании. Хорошо растворим в концентрированном растворе КОН, реагирует с кипящей водой, неустойчив в кислотной среде. Сильный окислитель.
Качественная реакция — образование красного осадка феррата бария. Применяется в синтезе ферритов — промышленно важных двойных оксидов железа (III) и других металлов.
Уравнения важнейших реакций:
FеО4 2- + Ва 2+ = ВаFеO4 (красн.)↓ (в конц. КОН)
Получение: образуется при окислении соединений железа, например метагидроксида FеО(ОН), бромной водой, а также при действии сильных окислителей (при спекании) на железо
и электролизе в растворе:
(феррат калия образуется на аноде).
Обнаружение ионов Fе 2+ и Fе 3+ в водном растворе проводят с помощью реактивов К3[Fе(СN)6] и К4[Fе(СN)6] соответственно; в обоих случаях выпадает синий продукт одинакового состава и строения, КFе III [Fе II (СN)6]. В лаборатории этот осадок называют берлинская лазурь, или турнбуллева синь:
Fе 2+ + К + + [Fе(СN)6] 3- = КFе III [Fе II (СN) 6]↓
Fе 3+ + К + + [Fе(СN)6] 4- = КFе III [Fе II (СN) 6]↓
Химические названия исходных реактивов и продукта реакций:
К3Fе III [Fе(СN) 6]- гексацианоферрат (III) калия
К4Fе III [Fе (СN) 6]- гексацианоферрат (II) калия
КFе III [Fе II (СN) 6]- гексацианоферрат (II) железа (Ш) калия
Fе 3+ + 6NСS — = [Fе(NСS)6] 3-
Этим реактивом (например, в виде соли КNСS) можно обнаружить даже следы железа (III) в водопроводной воде, если она проходит через железные трубы, покрытые изнутри ржавчиной.
 |
 |
Важную роль в геохимии железа играют окислительно-восстановительные реакции — переход 2-валентного железа в 3-валентное и обратно. В биосфере при наличии органических веществ Fe3+ восстанавливается до Fe2+ и легко мигрирует, а при встрече с кислородом воздуха Fe2+ окисляется, образуя скопления гидроокисей 3-валентного железа. Широко распространённые соединения 3-валентного железа имеют красный, жёлтый, бурый цвета. Этим определяется окраска многих осадочных горных пород и их наименование — «красно-цветная формация» (красные и бурые суглинки и глины, жёлтые пески и т. д.).
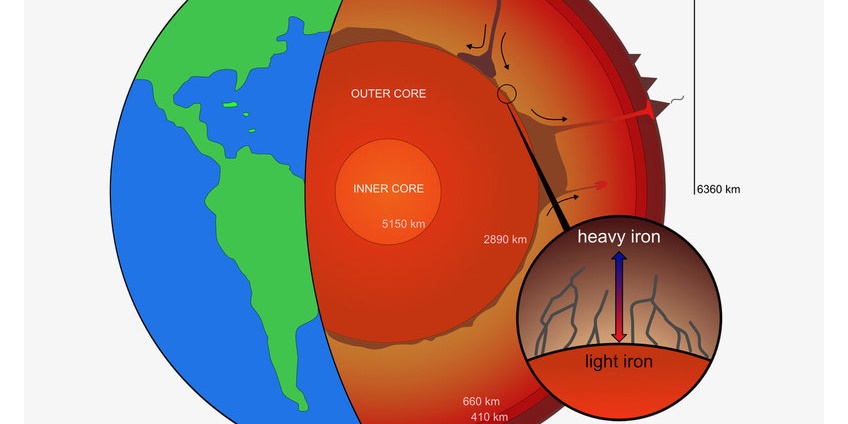
Железо — металл земных глубин, оно накапливается на ранних этапах кристаллизации магмы, в ультраосновных (9,85%) и основных (8,56%) породах (в гранитах его всего 2,7%). В биосфере железо накапливается во многих морских и континентальных осадках, образуя осадочные руды.
Железо входит в состав гемоглобина.
Типы железных руд
Промышленное значение имеют руды с содержанием Fe свыше 16%. Поэтому важнейшими рудными минералами железа являются:
Различают след. осн. типы железных руд.
Железо как материал (железо в технологиях)
Историческая справка о железе
Железо было известно ещё в доисторические времена, однако широкое применение нашло значительно позже, т. к. в свободном состоянии встречается в природе крайне редко, а получение его из руд стало возможным лишь на определённом уровне развития техники.
Вероятно, впервые человек познакомился с метеоритным железом, о чём свидетельствуют его названия на языках древних народов:
В хеттских текстах 14 в. до н. э. упоминается о железе. как о металле, упавшем с неба.
Способ получения железа из руд был изобретён в западной части Азии [Закавказье?] во II тысячелетии до н.э.. Затем применение железа распространилось в Вавилоне, Египте, Греции. Так на смену бронзовому веку пришёл железный век [после окончания Троянской войны в 12-м веке до н.э., когда секрет производства железа узнали от хеттов]. Гомер (в 23-й песне «Илиады») рассказывает, что Ахилл наградил диском из железной крицы победителя в соревновании по метанию диска.
В Европе и Древней Руси в течение многих веков железо получали по сыродутному процессу. Железную руду восстанавливали древесным углём в горне (восстановление металлов), устроенном в яме. Затем в горн мехами нагнетали воздух, а продукт восстановления — крицу ударами молота отделяли от шлака и из неё выковывали различные изделия.
По мере усовершенствования способов дутья и увеличения высоты горна температура процесса повышалась и часть железа науглероживалась, т. е. получался чугун; этот сравнительно хрупкий продукт считали отходом производства. Отсюда название чугуна «чушка», «свинское железо» — английское pig iron. Позже было замечено, что при загрузке в горн не железной руды, а чугуна также получается низкоуглеродистая железная крица, причём такой двухстадийный процесс (кричный передел) оказался более выгодным, чем сыродутный. В 12—13 вв. кричный способ был уже широко распространён. В 14 в. чугун начали выплавлять не только как полупродукт для дальнейшего передела, но и как материал для отливки различных изделий. К тому же времени относится и реконструкция горна в шахтную печь («домницу»), а затем и в доменную печь.
В середине 18 в. в Европе начал применяться тигельный процесс получения стали, который был известен на территории Сирии ещё в ранний период средневековья, но в дальнейшем оказался забытым. При этом способе сталь получали расплавлением металлические шихты в небольших сосудах (тиглях) из высокоогнеупорной массы.
В последней четверти 18 в. стал развиваться пудлинговый процесс передела чугуна в железо на поду пламенной отражательной печи (пудлингование).
Промышленный переворот 18 — начала 19 вв., изобретение паровой машины, строительство железных дорог, крупных мостов и парового флота вызвали громадную потребность в железе и его сплавах. Однако все существовавшие способы производства железа не могли удовлетворить потребности рынка. Массовое производство стали началось лишь в середине 19 в., когда были разработаны бессемеровский, томасовский и мартеновский процессы.
В 20 в. возник и получил широкое распространение электросталеплавильный процесс, дающий сталь высокого качества.
Определение (обнаружение) железа
Получение железа
Чистое железо получают в относительно небольших количествах электролизом водных растворов его солей или восстановлением водородом его окислов. Разрабатывается способ непосредственного получения железа из руд электролизом расплавов. Постепенно увеличивается производство достаточно чистого железа путём его прямого восстановления из рудных концентратов водородом, природным газом или углём при относительно низких температурах.
Применение железа
На основе желеха создаются материалы, способные выдерживать воздействие высоких и низких температур, вакуума и высоких давлений, агрессивных сред, больших переменных напряжений, ядерных излучений и т.п.
Использование железа как художественного материала
Железо как художественный материал использовалось с древности в Египте (подставка для головы из гробницы Тутанхамона около Фив, середина 14 в. до н. э., Музей Ашмола, Оксфорд), Месопотамии (кинжалы, найденные около Кархемиша, 500 до н.э., Британский музей, Лондон), Индии (железная колонна в Дели, 415).
Со времён средневековья сохранились многочисленные высокохудожественные изделия из железа в странах Европы (Англии, Франции, Италии, России и др.) — кованые ограды, дверные петли, настенные кронштейны, флюгера, оковки сундуков, светцы. Кованые сквозные изделия из прутьев и изделия из просечного листового железа (часто со слюдяной подкладкой) отличаются плоскостными формами, чётким линейно-графическим силуэтом и эффектно просматриваются на свето-воздушном фоне.
В 20 веке железо используется для изготовления решёток, оград, ажурных интерьерных перегородок, подсвечников, монументов.
Железо в организме и медицине
Железо присутствует в организмах всех животных и в растениях (в среднем, около 0,02%); оно необходимо, главным образом, для кислородного обмена и окислительных процессов. Почти всё железо в организмах животных и растений связано с белками. Существуют организмы (т.н. концентраторы), способные накапливать его в больших количествах, например, железобактерии — до 17—20% железа [видимо, из их отложений и возникло затем большинство железных руд].
Недостаток и избыток железа в почве и растениях
В земной коре железа сравнительно много — в среднем 4,2%. В разных почвах количество его сильно колеблется, приблизительно в пределах 1—5%. Особенно много железа в южных субтропических почвах (в западной части Грузии и южной части Азербайджана), где окиси железа нередко накопляется до 20 и более процентов. [Недаром в этих местах племя халибов впервые научилось добывать железо]
Среднее содержание железа в растениях приблизительно 0,02%. Общее количество этого элемента в урожаях разных культур колеблется от 1 до 10 кг на гектар.
В щелочных почвах образуются недоступные для усвоения корнями растений соединения железа, и растения не получают его в достаточном количестве [а значит, и животные, и люди]. В кислых почвах железо переходит в растворимые соединения в избыточном количестве. При недостатке или избытке в почвах усвояемых соединений железа, заболевания растений могут наблюдаться на значительных территориях (в некоторых биогеохимических провинциях).
Недостаток железа вызывает задержку роста и явление хлороза растений, связанное с пониженным образованием хлорофилла. При хлорозе листовые пластинки равномерно вначале бледнеют, а затем приобретают желтоватую окраску. Особую чувствительность к недостатку железа обнаруживают почти все плодовые деревья, ягодники и виноград. Страдают также, но в меньшей степени, некоторые полевые и овощные культуры (овес, кукуруза, картофель, томаты и др.).
Вредное влияние на развитие растений оказывает и избыток железа, вызывая, например, стерильность цветков риса и хлороз.
Потребность в железе в организмах животных и человека
В животных организмах железо входит в состав окислительных ферментов и красящего вещества крови (гемоглобин), в котором его количество доходит до 0,47%. Очень важна роль железа в процессах тканевого дыхания, нарушение которых приводит к быстрой гибели животных и человека.
В организм животных и человека железо поступает с пищей (наиболее богаты им печень, мясо, яйца, бобовые, хлеб, крупы, шпинат, свёкла). В норме человек получает с рационом 60—110 мг железа, что значительно превышает его суточную потребность. Всасывание поступившего с пищей железа происходит в верхнем отделе тонких кишок, откуда оно в связанной с белками форме поступает в кровь и разносится к органам и тканям, где депонируется в виде железо-белкового комплекса — ферритина. Основное депо железа в организме — печень и селезёнка.
Выделяется железо из организма, главным образом, через стенку толстых кишок (у человека около 6—10 мг в сутки) и в незначительной степени почками.
Потребность организма в железе меняется с возрастом и физическим состоянием. На 1 кг веса необходимо детям — 0,6, взрослым — 0,1 и беременным — 0,3 мг железа в сутки. У животных потребность в железе ориентировочно составляет (на 1 кг сухого вещества рациона): для дойных коров — не менее 50 мг, для молодняка — 30—50 мг, для поросят — до 200 мг, для супоросных свиней — 60 мг.
Применение железа в медицине и фармакологии
В медицине лекарственные препараты железа (восстановленное железо, лактат железа, глицерофосфат железа, сульфат 2-валентного железа, таблетки Бло, раствор яблочнокислого железа, ферамид, гемостимулин и др.) используют при лечении заболеваний, сопровождающихся недостатком железа в организме (железодефицитная анемия), а также как общеукрепляющие средства (после перенесённых инфекционных заболеваний и др.).
Изотопы железа (52Fe, 55Fe и 59Fe) применяют как индикаторы при медико-биологических исследованиях и диагностике заболеваний крови (анемии, лейкозы, полицитемия и др.).







