что значит в реанимации под кислородом
Что значит в реанимации под кислородом
Проблема поражения легких при вирусной инфекции, вызванной COVID-19 является вызовом для всего медицинского сообщества, и особенно для врачей анестезиологов-реаниматологов. Связано это с тем, что больные, нуждающиеся в реанимационной помощи, по поводу развивающейся дыхательной недостаточности обладают целым рядом специфических особенностей. Больные, поступающие в ОРИТ с тяжелой дыхательной недостаточностью, как правило, старше 65 лет, страдают сопутствующей соматической патологией (диабет, ишемическая болезнь сердца, цереброваскулярная болезнь, неврологическая патология, гипертоническая болезнь, онкологические заболевания, гематологические заболевания, хронические вирусные заболевания, нарушения в системе свертывания крови). Все эти факторы говорят о том, что больные поступающие в отделение реанимации по показаниям относятся к категории тяжелых или крайне тяжелых пациентов. Фактически такие пациенты имеют ОРДС от легкой степени тяжести до тяжелой.
В терапии классического ОРДС принято использовать ступенчатый подход к выбору респираторной терапии. Простая схема выглядит следующим образом: низкопоточная кислородотерапия – высокопоточная кислородотерапия или НИМВЛ – инвазивная ИВЛ. Выбор того или иного метода респираторной терапии основан на степени тяжести ОРДС. Существует много утвержденных шкал для оценки тяжести ОРДС. На наш взгляд в клинической практике можно считать удобной и применимой «Берлинскую дефиницую ОРДС».
Общемировая практика свидетельствует о крайне большом проценте летальных исходов связанных с вирусной инфекцией вызванной COVID-19 при использовании инвазивной ИВЛ (до 85-90%). На наш взгляд данный факт связан не с самим методом искусственной вентиляции легких, а с крайне тяжелым состоянием пациентов и особенностями течения заболевания COVID-19.
Тяжесть пациентов, которым проводится инвазивная ИВЛ обусловлена большим объемом поражения легочной ткани (как правило более 75%), а также возникающей суперинфекцией при проведении длительной искусственной вентиляции.
Собственный опыт показывает, что процесс репарации легочной ткани при COVID происходит к 10-14 дню заболевания. С этим связана необходимость длительной искусственной вентиляции легких. В анестезиологии-реаниматологии одним из критериев перевода на спонтанное дыхание и экстубации служит стойкое сохранение индекса оксигенации более 200 мм рт. ст. при условии, что используются невысокие значения ПДКВ (не более 5-6 см. вод. ст.), низкие значения поддерживающего инспираторного давления (не более 15 см. вод. ст.), сохраняются стабильные показатели податливости легочной ткани (статический комплайнс более 50 мл/мбар), имеется достаточное инспираторное усилие пациента ( p 0.1 более 2.)
Достижение адекватных параметров газообмена, легочной механики и адекватного спонтанного дыхания является сложной задачей, при условии ограниченной дыхательной поверхности легких.
При этом задача поддержания адекватных параметров вентиляции усугубляется присоединением вторичной бактериальной инфекции легких, что увеличивает объем поражения легочной ткани. Известно, что при проведении инвазинвой ИВЛ более 2 суток возникает крайне высокий риск возникновения нозокомиальной пневмонии. Кроме того, у больных с COVID и «цитокиновым штормом» применяются ингибиторы интерлейкина, которые являются выраженными иммунодепрессантами, что в несколько раз увеличивает риск возникновения вторичной бактериальной пневмонии.
В условиях субтотального или тотального поражения дыхательной поверхности легких процент успеха терапии дыхательной недостаточности является крайне низким.
Собственный опыт показывает, что выживаемость пациентов на инвазивной ИВЛ составляет 15.3 % на текущий момент времени.
Алгоритм безопасности и успешности ИВЛ включает:
В связи с тем, что процент выживаемости пациентов при использовании инвазивной ИВЛ остается крайне низким возрастает интерес к использованию неинвазивной искусственной вентиляции легких. Неинвазивную ИВЛ по современным представлениям целесообразно использовать при ОРДС легкой степени тяжести. В условиях пандемии и дефицита реанимационных коек процент пациентов с тяжелой формой ОРДС преобладает над легкой формой.
Тем не менее, в нашей клинической практике у 23% пациентов ОРИТ в качестве стартовой терапии ДН и ОРДС применялась неинвазивная масочная вентиляция (НИМВЛ). К применению НИМВЛ есть ряд ограничений: больной должен быть в ясном сознании, должен сотрудничать с персоналом. Допустимо использовать легкую седацию с целью обеспечения максимального комфорта пациента.
Критериями неэффективности НИМВЛ являются сохранение индекса оксигенации ниже 100 мм рт.ст., отсутствие герметичности дыхательного контура, возбуждение и дезориентация пациента, невозможность синхронизации пациента с респиратором, травмы головы и шеи, отсутствие сознания, отсутствие собственного дыхания. ЧДД более 35/мин.
В нашей практике успешность НИМВЛ составила 11.1 %. Зав. ОАИР: к.м.н. Груздев К.А.
Искусственная вентиляция легких (ИВЛ): инвазивная и неинвазивная респираторная поддержка
К искусственной вентиляции легких (ИВЛ) прибегают для оказания помощи пациентам с острой или хронической дыхательной недостаточностью, когда больной не может самостоятельно вдыхать необходимый для полноценного функционирования организма объем кислорода и выдыхать углекислый газ. Необходимость в ИВЛ возникает при отсутствии естественного дыхания или при его серьезных нарушениях, а также во время хирургических операций под общим наркозом.
Что такое ИВЛ?
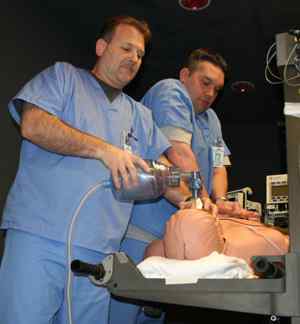
Искусственная вентиляция в общем виде представляет собой вдувание газовой смеси в легкие пациента. Процедуру можно проводить вручную, обеспечивая пассивный вдох и выдох путем ритмичных сжиманий и разжиманий легких или с помощью реанимационного мешка типа Амбу. Более распространенной формой респираторной поддержки является аппаратная ИВЛ, при которой доставка кислорода в легкие осуществляется с помощью специального медицинского оборудования.
Показания к искусственной вентиляции легких
Искусственная вентиляция легких проводится при острой или хронической дыхательной недостаточности, вызванной следующими заболеваниями или состояниями:
Инвазивная вентиляция легких
Эндотрахеальная трубка вводится в трахею через рот или через нос и подсоединяется к аппарату ИВЛ
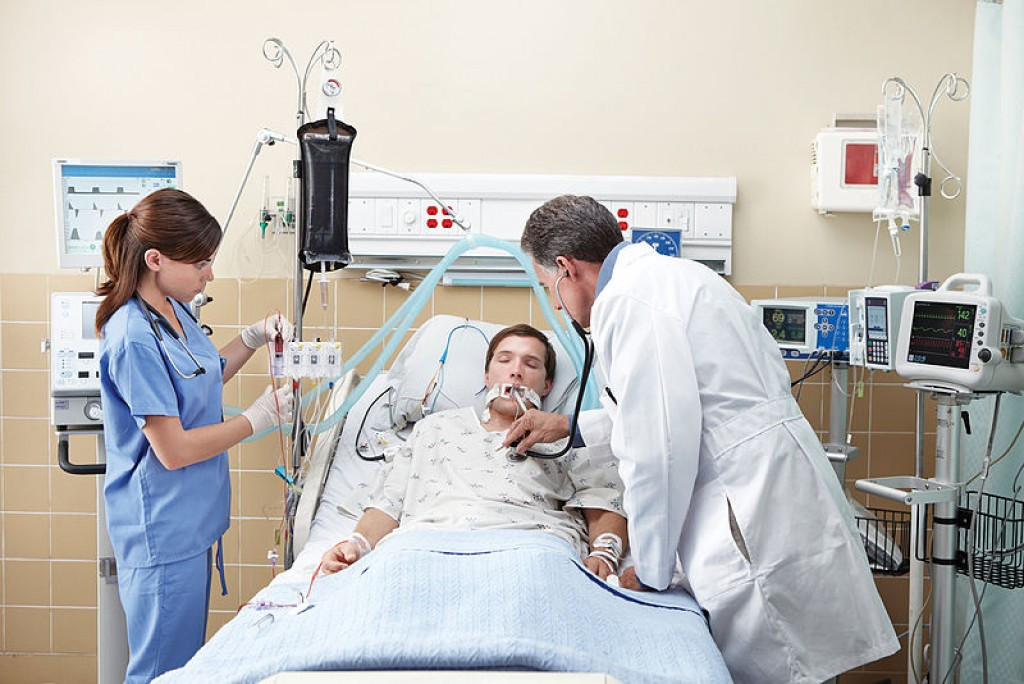
При инвазивной респираторной поддержке аппарат ИВЛ обеспечивает принудительную прокачку легких кислородом и полностью берет на себя функцию дыхания. Газовая смесь подается через эндотрахеальную трубку, помещенную в трахею через рот или нос. В особо критических случаях проводится трахеостомия – хирургическая операция по рассечению передней стенки трахеи для введения трахеостомической трубки непосредственно в ее просвет.
Инвазивная вентиляция обладает высокой эффективностью, но применяется лишь случае невозможности помочь больному более щадящим способом, т.е. без инвазивного вмешательства.
Кому и когда необходима инвазивная ИВЛ?
Подключенный к аппарату ИВЛ человек не может ни говорить, ни принимать пищу. Интубация доставляет не только неудобства, но и болезненные ощущения. Ввиду этого пациента, как правило, вводят в медикаментозную кому. Процедура проводится только в условиях стационара под наблюдением специалистов.
Инвазивная вентиляция легких отличается высокой эффективностью, однако интубация предполагает введение пациента в медикаментозную кому. Кроме того, процедура сопряжена с рисками.
Традиционно инвазивную респираторную поддержку применяют в следующих случаях:
Как работает аппарат инвазивной ИВЛ?
Принцип работы приборов для инвазивной ИВЛ можно описать следующим образом.
Особенности оборудования для инвазивной вентиляции
Оборудование для инвазивной вентиляции легких имеет ряд характерных особенностей.
Неинвазивная вентиляция легких
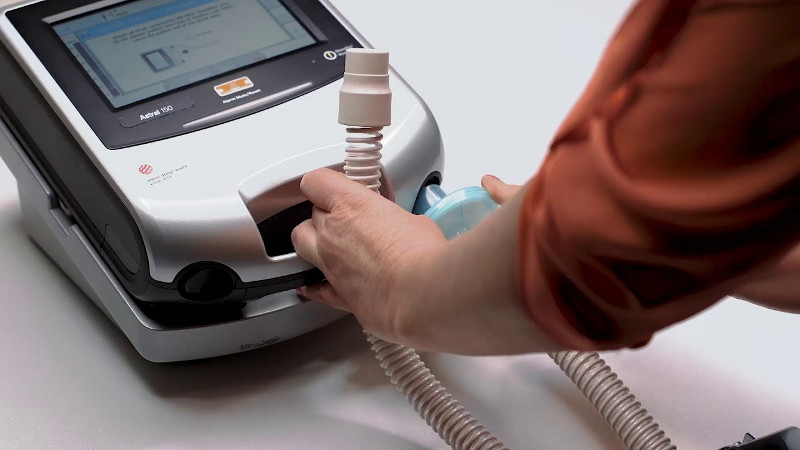
За последние два десятилетия заметно возросло использование оборудования неинвазивной искусственной вентиляции легких. НИВЛ стала общепризнанным и широко распространенным инструментом терапии острой и хронической дыхательной недостаточности как в лечебном учреждении, так и в домашних условиях.
Одним из ведущих производителей медицинских респираторных устройств является австралийская компания ResMed
НИВЛ — что это?
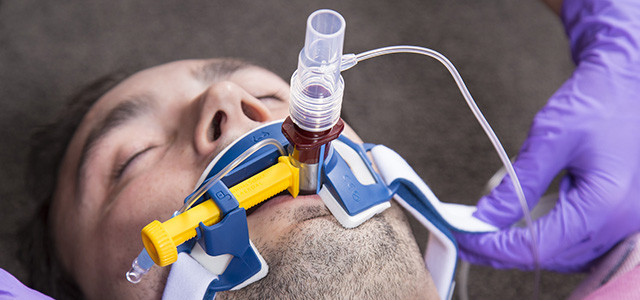
Неинвазивная вентиляция легких относится к искусственной респираторной поддержке без инвазивного доступа (т.е. без эндотрахеальной или трахеостомической трубки) с использованием различных известных вспомогательных режимов вентиляции.
Оборудование подает воздух в интерфейс пациента через дыхательный контур. Для обеспечения НИВЛ используются различные интерфейсы – носовая или рото-носовая маска, шлем, мундштук. В отличие от инвазивного метода, человек продолжает дышать самостоятельно, но получает аппаратную поддержку на вдохе.
Когда применяется неинвазивная вентиляция легких?
Ключом к успешному использованию неинвазивной вентиляции легких является признание ее возможностей и ограничений, а также тщательный отбор пациентов (уточнение диагноза и оценка состояния больного). Показаниями для НИВЛ являются следующие критерии:
Техника реанимации: поддержание дыхания и кровообращения искусственным путем
Основной задачей реанимации является снабжение головного мозга кислородом. Это можно осуществить:
Обе задачи должны выполняться одновременно, однако в дидактических целях мы излагаем здесь эти два способа реанимации отдельно.
Снабжение легких кислородом
Осуществить поступление кислорода в легкие можно различными путями, но в любом случае должно быть соблюдено два условия. Дыхательные пути должны быть свободными. Причиной смерти очень многих людей было западение языка назад, закупорка дыхательных путей аспирированным секретом из желудка. Вторым условием является то, что кислород должен вводиться в дыхательные пути под соответствующим давлением. Вдуваемый через рот или глотку кислород не всегда попадает в альвеолы, а ведь газовый обмен происходит только там.
В Венгрии ежегодно погибает во время аварий около 1500 человек, причем большой процент их не из-за тяжести травм, которые были бы несовместимы с жизнью, а просто от удушья, в результате того, что дыхательные пути оказываются закрытыми запавшим назад языком, кровью, секретом, содержимым желудка.
Именно поэтому непреложным правилом служит то, что реанимация должна в любом случае начинаться с освобождения дыхательных путей. Для этого «умершего» помещают на спину и становятся на колени справа от него. Голова больного резко запрокидывается назад, левой рукой мы открываем его рот и поддерживаем в открытом состоянии. Если рот наполнен слюной или содержимым желудка, его следует освободить от этого содержимого, вытерев слюну или удалив содержимое пальцами. Второй и третий пальцы правой руки просовывают ко входу в гортань, чтобы установить, нет ли там какого-либо чужеродного тела. Если реанимация начата в условиях стационара, в нашем распоряжении, конечно, имеется ларингоскоп и отсасывающий насос. Если же их нет, то указанные выше движения сами по себе часто уже могут спасти больному жизнь.
Самым простым методом вдувания кислорода является дыхание рот в рот или в нос больного. Все мы постоянно носим при себе прекрасный баллон с кислородом под большим давлением — это наши наполненные воздухом легкие. При форсированном выдохе можно легко достигнуть превышения обычного давления на 50—100 мм рт. ст., чего вполне достаточно для раздувания легких недышащего человека. Для этого голова лежащего на спине больного резко запрокидывается назад, левой рукой зажимают больному нос, чтобы вдуваемый воздух не смог выйти через нос, затем, прикладываясь ртом ко рту пострадавшего на возможно более широком его участке, ритмично вдувают в его легкие воздух, совершая 16—20 выдохов в минуту. Между двумя вдуваниями на мгновение отнимают рот ото рта больного, чтобы дать возможность вдутому воздуху выйти из его легких. Многие предпочитают метод вдувания воздуха в нос больному, при этом его губы сжимаются рукой проводящего реанимацию.
Описанный метод далеко не гигиеничен и очень неприятен, но тем более эффективен. Если есть возможность и время, на рот реанимируемого накладывают носовой платок, кусочек марли, бинта и пр., вдувая воздух через них. От всех неприятностей, связанных с вдуванием воздуха рот в рот, освобождает применение тубуса Safar. Его можно легко изготовить самим, соединяя в противоположном направлении две трубки Мауо. Один конец трубки проводящий реанимацию берет в рот, второй ее конец вводится в рот «мертвого». С помощью тубуса можно вдувать воздух в легкие реанимируемого под большим давлением. Это инструмент, которым легко могут пользоваться и те, кто не разбирается в анестезиологии, а потому целесообразно повсюду (в операционной, в приемной, там где проводится бронхоскопия, ректоскопия и т. д.) хранить много таких трубок.
Конечно, легче всего вводить воздух (кислород) в легкие больного («мертвого») через трахеальную трубку. Однако там, где есть такая трубка, как правило, есть и аппарат для наркоза, из которого гораздо проще давать чистый кислород. А потому в крайнем случае трахеальная трубка может использоваться для того, чтобы через нее сделать несколько вдуваний до тех пор, пока не будет подключен аппарат для наркоза и не начнется искусственная вентиляция кислородом.
Несколько эффективнее, чем дыхание методом рот в рот, использование баллона и маски Ambu, с их помощью можно вдувать в легкие реанимируемого чистый или обогащенный кислородом комнатный воздух. Если дыхательные пути свободны, можно в течение длительного времени проводить искусственное дыхание через маску.
Транспорт обогащенной кислородом крови из легких к клеткам головного мозга
Сердце человека, собственно говоря, не что иное как насос, активное сокращение и пассивное расслабление которого поддерживает кровообращение. Если сердце останавливается в состоянии диастолы или из-за мерцания желудочков, то его способность к расслаблению сохраняется неизменной, активное же сокращение может быть вызвано давлением извне. Это давление извне и называют массажем сердца. С его помощью в течение длительного времени, на протяжении многих часов может вызываться активное сокращение сердца. Ниже описываются различные методы массажа сердца.
Наружный (непрямой, трансстернальный) массаж сердца
Этот метод был описан разработавшим его Коn-wenhoven в 1960 году, с тех пор его широко применяют во всем мире. Метод очень прост. На нижнюю часть грудины реанимируемого, лежащего на спине, накладывается ладонь одной руки, а на тыльную сторону ее почти под прямым углом помещается вторая рука. Обеими руками, резкими, внезапными движениями надавливают на грудину 60—70 раз в мин. При этом грудина должна опуститься на 3—5 см. Руки должны двигаться только в локтевом суставе, чтобы можно было использовать давление веса тела производящего реанимацию.
Давление должно выполняться с такой силой, чтобы сердце, зажатое между грудиной и позвоночником, могло вытолкнуть кровь, но ни грудина, ни ребра при этом не должны быть повреждены, не должна повреждаться и печень. У детей, костно-хрящевая грудная стенка которых очень эластична, эффективный сердечный массаж может быть проведен и без приложения большой силы. У пожилых же больных с эмфиземой и негибкой грудной стенкой часто приходится прикладывать такую силу, что избежать перелома одного-двух ребер почти не удается.
Эффективность наружного массажа сердца может быть повышена различными путями. Проще всего достигнуть этого, положив больного на твердую основу, например, подложив под него доску, положить его на пол. Если сдавливание грудной стенки осуществляется на твердой основе, как бы с двух сторон, эффективность массажа повышается.
Повысить эффективность можно и постоянным надавливанием одной рукой на живот больного, это может выполнить ассистент. Этим простым путем оказывается разносторонняя помощь в реанимации:
Кроме этого сдавливание брюшной части аорты способствует более эффективной циркуляции крови в голове и туловище.
Можно осуществить постоянное давление на живот пострадавшего — особенно, если это ребенок — и без помощи ассистента. При этом одновременно одной рукой сдавливают грудину, а другой постоянно надавливают на живот. Лучше же, однако, — особенно у взрослых, когда требуется приложение большой силы, — чтобы массаж сердца проводился двумя руками, а давление на живот пострадавшего оказывал другой человек.
Внутренний (прямой, трансторакальный) массаж сердца
В случаях, когда закрытым массажем сердца не удается поддержать или восстановить кровообращение, может быть показан открытый массаж сердца.
Грудная полость вскрывается в IV, V или VI межреберье на левой стороне. Одним разрезом рассекается кожа и мышцы, покрывающие костную грудную стенку, вторым — открывается грудная полость в межреберье. В это время кровяного давления нет, а потому нет и кровотечения, пережатия сосудов, наложения лигатур не требуется. Вмешательство проводится в нестерильных условиях, без положенного предварительного мытья рук и соблюдения обязательных правил асептики.
Когда вскрыта левая часть грудной полости, начинают массаж сердца через закрытый перикард. Несколькими быстрыми сдавливающими движениями способствуют поступлению крови в головной мозг, затем перед и параллельно ходу диафрагмального нерва вскрывают перикард и продолжают массаж, непосредственно взяв сердце в руки.
Известны и используются несколько методов прямого массажа сердца. Если сердце небольших размеров, его можно взять в одну руку, совершая оппонирующие движения большим пальцем, противопоставленным остальным четырем, опорожняют желудочки. Можно ритмическими движениями прижимать сердце и к задней поверхности грудины.
Массаж сердца обеими руками проводят, помещая правую руку позади сердца, а левую — на переднюю его поверхность и ритмично надавливая двумя ладонями в направлении их друг к другу. Это наиболее щадящий метод.
Какой бы метод массажа нами ни применялся, нужно следить за тем, чтобы
Какой бы вид массажа сердца ни проводился — наружный или внутренний, убедиться в его эффективности можно, если другое лицо в это время прощупывает пульс над сонной или бедренной артерией пострадавшего. Если оказываемое нами сжатие сердца достаточно сильное, то пульс будет отчетливо прощупываться на вышеуказанных артериях, одновременно будет отмечаться и сужение зрачков.
В ходе эффективного массажа сердца рана внезапно начинает кровоточить, и, если при торакотомии была перерезана и внутренняя грудная артерия, кровь из нее начнет бить толчками. Продолжая массаж, необходимо зажать и перевязать кровоточащие сосуды. Теперь мы уже располагаем временем и для того, чтобы обмыть и изолировать кожу вокруг торакотомического отверстия, чтобы помогающий нам второй врач как следует вымыл руки, надел стерильный халат, стерильные резиновые перчатки и взял на себя проведение дальнейшего массажа сердца уже в стерильных условиях. Лучше всего, если каждые 4—5 мин врача, массирующего сердце, меняют, поэтому неплохо, если массаж проводят два, а то и три врача. Тем самым достигается не только большая эффективность вмешательства, но снижается и возможность побочных повреждений.
После успешной реанимации грудная полость промывается антисептиком или антибиотиками, в нее помещается отсасывающий дренаж, рана закрывается послойно.
Часто задают вопрос: когда проводящий реанимацию врач должен прибегнуть к торакотомии? Многолетний опыт показывает, что наружный и внутренний массаж сердца приблизительно одинаково способствуют восстановлению кровотока. Однако при наружном массаже чаще отмечаются повреждения грудной стенки (переломы грудины, ребер), при внутреннем же — чаще страдает само сердце, следовательно, после эффективного наружного массажа работа сердца будет лучше, чем после эффективного внутреннего массажа.
Поэтому нам думается, что в любом случае внезапной остановки сердца, лучше начинать с наружного сердечного массажа. Это правило имеет всего лишь несколько исключений, когда необходимо немедленно прибегнуть к внутреннему массажу сердца:
Восстановление спонтанной сердечной деятельности
Если реанимация начата немедленно после обнаружения остановки сердца, причин для спешки больше нет. Можно спокойно обдумать дальнейшие действия. Ближайшей задачей является восстановление спонтанной сердечной деятельности. Метод выбирается в соответствии с тем, в каком состоянии находится сердце.
При мерцании желудочков хорошим прогностическим признаком служит величина мерцательных волн. Чем грубее волны и ниже частота фибрилляции желудочков, тем лучше прогноз, и чем тоньше волны и выше частота мерцаний, тем хуже прогноз. Часто под влиянием уже кратковременного массажа сердце переходит из состояния крупноволновой фибрилляции желудочков к нормальному синусовому ритму. Нужно обращать внимание на цвет сердца, ибо оживить можно только хорошо оксигенизированное сердце розового цвета.
В случае внутренней дефибрилляции два металлических электрода, как правило, имеют изогнутую форму, что позволяет им лучше прилегать к сердцу. Если электрод соприкасается с сердцем лишь на небольшой поверхности, то вместо дефибрилляции произойдет ожог сердечной мышцы, словно мы коснулись ее диатермическим ножом.
При открытой грудной клетке, если электроды дефибриллятора накладываются на сердце непосредственно, нужно обязательно следить за тем, чтобы они прикасались к нему всей своей поверхностью и чтобы при этом сердце было как можно меньше сдвинуто со своего места. При наружной дефибрилляции используются электроды с прямой поверхностью.
Под действием удара тока сердце делает «скачок», в скелетной мускулатуре возникают клонические судороги. Эти судороги могут быть предупреждены введением сукцинилхолина.
Большие дозы медикамента во время реанимации скорее вредят, чем помогают. Путем медикаментозного воздействия можно достигнуть двоякой цели:
Поскольку эти два состояния исключают друг друга, при выборе медикаментозного лечения также следует избрать тот или иной путь.
Наиболее эффективным средством тонизации сердечной мускулатуры является тоноген (адреналин). Его можно вводить внутривенно, а при открытой грудной клетке в любую полость сердца в дозе 0,5—1,0 мг. Введение таких доз повторяется каждые 10 мин вплоть до введения общей дозы в 10 мг. Тоноген помогает парализованным артериолам вернуть свой прежний тонус. Тем самым поднимается диастолическое кровяное давление, что, в свою очередь, повышает среднее артериальное давление, определяющее степень кровотока в органах и тканях. Кроме этого адреналин оказывает и положительное инотропное действие, способствует восстановлению спонтанной сократительной способности сердечной мышцы и, если сердце возобновило деятельность, повышает его силу.
В последнее время вместо тоногена или вперемежку с ним тонизируют сердце препаратом изо-протеренола — изупрелом, ибо это менее грубое средство, которое может повторно вводиться в течение продолжительного времени. Доза его в разведении составляет 0,2 мг внутривенно или 0,02 мг интракардиально.
Благоприятное тонизирующее воздействие на атоническое сердце оказывают и ионы кальция (Са ++ ): они тотчас же и в значительной мере повышают силу сердечных сокращений. Поэтому следует как можно раньше вводить кальций. При наружном массаже он вводится внутривенно или через грудную стенку длинной иглой в полость сердца, при внутреннем — прямо в полость левого желудочка. Однократная доза 10% раствора хлористого кальция составляет до 20 мл, причем она может вводиться повторно через короткие промежутки времени.
В целях прекращения ацидоза кроме тонизирующих средств необходимо и введение буфера. При низкой рН проводить реанимацию значительно труднее, чем при нормальной величине рН (ок. 7,4). Чаще всего с этой целью вводят гидрокарбонат натрия, но можно вводить и лактат и ТГАМ (три-гидрометиламинометан). Как правило, на 1 кг веса вводится 1 мэкв буфера, что является минимальной начальной дозой.
В случае повышенной возбудимости мышцы сердца, если мерцание желудочков не удается прекратить даже повторными ударами тока, нужно предполагать возможность гипокалиемии. В таких случаях, даже при отсутствии анализа содержания калия в сыворотке, можно спокойно вводить 1,0 — даже 2,0 г хлорида калия внутривенно или в полость сердца. Наряду с этим повышенная возбудимость может быть снижена и с помощью таких препаратов, как лидокаин, прокаинамид, индерал.
Применяя антиаритмические средства, нельзя забывать о том, что все они снижают сократительную способность сердца (функцию «насоса») и, естественно, кровяное давление у больного.>
Оксигенотерапия. Цели, методы и механизм воздействия.
Оксигенотерапия (кислородотерапия) – это применение кислорода в целях лечения и профилактики заболеваний – прежде всего, дыхательной и сердечнососудистой систем. Что также положительно влияет на остальные органы человека.
Кислородотерапия относится к наиболее важным, жизнеспасающим методам лечения угрожающих и тяжелых состояний. Как и всякое лекарственное средство, O2 требует соблюдения правильного дозирования, четких показаний к назначению. Важное значение имеют методы доставки O2. Неадекватное дозирование O2 и отсутствие мониторинга кислородотерапии могут привести к серьезным последствиям.
Кратковременное дыхание концентрированным медицинским кислородом положительно влияет на весь организм и может использоваться в прафилактических целях ежедневно, без наблюдения врача. Рекомендуется дышать не более 2 минут за сеанс и не более 3-х раз в день с интервалами в несколько часов. Для профилактики достаточно одного раза в день по 2 минуты. При соблюдении дозирования, ежедневная кратковременная оксигенотерапия даёт сильное укрепление иммунной системы и оказывает воздействие на все жизненноважные органы. Обладает антисептическим действием, поэтому при дыхании происходит обеззараживание слизистой. Кислород способствует расщеплению жировых клеток. Из за чего воздействует положительно на всю сердечнососудистую систему и способствует похуданию. Увеличивает кровоток к мозгу, что даёт не мало положительных эффектов: снятие головных болей, уменьшение стресса, ясность ума, концентрация внимания, лёгкое пробуждение утром и крепкий сон ночью. Кислород способствует интоксикации организма, выводит шлаки и вытесняет вредные газы, например угарный газ.
При кратковременной профилактической оксигенотерапии противопоказаний нет!
ВАЖНО — все положительные эффекты кратковременного дыхания концентрированным кислородом можно получить используя только чистый медицинский кислород в баллонах.
Концентраторы кислорода не дают нужной концентрации и чистоты кислорода, а также недостаточный поток также будет снижать его концентрацию. Концентраторы кислорода хорошо подходят для длительной Оксигенотерапии и только по рекомендации врача. Можно использовать кислородные баллончики, но у них есть ряд существенных недостатов: стоимость процедуры дыхания существенно выше, и не всегда в маленьких баллончиках с кислородом находится медицинский кислород, зачастую его получают при помощи концентраторов, после чего сжимают и заправляют в баллон. Обязательно и необходимо проверять сертификаты на продукцию и уточнять какой кислород и какой концентрации заправлен в маленький кислородный баллончик.
Способ получения высоко очищенного Медицинского кислорода.
Медицинский кислород получается путем низкотемпературной(криогенной) ректификации, когда перерабатываемый воздух сжимается и благодаря разности температур кипения кислорода (–183 °C), азота (–195,8 °C) и аргона (–185,8°C) разделяется. В настоящее время криогенные технологии значительно усовершенствованы. Внедрение в установку низкотемпературной(криогенной) ректификации дополнительного модуля очистки – адсорбера с цеолитом позволяет не только получить кислород высокой степени очистки и объемной концентрации, но и другие газы, в частности азот и аргон.
При получении кислорода низкотемпературной(криогенной) ректификацией, атмосферный воздух, проходя через фильтры, очищается от пыли и механических примесей, а затем компримируется и последовательно подается в масловлагоотделитель, теплообменникожижитель и блок осушки. Влага, содержащаяся в воздухе, конденсируется и периодически отводится в атмосферу. Далее воздух проходит через молекулярные сита из цеолита, которые адсорбируют оставшуюся влагу, углекислый газ, ацетилен и другие примеси. Очищенный от примесей воздух подается в предварительный теплообменник для предварительного охлаждения, а затем одна часть воздуха подается в теплообменник, а вторая – турбодекантер. После этого они объединяются и поступают в нижнюю ректификационную колонну. В нижней части ректификационной колонны происходит предварительное разделение газов воздуха на обогащенную кислородом (кубовую) жидкость и азотную флегму с кислородом. Далее обогащенная кислородом жидкость разделяется на жидкий кислород (в поддоне) и чистый азот (в верхней части колонны), которые в последствие разделяется на жидкий и газообразный азот и газообразный кислород. В то время, когда насыщенная аргоном жидкость в средней части колонны поступает на следующую криогенную ректификационную колонну, газообразный кислород проходит в кислородный теплообменник и подается на участок наполнения баллонов, а жидкий кислород из нижней части ректификационной колонны сливается в резервуар (конструктивно – «сосуд Дьюара»2). Насыщенная аргоном жидкость из средней части колонны поступает на дополнительную криогенную ректификацию для получения жидкого аргона или, проходя через газификатор, превращается в газообразный аргон.
Способ низкотемпературной(криогенной) ректификацией получения медицинского кислорода является наиболее распространенным, а современное криогенное оборудование обеспечивает необходимое качество готового продукта и полное отсутствие в нем таких примесей как ацетилен, масло, газообразные кислоты и основания, а также газы-окислители. Качество медицинского кислорода регламентируется ГОСТами 6331-78 «Кислород жидкий медицинский. Технические условия» и 5583-78 «Кислород газообразный медицинский. Технические условия».
Применение O2 является наиболее патофизиологически обоснованным методом терапии гипоксемии. Кроме того, кислородотерапия примененяется при некоторых состояниях, не сопровождающихся снижением РаO2: при легочной гипертензии, отравлении угарным газом, пневмотораксе и т.п.
Механизм действия
Проникновение O2 через альвеоло-капиллярную мембрану осуществляется путем простой диффузии, т.е. из области высокого в область низкого парциального давления. O2 переносится к тканям в двух формах: связанный с гемоглобином и растворенный в плазме. При нормальных физиологических условиях (РаO2 = 100 мм рт. ст.) в 100 мл крови растворяется 0,31 мл O2, т.е. 0,31 об.%. Такое количество O2 не в состоянии обеспечить потребности в нем организма человека, поэтому основное значение имеет другой способ переноса — в соединении с гемоглобином в эритроцитах. 1 г гемоглобина способен связать до 1,34 мл О2. Учитывая, что нормальное содержание гемоглобина составляет 15г/дл, можно рассчитать, что в 100 мл крови максимально может содержаться 201 мл О2, связанного с гемоглобином. Наиболее важным параметром, определяющим количество О2, связанного с гемоглобином, является насыщение гемоглобина кислородом (SаO2). При РаO2, 100 мм рт. ст. SаО2 артериальной крови составляет около 97%.
В зависимости от пути введения кислорода способы оксигенотерапии разделяют на два основных вида:
Ингаляционная кислородотерапия включает все способы введения кислорода в легкие через дыхательные пути. Наиболее распространенный метод оксигенотерапии – ингаляция кислорода и кислородных смесей. Ингаляция осуществляется с помощью различной кислородно-дыхательной аппаратуры через носовые и ротовые маски, носовые катетеры, интубационные и трахеотомические трубки или одноразовые мундштуки для кратковременной кислородотерапии в домашних условиях.
Ингаляционные способы подачи кислорода
Оксигенотерапия может проводиться как в клинических, так и в домашних условиях. Дома можно использовать концентраторы, подушки или баллоны. Эти способы показаны для длительной кислородной терапии, но назначать лечение и выбирать метод может только специалист. Неправильное использование кислородных смесей может быть опасно! Для кратковременной процедуры оксигенотерапии необходимо использовать специальное оборудование подающие концентрированный медицинский кислород из баллона, при обязательном соблюдении рекомендаций по длительности и частоте процедур данного устройства.
В клинических условиях есть следующие виды подачи:
Носовые катетеры. При использовании носовых канюль или катетеров поток кислорода от 1 до 6 л/мин создает во вдыхаемом воздухе его концентрацию, равную 24—44 %. Более высокие значения FiO2 достигаются при нормальной минутной вентиляции легких (5—6 л/мин). Если минутная вентиляция превышает поток кислорода, то избыток последнего будет сбрасываться в атмосферу, а FiO2 окажется сниженной. Носовые катетеры обычно хорошо переносятся больными. Их не следует применять при высокой ЧД и гиповентиляции.
Носовые и лицевые маски. Маски снабжены клапанами, с помощью которых выдыхаемый воздух выводится в окружающую среду. Более удобны для пациента носовые маски. Последние имеют меньшее мертвое пространство и позволяют пациенту принимать пищу. Достоинством лицевых масок является их способность лучше справляться с непреднамеренной утечкой потока кислорода через рот, что является проблемой для многих больных. Они могут быть использованы даже в тех случаях, когда словесный контакт с пациентом ограничен. Оба типа масок эффективны у больных с ОДН, однако в острых ситуациях лицевые маски предпочтительнее. Лицевые маски могут быть использованы у больных с более выраженными нарушениями сознания. Стандартные лицевые маски позволяют подавать кислород до 15 л/мин и, соответственно, обеспечивать более высокую FiO2 (50—60 %). У больных с высокой минутной вентиляцией легких применение масок, как и катетеров, ограничено.
Неингаляционная кислородотерапия
Газовый состав для оксигенотерапии обычно содержит 50-60% (до 80%) кислорода, но в некоторых случаях используют другие соотношения. Показание к применению карбогена (95% кислорода и 5% углекислого газа) – отравление угарным газом. При отеке легких с выделением пенистой жидкости газовую смесь пропускают через пеногаситель (50%-й р-р этилового спирта).
Самый безопасный состав для длительной оксигенотерапии содержит 40-60% кислорода. Чистый кислород при длительной оксигенотерапии способен вызывать ожоги дыхательных путей (при процедуре более 30 минут). Он также может быть токсичным для человека, что проявляется в виде сухости во рту, боли в груди, судорог, потери сознания. Поэтому подача чистого концентрированного медицинского кислорода в домашних условиях ограничена самим аппаратом по 1-2 минуты. Хотя безопасное время процедуры считается до 15 минут. Аппараты для дыхания чистым концентрированным медицинским кислородом обязательно должны иметь увлажнитель кислородного потока.
Основные правила кислородотерапии: